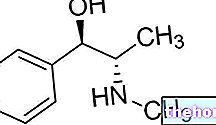
सक्रिय तत्व: कैपेसिटाबाइन
ज़ेलोडा 500 मिलीग्राम फिल्म-लेपित गोलियां
Xeloda पैकेज आवेषण पैक आकार के लिए उपलब्ध हैं:- ज़ेलोडा 150 मिलीग्राम फिल्म-लेपित गोलियां
- ज़ेलोडा 500 मिलीग्राम फिल्म-लेपित गोलियां
ज़ेलोडा का उपयोग क्यों किया जाता है? ये किसके लिये है?
ज़ेलोडा 'साइटोस्टैटिक दवाएं' नामक दवाओं के एक समूह से संबंधित है, जो कैंसर कोशिकाओं के विकास को रोकता है। ज़ेलोडा में 150 मिलीग्राम कैपेसिटाबाइन होता है, जो स्वयं एक साइटोस्टैटिक दवा नहीं है। केवल एक बार शरीर द्वारा अवशोषित कर लिया जाता है, यह एक सक्रिय एंटीकैंसर दवा (सामान्य ऊतकों की तुलना में ट्यूमर के ऊतकों में अधिक हद तक) में बदल जाता है।
Xeloda डॉक्टरों द्वारा बृहदान्त्र, मलाशय, पेट या स्तन के कैंसर के इलाज के लिए निर्धारित है। इसके अलावा, ज़ेलोडा को ट्यूमर के पूर्ण शल्य चिकित्सा हटाने के बाद नए कोलन कैंसर को प्रकट होने से रोकने के लिए निर्धारित किया गया है।
ज़ेलोडा का उपयोग अकेले या अन्य दवाओं के साथ संयोजन में किया जा सकता है।
ज़ेलोडा का सेवन कब नहीं करना चाहिए
ज़ेलोडा न लें:
- यदि आपको कैपेसिटाबाइन या इस दवा के किसी अन्य तत्व से एलर्जी है (धारा ६ में सूचीबद्ध)। आपको अपने डॉक्टर को बताना चाहिए कि क्या आप जानते हैं कि आपको एलर्जी है या इस दवा के प्रति अधिक प्रतिक्रिया है,
- यदि आपको फ़्लोरोपाइरीमिडीन थेरेपी (फ्लूरोरासिल जैसी कैंसर-रोधी दवाओं का एक समूह) के लिए पिछली गंभीर प्रतिक्रिया हुई हो,
- यदि आप गर्भवती हैं या स्तनपान कराती हैं,
- यदि आपके रक्त में श्वेत रक्त कोशिकाओं और प्लेटलेट्स का स्तर अत्यधिक कम है (ल्यूकोपेनिया, न्यूट्रोपेनिया या थ्रोम्बोसाइटोपेनिया),
- अगर आपको लीवर या किडनी की गंभीर समस्या है,
- यदि आपके पास यूरैसिल और थाइमिन के चयापचय में शामिल एंजाइम डाइहाइड्रोपाइरीमिडीन डिहाइड्रोजनेज (डीपीडी) की ज्ञात कमी है या
- यदि आपका वर्तमान में इलाज किया जा रहा है या पिछले 4 हफ्तों के भीतर ब्रिवुडिन, सोरिवुडिन या समान वर्गों के पदार्थों के साथ हर्पीस ज़ोस्टर (चिकन पॉक्स या सेंट एंथोनी की आग) के उपचार के हिस्से के रूप में इलाज किया गया है।
ज़ेलोडा लेने से पहले आपको क्या जानना चाहिए?
Xeloda लेने से पहले अपने डॉक्टर या फार्मासिस्ट से बात करें:
- अगर आपको किडनी या लीवर की बीमारी है,
- यदि आपको हृदय की समस्या है या है (उदाहरण के लिए, अनियमित हृदय गति या छाती से जबड़े तक दर्द और इसके विपरीत शारीरिक परिश्रम के कारण और हृदय में रक्त के प्रवाह में समस्या के कारण),
- यदि आपको मस्तिष्क की बीमारी है (उदाहरण के लिए एक ट्यूमर जो मस्तिष्क में फैल गया है) या तंत्रिका क्षति (न्यूरोपैथी),
- यदि आपके पास कैल्शियम के स्तर में असंतुलन है (जिसे रक्त परीक्षण में देखा जा सकता है),
- अगर आपको मधुमेह है,
- यदि आप गंभीर मतली और उल्टी के कारण अपने शरीर में भोजन या पानी नहीं रख सकते हैं,
- यदि आप दस्त से पीड़ित हैं,
- यदि आप निर्जलित हैं या हो सकते हैं,
- यदि आपके रक्त में आयन असंतुलन है (इलेक्ट्रोलाइट असंतुलन, जो रक्त परीक्षण में पाया जा सकता है),
- यदि आप आंखों की समस्याओं से पीड़ित हैं क्योंकि आपको अतिरिक्त आंखों की निगरानी की आवश्यकता हो सकती है।
- यदि आपकी त्वचा की गंभीर प्रतिक्रिया है।
डायहाइड्रोपाइरीमिडीन डिहाइड्रोजनेज (डीपीडी) की कमी: डीपीडी की कमी जन्म के समय मौजूद एक दुर्लभ बीमारी है जो आमतौर पर स्वास्थ्य समस्याओं से जुड़ी नहीं होती है जब तक कि कुछ दवाएं नहीं ली जाती हैं।यदि आपके पास अज्ञात डीपीडी की कमी है और ज़ेलोडा ले रहे हैं, तो धारा 4 "संभावित दुष्प्रभाव" में सूचीबद्ध दुष्प्रभाव गंभीर रूप में हो सकते हैं। अपने चिकित्सक को बताएं कि क्या कोई भी दुष्प्रभाव आपको चिंतित करता है या यदि आपको कोई साइड इफेक्ट दिखाई देता है जो इस पत्रक में सूचीबद्ध नहीं है (खंड 4 "संभावित दुष्प्रभाव" देखें)।
बच्चे और किशोर
Xeloda बच्चों और किशोरों के इलाज के लिए संकेत नहीं दिया गया है। बच्चों और किशोरों को ज़ेलोडा न दें।
कौन सी दवाएं या खाद्य पदार्थ Xeloda के प्रभाव को बदल सकते हैं?
अन्य दवाएं और ज़ेलोडा
उपचार शुरू करने से पहले, अपने डॉक्टर या फार्मासिस्ट को बताएं कि क्या आप ले रहे हैं, हाल ही में लिया है या कोई अन्य दवा ले सकते हैं। यह मौलिक महत्व का है, क्योंकि कई दवाओं के सहवर्ती सेवन से उनके प्रभाव को मजबूत या कम किया जा सकता है। सहवर्ती सेवन के मामले में विशेष ध्यान दिया जाना चाहिए:
- गाउट दवाएं (एलोप्यूरिनॉल),
- दवाएं जो रक्त को पतला करती हैं (Coumarin, Warfarin),
- कुछ एंटीवायरल दवाएं (सोरिवुडिन और ब्रिवुडिन),
- दौरे या कंपकंपी (फ़िनाइटोइन) का इलाज करने के लिए दवाएं,
- इंटरफेरॉन अल्फा,
- रेडियोथेरेपी और कैंसर के इलाज के लिए इस्तेमाल की जाने वाली कुछ दवाएं (फोलिनिक एसिड, ऑक्सिप्लिप्टिन, बेवाकिज़ुमैब, सिस्प्लैटिन, इरिनोटेकन),
- फोलिक एसिड की कमी के इलाज के लिए इस्तेमाल की जाने वाली दवाएं।
खाने-पीने के साथ ज़ेलोडा
भोजन के अंत के 30 मिनट के भीतर आपको ज़ेलोडा लेना चाहिए।
चेतावनियाँ यह जानना महत्वपूर्ण है कि:
गर्भावस्था और स्तनपान
उपचार शुरू करने से पहले, अपने चिकित्सक को बताएं कि क्या आप गर्भवती हैं, संदेह है या गर्भवती होने की योजना है। यदि आप गर्भवती हैं या गर्भवती होने का संदेह है तो आपको ज़ेलोडा नहीं लेना चाहिए। ज़ेलोडा लेते समय आपको स्तनपान नहीं कराना चाहिए। इस दवा को लेने से पहले अपने डॉक्टर या फार्मासिस्ट से सलाह लें।
ड्राइविंग और मशीनों का उपयोग
ज़ेलोडा आपको चक्कर, बीमार या थका हुआ महसूस करा सकता है। इसलिए यह संभव है कि ज़ेलोडा मशीनों को चलाने या उपयोग करने की क्षमता को प्रभावित कर सकता है।
ज़ेलोडा में निर्जल लैक्टोज होता है
यदि आपके डॉक्टर ने आपको बताया है कि आपको "कुछ शर्करा के प्रति असहिष्णुता है, तो इस औषधीय उत्पाद को लेने से पहले अपने चिकित्सक से संपर्क करें।
खुराक, विधि और प्रशासन का समय Xeloda का उपयोग कैसे करें: Posology
इस दवा को हमेशा ठीक वैसे ही लें जैसे आपके डॉक्टर या फार्मासिस्ट ने आपको बताया है। यदि आप अनिश्चित हैं, तो अपने डॉक्टर या फार्मासिस्ट से परामर्श लें।
ज़ेलोडा केवल एक डॉक्टर द्वारा निर्धारित किया जाना चाहिए जो एंटीनोप्लास्टिक दवाओं के उपयोग में माहिर हैं।
भोजन के अंत के 30 मिनट के भीतर ज़ेलोडा की गोलियों को पानी के साथ पूरा निगल लिया जाना चाहिए।
आपका डॉक्टर आपके लिए सही खुराक और उपचार के नियम लिखेगा। ज़ेलोडा की खुराक शरीर के सतह क्षेत्र पर आधारित है। इसकी गणना ऊंचाई और वजन से की जाती है। वयस्कों के लिए सामान्य खुराक दिन में दो बार (सुबह और शाम) शरीर की सतह क्षेत्र का 1250 मिलीग्राम / एम 2 है। दो उदाहरण प्रस्तावित हैं: एक व्यक्ति जिसका वजन 64 किलो है और ऊंचाई 1.64 मीटर है शरीर की सतह का क्षेत्रफल 1.7 m2 है और 500 मिलीग्राम की 4 गोलियां और 150 मिलीग्राम की 1 गोली दिन में दो बार लेनी चाहिए। एक व्यक्ति जिसका वजन 80 किलोग्राम और ऊंचाई 1.80 मीटर है, उसके शरीर की सतह का क्षेत्रफल 2.00 मीटर 2 है और उसे चाहिए 500 मिलीग्राम की 5 गोलियां दिन में दो बार लें।
ज़ेलोडा की गोलियां आमतौर पर 14 दिनों के लिए ली जाती हैं, इसके बाद 7 दिनों की आराम अवधि (जिस दौरान कोई टैबलेट नहीं ली जाती है)। ये 21 दिन चिकित्सा के एक चक्र के अनुरूप हैं।
अन्य दवाओं के साथ संयोजन में, सामान्य वयस्क खुराक शरीर की सतह क्षेत्र के 1250 मिलीग्राम / एम 2 से कम हो सकती है और गोलियों को अलग-अलग समय के लिए लेने की आवश्यकता हो सकती है (उदाहरण के लिए हर दिन, बिना किसी आराम अवधि के)।
आपका डॉक्टर आपको बताएगा कि आपको कौन सी खुराक लेनी है, कब लेनी है और कितने समय तक लेनी है।
आपका डॉक्टर प्रत्येक शक्ति के लिए 150 मिलीग्राम और 500 मिलीग्राम की गोलियों का संयोजन लिख सकता है।
- डॉक्टर द्वारा बताई गई गोलियों को सुबह और शाम लें।
- भोजन (नाश्ता और रात का खाना) खत्म करने के 30 मिनट के भीतर गोलियां लें।
- अपने चिकित्सक द्वारा निर्धारित सभी दवाएं लेना महत्वपूर्ण है।
अधिक मात्रा में ज़ेलोडा का अधिक मात्रा में सेवन करने पर क्या करें?
यदि आप अपने से अधिक ज़ेलोडा लेते हैं
यदि आप अपने से अधिक ज़ेलोडा लेते हैं, तो अपनी अगली खुराक लेने से पहले जितनी जल्दी हो सके अपने डॉक्टर से संपर्क करें।
यदि आप अपनी अपेक्षा से अधिक ज़ेलोडा लेते हैं, तो आपको निम्नलिखित दुष्प्रभाव का अनुभव हो सकता है: मतली या उल्टी, दस्त, आंत या मुंह में सूजन या अल्सर, पेट या पेट से दर्द या रक्तस्राव, या अस्थि मज्जा अवसाद (एक निश्चित कमी में कमी) रक्त कोशिकाओं के प्रकार)। अगर आपको इनमें से कोई भी लक्षण मिले तो तुरंत अपने डॉक्टर से संपर्क करें।
यदि आप ज़ेलोडा लेना भूल जाते हैं:
छूटी हुई खुराक न लें और अगली खुराक को दोगुना न करें। इसके बजाय, अपनी सामान्य खुराक जारी रखें और अपने डॉक्टर से संपर्क करें।
यदि आप ज़ेलोडा लेना बंद कर देते हैं:
कैपेसिटाबाइन उपचार को रोकने से कोई दुष्प्रभाव नहीं होता है। कैपेसिटाबाइन को रोकना, यदि आप कौमारिन एंटीकोआगुलंट्स (जैसे फेनप्रोकोमोन युक्त) ले रहे हैं, तो आपके डॉक्टर को एंटीकोआगुलेंट की खुराक बदलने की आवश्यकता हो सकती है।
यदि इस उत्पाद के उपयोग के बारे में आपके कोई और प्रश्न हैं, तो अपने डॉक्टर या फार्मासिस्ट से पूछें।
ज़ेलोडा के दुष्प्रभाव क्या हैं?
सभी दवाओं की तरह, यह दवा दुष्प्रभाव पैदा कर सकती है, हालांकि हर किसी को यह नहीं मिलता है।
ज़ेलोडा को तुरंत लेना बंद कर दें और निम्न में से कोई भी लक्षण विकसित होने पर अपने डॉक्टर से संपर्क करें:
- अतिसार: यदि आपके सामान्य मल त्याग या निशाचर दस्त की तुलना में प्रति दिन 4 या अधिक मल त्याग होता है।
- उल्टी: यदि आप 24 घंटे की अवधि में एक से अधिक बार उल्टी करते हैं।
- जी मिचलाना: यदि आप अपनी भूख खो देते हैं और एक दिन में खाए जाने वाले भोजन की मात्रा सामान्य से बहुत कम है।
- Stomatitis: अगर आपको मुंह या गले में दर्द, लालिमा, सूजन या अल्सर है।
- हाथ-पैर की त्वचा की प्रतिक्रिया: यदि आपके हाथों और/या पैरों में दर्द, सूजन और लालिमा या झुनझुनी है।
- बुखार: यदि आपके शरीर का तापमान 38 डिग्री सेल्सियस या इससे अधिक है।
- संक्रमण: यदि आपके पास बैक्टीरिया या वायरस, या अन्य जीवों से संक्रमण के कोई लक्षण हैं।
- सीने में दर्द: यदि आप छाती के केंद्र में दर्द का अनुभव करते हैं, खासकर अगर यह व्यायाम के दौरान होता है।
- स्टीवन-जॉनसन सिंड्रोम: यदि आप एक दर्दनाक लाल या बैंगनी रंग के दाने का अनुभव करते हैं जो फैलता है और छाले और / या अन्य घाव जो श्लेष्म झिल्ली (जैसे मुंह और होंठ) में दिखाई देने लगते हैं, खासकर यदि आपको पहले प्रकाश में संवेदनशीलता थी, तो संक्रमण श्वसन प्रणाली (जैसे ब्रोंकाइटिस) और / या बुखार।
यदि जल्दी पकड़ा जाता है, तो ये दुष्प्रभाव आमतौर पर दवा बंद करने के 2-3 दिनों के भीतर ठीक हो जाते हैं। यदि लक्षण बने रहते हैं, तो तुरंत अपने डॉक्टर से संपर्क करें। आपका डॉक्टर आपको कम खुराक पर दवा लेना फिर से शुरू करने की सलाह दे सकता है।
ऊपर सूचीबद्ध लोगों के अलावा, अकेले ज़ेलोडा के उपयोग से रिपोर्ट किए गए अन्य बहुत ही सामान्य दुष्प्रभाव, जो 10 में से 1 से अधिक लोगों को प्रभावित कर सकते हैं, वे हैं:
- पेट में दर्द
- दाने, सूखी या खुजली वाली त्वचा
- थकान
- भूख न लगना (एनोरेक्सिया)।
ये दुष्प्रभाव गंभीर हो सकते हैं। इसलिए, जब भी आपको कोई साइड इफेक्ट दिखे तो तुरंत अपने डॉक्टर से संपर्क करें। आपका डॉक्टर आपको खुराक कम करने और / या अस्थायी रूप से ज़ेलोडा उपचार बंद करने के लिए कहेगा। यह साइड इफेक्ट के बने रहने या इसे गंभीर साइड इफेक्ट में बदलने की संभावना को कम करने में मदद करेगा।
अन्य दुष्प्रभाव हैं:
आम दुष्प्रभाव (10 लोगों में से 1 को प्रभावित कर सकते हैं) में शामिल हैं:
- रक्त में सफेद या लाल रक्त कोशिकाओं की संख्या में कमी (परीक्षणों में देखा गया),
- निर्जलीकरण, वजन घटाने,
- नींद की कमी (अनिद्रा), अवसाद,
- सिरदर्द, तंद्रा, चक्कर आना, असामान्य त्वचा सनसनी (सुन्न या झुनझुनी), स्वाद में परिवर्तन,
- आंखों में जलन, फटने में वृद्धि, लाल आंख (नेत्रश्लेष्मलाशोथ),
- नसों की सूजन (थ्रोम्बोफ्लिबिटिस),
- सांस की तकलीफ, नकसीर, खांसी, बहती नाक,
- कोल्ड सोर या अन्य दाद संक्रमण,
- फेफड़ों या श्वसन प्रणाली के संक्रमण (जैसे निमोनिया या ब्रोंकाइटिस),
- मल त्याग, कब्ज, ऊपरी पेट में दर्द, अपच, अतिरिक्त हवा, शुष्क मुँह,
- त्वचा पर लाल चकत्ते, बालों का झड़ना (खालित्य), त्वचा का लाल होना, शुष्क त्वचा, खुजली, त्वचा का मलिनकिरण, त्वचा का झड़ना, त्वचा में सूजन, नाखून में बदलाव,
- जोड़ों या अंगों (अंगों), छाती या पीठ में दर्द,
- बुखार, अंगों की सूजन, अस्वस्थ महसूस करना,
- जिगर समारोह के साथ समस्याएं (रक्त परीक्षण में देखा गया) और रक्त में बिलीरुबिन में वृद्धि (यकृत के माध्यम से उत्सर्जित)।
असामान्य दुष्प्रभाव (100 लोगों में 1 से कम को प्रभावित कर सकते हैं) में शामिल हैं:
- रक्त संक्रमण, मूत्र पथ संक्रमण, त्वचा संक्रमण, नाक और गले में संक्रमण, फंगल संक्रमण (मुंह सहित), फ्लू, आंत्रशोथ, फोड़ा,
- त्वचा के नीचे नरम सूजन (लिपोमा),
- प्लेटलेट्स सहित रक्त कोशिकाओं में कमी, रक्त का पतला होना (परीक्षणों में देखा गया),
- एलर्जी,
- मधुमेह, रक्त में पोटेशियम की कमी, कुपोषण, रक्त ट्राइग्लिसराइड्स में वृद्धि,
- भ्रम की स्थिति, घबराहट के दौरे, उदास मनोदशा, कामेच्छा में कमी,
- बोलने में कठिनाई, स्मृति हानि, गति समन्वय की हानि, संतुलन में गड़बड़ी, बेहोशी, तंत्रिका क्षति (न्यूरोपैथी) और इंद्रियों की समस्याएं,
- धुंधली या दोहरी दृष्टि,
- चक्कर आना, कान दर्द,
- अनियमित दिल की धड़कन और धड़कन (अतालता), सीने में दर्द और दिल का दौरा (दिल का दौरा),
- गहरी नसों में रक्त के थक्के, उच्च या निम्न रक्तचाप, निस्तब्धता, अंगों (अंगों) में ठंड लगना, त्वचा पर बैंगनी धब्बे,
- फेफड़े की नसों में रक्त के थक्के (फुफ्फुसीय अन्त: शल्यता), फेफड़े का गिरना, खाँसी के साथ खून की कमी, दमा, परिश्रम के साथ सांस की तकलीफ,
- आंत्र रुकावट, पेट में तरल पदार्थ का संग्रह, छोटी या बड़ी आंत की सूजन, पेट या अन्नप्रणाली, पेट के निचले हिस्से में दर्द, पेट की परेशानी, नाराज़गी (पेट से भोजन का बहना), मल में रक्त,
- पीलिया (त्वचा और आंखों का पीला पड़ना),
- त्वचा के छाले और छाले, धूप में त्वचा की प्रतिक्रिया, हथेलियों का लाल होना, चेहरे की सूजन या दर्द,
- जोड़ों में सूजन या जकड़न, हड्डी में दर्द, मांसपेशियों में कमजोरी या जकड़न,
- गुर्दे में द्रव संग्रह, रात में मूत्र आवृत्ति में वृद्धि, असंयम, मूत्र में रक्त, रक्त क्रिएटिनिन में वृद्धि (गुर्दे की शिथिलता का संकेत),
- योनि से असामान्य रक्तस्राव,
- सूजन (एडिमा), ठंड लगना और जकड़न।
इनमें से कुछ दुष्प्रभाव आम हैं जब कैंसर के इलाज के लिए अन्य दवाओं के साथ केपेसिटाबाइन का उपयोग किया जाता है। इस संदर्भ में देखे गए अन्य दुष्प्रभाव हैं:
आम दुष्प्रभाव (10 लोगों में से 1 को प्रभावित कर सकते हैं) में शामिल हैं:
- रक्त में सोडियम, मैग्नीशियम और कैल्शियम की कमी, रक्त शर्करा में वृद्धि,
- तंत्रिका दर्द,
- कानों में बजना (टिनिटस), सुनवाई हानि,
- नसों की सूजन,
- हिचकी, बदली हुई आवाज,
- दर्द या परिवर्तित / मुंह में असामान्य सनसनी, जबड़े में दर्द,
- पसीना आना, रात को पसीना आना,
- मांसपेशी में ऐंठन,
- पेशाब करने में कठिनाई, पेशाब में रक्त या प्रोटीन,
- चोट लगने या इंजेक्शन साइट प्रतिक्रियाएं (एक ही समय में इंजेक्शन द्वारा दी गई दवाओं के कारण)।
दुर्लभ दुष्प्रभाव (1,000 लोगों में 1 को प्रभावित कर सकते हैं) में शामिल हैं:
- आंसू वाहिनी का संकुचन या रुकावट (आंसू वाहिनी स्टेनोसिस),
- लीवर फेलियर,
- सूजन के कारण पित्त स्राव में शिथिलता या रुकावट (कोलेस्टेटिक हेपेटाइटिस),
- इलेक्ट्रोकार्डियोग्राम में विशिष्ट परिवर्तन (क्यूटी लम्बा होना),
- कुछ प्रकार के अतालता (वेंट्रिकुलर फाइब्रिलेशन, टॉरडेस डी पॉइंट्स और ब्रैडीकार्डिया सहित),
- आंखों की सूजन दर्द और संभावित दृष्टि समस्याओं का कारण बनती है,
- प्रतिरक्षा प्रणाली की बीमारी के कारण त्वचा की सूजन लाल धब्बे और छीलने के लिए अग्रणी।
बहुत दुर्लभ दुष्प्रभाव (10,000 लोगों में से 1 को प्रभावित कर सकते हैं) में शामिल हैं:
- गंभीर त्वचा प्रतिक्रियाएं, जैसे कि दाने, छाले और छाले, जिसमें मुंह, नाक, जननांगों, हाथों, पैरों और आंखों (लाल और सूजी हुई आंखें) के अल्सर शामिल हो सकते हैं।
साइड इफेक्ट की रिपोर्टिंग
यदि आपको कोई साइड इफेक्ट मिलता है, तो अपने डॉक्टर, फार्मासिस्ट या नर्स से बात करें। इसमें कोई भी संभावित दुष्प्रभाव शामिल हैं जो इस पत्रक में सूचीबद्ध नहीं हैं। आप परिशिष्ट V में सूचीबद्ध राष्ट्रीय रिपोर्टिंग सिस्टम के माध्यम से सीधे साइड इफेक्ट की रिपोर्ट कर सकते हैं। साइड इफेक्ट्स जो आप मदद कर सकते हैं इस दवा की सुरक्षा के बारे में अधिक जानकारी प्रदान करें।
समाप्ति और अवधारण
बच्चों की दृष्टि और पहुंच से दूर रखें।
30 डिग्री सेल्सियस से ऊपर के तापमान पर स्टोर न करें।
इस दवा का प्रयोग बाहरी कार्टन पर और "EXP" के बाद लेबल पर बताई गई समाप्ति तिथि के बाद न करें। समाप्ति तिथि महीने के अंतिम दिन को संदर्भित करती है।
अपशिष्ट जल या घरेलू कचरे के माध्यम से दवाओं का निपटान नहीं किया जाना चाहिए। अपने फार्मासिस्ट से उन दवाओं का निपटान करने का तरीका पूछें जिनका आप अब उपयोग नहीं करते हैं। इससे पर्यावरण की रक्षा करने में मदद मिलेगी।
संरचना और फार्मास्युटिकल फॉर्म
ज़ेलोडा में क्या शामिल है
सक्रिय पदार्थ कैपेसिटाबाइन (प्रत्येक फिल्म-लेपित टैबलेट के लिए 500 मिलीग्राम) है।
अन्य सहायक पदार्थ हैं:
- टैबलेट कोर: निर्जल लैक्टोज, croscarmellose सोडियम, हाइपोर्मेलोज, माइक्रोक्रिस्टलाइन सेलुलोज, मैग्नीशियम स्टीयरेट।
- टैबलेट कोटिंग: हाइपोमेलोज, टाइटेनियम डाइऑक्साइड (E171), पीला और लाल आयरन ऑक्साइड (E172), तालक।
ज़ेलोडा कैसा दिखता है और पैक की सामग्री
आड़ू रंग का, उभयलिंगी, आयताकार आकार का फिल्म-लेपित टैबलेट, एक तरफ "500" और दूसरी तरफ "ज़ेलोडा" के साथ डिबॉस किया गया।
ज़ेलोडा 500 मिलीग्राम फिल्म-लेपित गोलियों के पैक में 120 फिल्म-लेपित गोलियां (10 गोलियों के 12 छाले) हैं।
स्रोत पैकेज पत्रक: एआईएफए (इतालवी मेडिसिन एजेंसी)। सामग्री जनवरी 2016 में प्रकाशित हुई। हो सकता है कि मौजूद जानकारी अप-टू-डेट न हो।
सबसे अप-टू-डेट संस्करण तक पहुंचने के लिए, एआईएफए (इतालवी मेडिसिन एजेंसी) वेबसाइट तक पहुंचने की सलाह दी जाती है। अस्वीकरण और उपयोगी जानकारी।
01.0 औषधीय उत्पाद का नाम
फिल्म के साथ लेपित ज़ेलोडा ५०० एमजी टैबलेट
02.0 गुणात्मक और मात्रात्मक संरचना
प्रत्येक फिल्म-लेपित टैबलेट में 500 मिलीग्राम कैपेसिटाबाइन होता है।
ज्ञात प्रभावों के साथ सहायक पदार्थ:
प्रत्येक फिल्म-लेपित टैबलेट में 52 मिलीग्राम निर्जल लैक्टोज होता है।
Excipients की पूरी सूची के लिए, खंड ६.१ देखें।
03.0 फार्मास्युटिकल फॉर्म
फिल्म-लेपित गोली
ज़ेलोडा 500 मिलीग्राम आड़ू के रंग की, उभयलिंगी आयताकार आकार की फिल्म-लेपित गोलियां हैं, जो एक तरफ "500" और दूसरी तरफ "ज़ेलोडा" से उभरी हुई हैं।
04.0 नैदानिक सूचना
04.1 चिकित्सीय संकेत
Xeloda को चरण III (ड्यूक्स सी) कोलन कैंसर (खंड 5.1 देखें) के लिए सर्जरी के दौर से गुजर रहे रोगियों में सहायक चिकित्सा के लिए संकेत दिया गया है।
ज़ेलोडा को मेटास्टेटिक कोलोरेक्टल कैंसर (खंड 5.1 देखें) के उपचार के लिए संकेत दिया गया है।
ज़ेलोडा को प्लैटिनम-आधारित आहार के संयोजन में उन्नत गैस्ट्रिक कैंसर के प्रथम-पंक्ति उपचार के लिए संकेत दिया गया है (खंड 5.1 देखें)।
डोकैटेक्सेल के साथ संयोजन में ज़ेलोडा (खंड 5.1 देखें) साइटोटोक्सिक कीमोथेरेपी की विफलता के बाद स्थानीय रूप से उन्नत या मेटास्टेटिक स्तन कैंसर के रोगियों के उपचार के लिए संकेत दिया गया है। पिछली चिकित्सा में "एंथ्रासाइक्लिन" शामिल होना चाहिए। इसके अलावा, ज़ेलोडा को स्थानीय रूप से उन्नत या मेटास्टेटिक स्तन कैंसर के रोगियों के इलाज के लिए मोनोथेरेपी के रूप में इंगित किया जाता है, जो कि एक टैक्सेन की विफलता के बाद और कीमोथेरेपी आहार युक्त एन्थ्रासाइक्लिन या जिनके लिए एन्थ्रासाइक्लिन का संकेत नहीं है। " आगे एंथ्रासाइक्लिन थेरेपी।
०४.२ खुराक और प्रशासन की विधि
ज़ेलोडा केवल एक डॉक्टर द्वारा निर्धारित किया जाना चाहिए जो एंटीनोप्लास्टिक दवाओं के उपयोग में माहिर हैं। उपचार के पहले कोर्स के दौरान सभी रोगियों के लिए करीबी निगरानी की सिफारिश की जाती है।
गंभीर विषाक्तता या रोग की प्रगति होने पर उपचार बंद कर दिया जाना चाहिए।1250 मिलीग्राम / एम 2 और 1000 मिलीग्राम / एम 2 की ज़ेलोडा खुराक शुरू करने के लिए शरीर की सतह क्षेत्र के आधार पर मानक और कम खुराक की गणना क्रमशः टेबल्स 1 और 2 में विस्तृत है।
मात्रा बनाने की विधि
अनुशंसित खुराक (खंड 5.1 देखें):
मोनोथेरापी
कोलन, कोलोरेक्टल और स्तन कैंसर
मोनोथेरेपी उपचार में, कोलन, मेटास्टैटिक कोलोरेक्टल, या स्थानीय रूप से उन्नत या मेटास्टैटिक स्तन कैंसर के सहायक उपचार में कैपेसिटाबाइन की अनुशंसित प्रारंभिक खुराक 1250 मिलीग्राम / एम 2 है, जिसे दो बार दैनिक (सुबह और शाम; 2500 मिलीग्राम / एम 2 की कुल खुराक) के लिए प्रशासित किया जाता है। 14 दिन, उसके बाद 7 दिन की आराम अवधि। चरण III कोलन कैंसर वाले रोगियों में कुल 6 महीने के लिए सहायक चिकित्सा की सिफारिश की जाती है।
एसोसिएशन थेरेपी
कोलन, कोलोरेक्टल और गैस्ट्रिक कैंसर
संयोजन उपचार में, कैपेसिटाबाइन की अनुशंसित प्रारंभिक खुराक को घटाकर 800 - 1000 मिलीग्राम / एम 2 किया जाना चाहिए जब 14 दिनों के लिए प्रतिदिन दो बार प्रशासित किया जाता है, इसके बाद 7 दिन की आराम अवधि या 625 मिलीग्राम / एम 2 प्रतिदिन दो बार। लगातार प्रशासित होने पर (अनुभाग देखें) 5.1)। इरिनोटेकन के साथ संयोजन में, अनुशंसित प्रारंभिक खुराक 800 मिलीग्राम / एम 2 है जब 14 दिनों के लिए प्रतिदिन दो बार प्रशासित किया जाता है, इसके बाद दिन में इरिनोटेकन 200 मिलीग्राम / एम 2 के संयोजन में 7-दिन की आराम अवधि होती है। संयोजन आहार में बेवाकिज़ुमैब की शुरूआत कैपेसिटाबाइन की शुरुआती खुराक पर कोई प्रभाव नहीं पड़ता है। सिस्प्लैटिन के उत्पाद विशेषताओं के सारांश के अनुसार, कैपेसिटाबाइन प्लस सिस्प्लैटिन के संयोजन के साथ इलाज किए गए रोगियों में, सिस्प्लैटिन प्रशासन से पहले पर्याप्त जलयोजन और एंटीमैटिक उपचार बनाए रखने के लिए पूर्व-दवा शुरू की जानी चाहिए। एंटीमैटिक्स के साथ पूर्व-दवा ऑक्सिप्लिप्टिन के उत्पाद विशेषताओं के सारांश के अनुसार संयोजन कैपेसिटाबाइन प्लस ऑक्सिप्लिप्टिन के साथ इलाज किए गए मरीजों में अनुशंसा की जाती है। चरण III कोलन कैंसर वाले रोगियों में सहायक उपचार की 6 महीने की अवधि की सिफारिश की जाती है।
स्तन कैंसर
डोकैटेक्सेल के साथ संयोजन में, मेटास्टेटिक स्तन कैंसर के उपचार में कैपेसिटाबाइन की अनुशंसित प्रारंभिक खुराक 14 दिनों के लिए प्रतिदिन दो बार 1250 मिलीग्राम / एम 2 है, इसके बाद 7-दिन की आराम अवधि, डोकेटेक्सेल 75 मिलीग्राम / एम 2 के साथ 1 घंटे में अंतःशिरा में संयोजन में हर 3 सप्ताह में जलसेक। संयोजन कैपेसिटाबाइन और डोकैटेक्सेल प्राप्त करने वाले रोगियों में, मौखिक कॉर्टिकोस्टेरॉइड के साथ पूर्व-दवा, जैसे डेक्सामेथासोन, को डॉकेटेक्सेल प्रशासन से पहले उत्पाद विशेषताओं के डॉकेटेक्सेल सारांश के अनुसार शुरू किया जाना चाहिए।
ज़ेलोडा की खुराक की गणना
तालिका 1 शरीर की सतह क्षेत्र के आधार पर कैपेसिटाबाइन की मानक और कम खुराक की गणना, 1250 मिलीग्राम / एम 2 की प्रारंभिक खुराक
तालिका 2 शरीर की सतह क्षेत्र के आधार पर कैपेसिटाबाइन की मानक और कम खुराक की गणना, 1000 मिलीग्राम / एम 2 . की प्रारंभिक खुराक
उपचार के दौरान खुराक समायोजन:
आम
कैपेसिटाबाइन प्रशासन के कारण होने वाली विषाक्तता को रोगसूचक उपचार और / या खुराक संशोधन (उपचार में रुकावट या खुराक में कमी) के साथ प्रबंधित किया जा सकता है। एक बार खुराक कम हो जाने के बाद, इसे उसके बाद नहीं बढ़ाया जाना चाहिए। विषाक्तता के मामले में, जो इलाज करने वाले चिकित्सक की राय में गंभीर या घातक होने की संभावना नहीं है, जैसे कि खालित्य, परिवर्तित स्वाद, नाखून परिवर्तन, उसी खुराक पर उपचार बिना किसी कमी या रुकावट के जारी रखा जा सकता है। मध्यम या गंभीर विषाक्तता होने पर कैपेसिटाबाइन लेने वाले मरीजों को तुरंत उपचार बंद करने की आवश्यकता के बारे में सलाह दी जानी चाहिए। विषाक्तता के कारण बाहर रखी गई कैपेसिटाबाइन की खुराक को प्रतिस्थापित नहीं किया जा सकता है। विषाक्तता के मामले में निम्नलिखित अनुशंसित खुराक संशोधन हैं:
तालिका 3 कैपेसिटाबाइन खुराक में कमी अनुसूची (3 सप्ताह का चक्र या निरंतर उपचार)
* नेशनल कैंसर इंस्टीट्यूट ऑफ कनाडा क्लिनिकल ट्रायल ग्रुप (एनसीआईसी सीजीटी) के कॉमन टॉक्सिसिटी क्राइटेरिया (संस्करण 1) के अनुसार या कैंसर थेरेपी इवैल्यूएशन प्रोग्राम के कॉमन टर्मिनोलॉजी क्राइटेरिया फॉर एडवर्स इवेंट्स (सीटीसीएई), यूएस नेशनल कैंसर इंस्टीट्यूट, वर्जन 4.0 . हाथ-पैर सिंड्रोम और हाइपरबिलीरुबिनेमिया के लिए, खंड 4.4 देखें।
रुधिर
बेसलाइन न्यूट्रोफिल काउंट वाले मरीज
विषाक्तता के लिए खुराक में संशोधन जब कैपेसिटाबाइन का उपयोग अन्य औषधीय उत्पादों के साथ संयोजन में 3 सप्ताह के चक्र के रूप में किया जाता है
जब अन्य औषधीय उत्पादों के साथ संयोजन में 3 सप्ताह के चक्रों में कैपेसिटाबाइन का उपयोग किया जाता है, तो विषाक्तता के लिए खुराक संशोधनों को कैपेसिटाबाइन के लिए उपरोक्त तालिका 3 के अनुसार और अन्य औषधीय उत्पादों के लिए उत्पाद विशेषताओं के प्रासंगिक सारांश के अनुसार किया जाना चाहिए। .
उपचार चक्र की शुरुआत में, यदि कैपेसिटाबाइन या अन्य औषधीय उत्पाद (ओं) के लिए उपचार के स्थगन का संकेत दिया जाता है, तो सभी दवाओं के प्रशासन को फिर से शुरू करने की आवश्यकताओं तक सभी औषधीय उत्पादों के प्रशासन को स्थगित कर दिया जाना चाहिए।
उपचार के दौरान, उपचार करने वाले चिकित्सक द्वारा माना जाने वाला उन विषाक्त पदार्थों के लिए केपेसिटाबाइन से संबंधित नहीं होने के लिए, कैपेसिटाबाइन के साथ उपचार जारी रखा जाना चाहिए और अन्य औषधीय उत्पाद की खुराक को प्रासंगिक निर्धारित जानकारी के अनुसार समायोजित किया जाना चाहिए।
यदि अन्य औषधीय उत्पादों को स्थायी रूप से बंद किया जाना है, तो कैपेसिटाबाइन के साथ उपचार फिर से शुरू किया जा सकता है जब कैपेसिटाबाइन के पुन: परिचय की आवश्यकताएं पूरी हो जाती हैं।
यह दृष्टिकोण सभी संकेतों और सभी विशेष रोगी आबादी पर लागू होता है।
विषाक्तता के लिए खुराक में संशोधन जब कैपेसिटाबाइन का उपयोग अन्य औषधीय उत्पादों के साथ संयोजन में निरंतर उपचार के रूप में किया जाता है
विषाक्तता के लिए खुराक संशोधन जब अन्य औषधीय उत्पादों के साथ संयोजन में निरंतर उपचार के रूप में कैपेसिटाबाइन का उपयोग किया जाता है, तो कैपेसिटाबाइन के लिए उपरोक्त तालिका 3 के अनुसार और अन्य औषधीय उत्पाद के लिए उत्पाद विशेषताओं के प्रासंगिक सारांश के अनुसार किया जाना चाहिए।
विशेष रूप से रोगी आबादी में खुराक समायोजन:
बिगड़ा हुआ जिगर समारोह
बिगड़ा हुआ यकृत समारोह वाले रोगियों के लिए खुराक समायोजन पर मार्गदर्शन प्रदान करने के लिए अपर्याप्त सुरक्षा और प्रभावकारिता डेटा हैं। सिरोसिस या हेपेटाइटिस के कारण जिगर की विफलता पर कोई डेटा नहीं है।
बिगड़ा हुआ गुर्दे समारोह
कैपेसिटाबाइन को गंभीर गुर्दे की कमी (बेसलाइन पर 30 मिली / मिनट [कॉकक्रॉफ्ट और गॉल्ट] से कम क्रिएटिनिन क्लीयरेंस) वाले रोगियों में contraindicated है। मध्यम गुर्दे की हानि (बेसलाइन पर क्रिएटिनिन क्लीयरेंस 30-50 एमएल / मिनट) वाले रोगियों में ग्रेड 3 या 4 प्रतिकूल प्रतिक्रिया की घटना कुल आबादी की तुलना में अधिक है। 1250 मिलीग्राम / एम 2 की प्रारंभिक खुराक के लिए 75% की कमी की सिफारिश की जाती है बेसलाइन पर मध्यम गुर्दे की हानि वाले मरीजों में बेसलाइन पर मध्यम गुर्दे की हानि वाले मरीजों में 1000 मिलीग्राम / एम 2 की शुरुआती खुराक के लिए खुराक में कमी की आवश्यकता नहीं है। हल्के गुर्दे की हानि वाले मरीजों में प्रारंभिक खुराक (क्रिएटिनिन क्लीयरेंस 51-80 मिलीलीटर / मिनट पर आधार रेखा)।यदि रोगी उपचार के दौरान ग्रेड 2, 3 या 4 प्रतिकूल घटना विकसित करता है, तो सावधानीपूर्वक निगरानी और उपचार को तत्काल बंद करने की सलाह दी जाती है, और अगली खुराक को ऊपर तालिका 3 में संकेत के अनुसार समायोजित किया जाना चाहिए। गणना की गई क्रिएटिनिन 30 मिली / मिनट से नीचे आती है, ज़ेलोडा बंद कर दिया जाना चाहिए। गुर्दे की हानि की स्थिति में खुराक समायोजन पर ये सिफारिशें मोनोथेरेपी और संयोजन उपयोग दोनों पर लागू होती हैं (निम्नलिखित में "बुजुर्ग" अनुभाग भी देखें)।
वरिष्ठ नागरिकों
अकेले कैपेसिटाबाइन का उपयोग करते समय कोई प्रारंभिक खुराक समायोजन की आवश्यकता नहीं होती है। हालांकि, छोटे विषयों की तुलना में 60 वर्ष की आयु के रोगियों ने अक्सर ग्रेड 3 या 4 उपचार से संबंधित प्रतिकूल प्रतिक्रियाओं की सूचना दी।
जब अन्य एजेंटों के साथ संयोजन में कैपेसिटाबाइन का उपयोग किया गया था, तो बुजुर्ग रोगियों (≥ 65 वर्ष) ने युवा रोगियों की तुलना में अधिक ग्रेड 3 और 4 प्रतिकूल दवा प्रतिक्रियाओं का अनुभव किया, जिनमें उपचार बंद करने वाले लोग शामिल थे। रोगियों की करीबी निगरानी ≥ 60 वर्ष की आयु की सलाह दी जाती है।
- डोकैटेक्सेल के साथ संयोजन में: ग्रेड 3 या 4 उपचार से संबंधित प्रतिकूल प्रतिक्रियाओं और उपचार से संबंधित गंभीर प्रतिकूल प्रतिक्रियाओं की एक बढ़ी हुई घटना 60 वर्ष और उससे अधिक उम्र के रोगियों में देखी गई (देखें खंड 5.1)। कैपेसिटाबाइन की एक प्रारंभिक खुराक की सिफारिश की जाती है। 75% तक कम (950) मिलीग्राम / एम २ दो बार दैनिक) ६० वर्ष और उससे अधिक आयु के रोगियों में। यदि रोगियों में कोई विषाक्तता नहीं होती है ≥ ६० वर्ष की आयु में डोकेटेक्सेल के साथ संयोजन में कैपेसिटाबाइन की कम प्रारंभिक खुराक के साथ इलाज किया जाता है, तो कैपेसिटाबाइन की खुराक को सावधानी से १२५० मिलीग्राम / तक बढ़ाया जा सकता है। एम 2 दिन में दो बार।
बाल चिकित्सा जनसंख्या
कोलन, कोलोरेक्टल, गैस्ट्रिक और स्तन कैंसर के संकेतों में बाल चिकित्सा आबादी में कैपेसिटाबाइन का कोई प्रासंगिक उपयोग नहीं है।
प्रशासन का तरीका
भोजन समाप्त होने के 30 मिनट के भीतर ज़ेलोडा की गोलियों को पानी के साथ निगल लेना चाहिए।
04.3 मतभेद
• फ्लोरोपाइरीमिडीन थेरेपी के प्रति गंभीर या अप्रत्याशित प्रतिक्रियाओं का इतिहास।
• कैपेसिटाबाइन या धारा ६.१ में सूचीबद्ध किसी भी घटक या फ्लूरोरासिल के प्रति अतिसंवेदनशीलता।
• डायहाइड्रोपाइरीमिडीन डिहाइड्रोजनेज (डीपीडी) गतिविधि की ज्ञात पूर्ण अनुपस्थिति वाले रोगियों में (खंड 4.4 देखें)।
गर्भावस्था और स्तनपान के दौरान।
• ल्यूकोपेनिया, न्यूट्रोपेनिया या थ्रोम्बोसाइटोपेनिया के गंभीर रूपों वाले रोगियों में।
• गंभीर यकृत हानि वाले रोगियों में।
• गंभीर गुर्दे की हानि (30 मिली / मिनट से कम क्रिएटिनिन क्लीयरेंस) वाले रोगियों में।
• सॉरीवुडिन या इसके रासायनिक रूप से संबंधित एनालॉग्स जैसे ब्रिवुडिन के साथ उपचार के दौरान (खंड 4.5 देखें)।
• यदि संयोजन आहार में किसी भी दवा के लिए मतभेद हैं, तो उस दवा का उपयोग नहीं किया जाना चाहिए।
04.4 उपयोग के लिए विशेष चेतावनी और उचित सावधानियां
NS खुराक सीमित विषाक्तता दस्त, पेट में दर्द, मतली, स्टामाटाइटिस और हाथ-पैर सिंड्रोम (हाथ-पैर की त्वचा की प्रतिक्रिया, पामर-प्लांटर एरिथ्रोडायस्थेसिया) शामिल हैं। अधिकांश प्रतिकूल प्रतिक्रियाएं प्रतिवर्ती होती हैं और चिकित्सा के स्थायी विच्छेदन की आवश्यकता नहीं होती है, हालांकि खुराक में रुकावट या कमी आवश्यक हो सकती है।
दस्त। गंभीर दस्त वाले मरीजों पर कड़ी निगरानी रखी जानी चाहिए और निर्जलीकरण की स्थिति में तरल पदार्थ और इलेक्ट्रोलाइट्स दिए जाने चाहिए। मानक रोधी उपचार (जैसे लोपरामाइड) दिए जा सकते हैं। एनसीआईसी के सामान्य विषाक्तता मानदंड के अनुसार ग्रेड 2 डायरिया का अर्थ है प्रति दिन 4 से 6 डिस्चार्ज या रात में डिस्चार्ज, ग्रेड 3 डायरिया के लिए प्रति दिन 7 से 9 डिस्चार्ज की वृद्धि या असंयम और कुअवशोषण, और डायरिया के लिए ग्रेड 4 ए प्रति दिन 10 डिस्चार्ज की वृद्धि या अत्यधिक रक्तस्रावी दस्त या पैरेंट्रल सपोर्ट की आवश्यकता। यदि आवश्यक हो, तो खुराक में कमी की जानी चाहिए (खंड 4.2 देखें)।
निर्जलीकरण। ऐसा होने पर निर्जलीकरण को रोका या ठीक किया जाना चाहिए। एनोरेक्सिया, अस्टेनिया, मितली, उल्टी या दस्त के रोगी तेजी से निर्जलित हो सकते हैं। निर्जलीकरण तीव्र गुर्दे की विफलता का कारण बन सकता है, विशेष रूप से पहले से मौजूद गुर्दे की हानि वाले रोगियों में या जब ज्ञात नेफ्रोटॉक्सिक दवाओं के संयोजन में केपेसिटाबाइन दिया जाता है। निर्जलीकरण के लिए माध्यमिक तीव्र गुर्दे की विफलता संभावित रूप से घातक हो सकती है। यदि ग्रेड 2 (या उच्चतर) निर्जलीकरण होता है, तो कैपेसिटाबाइन उपचार तुरंत रोक दिया जाना चाहिए और निर्जलीकरण को ठीक किया जाना चाहिए। उपचार तब तक फिर से शुरू नहीं किया जाना चाहिए जब तक कि रोगी को पुनर्जलीकरण नहीं किया जाता है और किसी भी प्रारंभिक कारण को ठीक या नियंत्रित नहीं किया जाता है। आवश्यक प्रतिकूल घटना के लिए खुराक में संशोधन किया जाना चाहिए (खंड 4.2 देखें)।
हाथ-पैर सिंड्रोम (हाथ-पैर की त्वचा की प्रतिक्रिया या पामर-प्लांटर एरिथ्रोडिसैस्थेसिया या चरम सीमाओं के कीमोथेरेपी-प्रेरित एरिथेमा के रूप में भी जाना जाता है)। ग्रेड 1 हैंड-फुट सिंड्रोम को सुन्नता, डिस्थेसिया / पैरास्थेसिया, झुनझुनी, दर्द रहित एडिमा या हाथों और / या पैरों की एरिथेमा, और / या बेचैनी के रूप में परिभाषित किया गया है जो रोगी को सामान्य रूप से काम करने से नहीं रोकता है।
ग्रेड 2 हैंड-फुट सिंड्रोम को दर्दनाक एरिथेमा और हाथों और / या पैरों में एडिमा और / या बेचैनी के रूप में परिभाषित किया गया है जो रोगी की दैनिक गतिविधियों को प्रभावित करता है।
ग्रेड 3 हैंड-फुट सिंड्रोम को गीले स्केलिंग, अल्सरेशन, ब्लिस्टरिंग और हाथों और / या पैरों में गंभीर दर्द और / या गंभीर असुविधा के रूप में परिभाषित किया जाता है जिससे रोगी को काम करना या दैनिक गतिविधियों को करना असंभव हो जाता है। यदि ग्रेड 2 या 3 हाथ -फुट सिंड्रोम होता है, कैपेसिटाबाइन प्रशासन को तब तक रोकें जब तक कि लक्षण तीव्रता का समाधान न हो जाए या ग्रेड 1 तक कम न हो जाए। ग्रेड 3 हैंड-फुट सिंड्रोम की शुरुआत के बाद, कैपेसिटाबाइन की बाद की खुराक को कम किया जाना चाहिए। जब कैपेसिटाबाइन और सिस्प्लैटिन का संयोजन में उपयोग किया जाता है, तो हाथ-पैर सिंड्रोम के रोगसूचक या माध्यमिक प्रोफिलैक्सिस उपचार के लिए विटामिन बी 6 (पाइरिडोक्सिन) के उपयोग की सिफारिश नहीं की जाती है, क्योंकि प्रकाशित मामलों से पता चला है कि यह सिस्प्लैटिन की प्रभावकारिता को कम कर सकता है। कुछ प्रमाण हैं कि डेक्सपैंथेनॉल ज़ेलोडा के साथ इलाज किए गए रोगियों में हाथ-पैर सिंड्रोम के प्रोफिलैक्सिस के लिए प्रभावी है।
कार्डियोटॉक्सिसिटी। फ्लोरोपाइरीमिडीन थेरेपी कार्डियोटॉक्सिसिटी से जुड़ी हुई है, जिसमें मायोकार्डियल इंफार्क्शन, एनजाइना, अतालता, कार्डियोजेनिक शॉक, अचानक मौत और इलेक्ट्रोकार्डियोग्राफिक परिवर्तन (क्यूटी अंतराल के लंबे होने के बहुत दुर्लभ मामलों सहित) शामिल हैं। ये प्रतिकूल प्रतिक्रियाएं कोरोनरी धमनी के पिछले इतिहास वाले रोगियों में अधिक सामान्य रूप से हो सकती हैं। रोग। कार्डिएक अतालता (वेंट्रिकुलर फाइब्रिलेशन, टॉरडेस डी पॉइंट्स और ब्रैडीकार्डिया सहित), एनजाइना पेक्टोरिस, मायोकार्डियल रोधगलन, हृदय की विफलता और कार्डियोमायोपैथी केपेसिटाबाइन लेने वाले रोगियों में रिपोर्ट की गई है। महत्वपूर्ण एनजाइना पेक्टोरिस विशेष सावधानी बरती जानी चाहिए (धारा 4.8 देखें)।
हाइपो- या हाइपरलकसीमिया। कैपेसिटाबाइन के साथ उपचार के दौरान हाइपो- या हाइपरलकसीमिया के मामले सामने आए हैं। हाइपो- या हाइपरलकसीमिया के पहले से मौजूद इतिहास वाले रोगियों में विशेष सावधानी बरती जानी चाहिए (देखें खंड 4.8 )।
केंद्रीय या परिधीय तंत्रिका तंत्र के रोग। केंद्रीय या परिधीय तंत्रिका तंत्र की बीमारियों वाले मरीजों, जैसे मस्तिष्क मेटास्टेस या न्यूरोपैथी, को सावधानी के साथ देखा जाना चाहिए (धारा 4.8 देखें)।
मधुमेह मेलेटस या इलेक्ट्रोलाइट गड़बड़ी। मधुमेह मेलिटस या इलेक्ट्रोलाइट गड़बड़ी वाले मरीजों को कैपेसिटाबाइन के साथ उपचार के दौरान बढ़ने की संभावना को देखते हुए सावधानी के साथ विचार किया जाना चाहिए।
Coumarin-व्युत्पन्न थक्कारोधी। वारफेरिन की एकल खुराक के प्रशासन के साथ एक बातचीत अध्ययन में, एस-वारफारिन के औसत एयूसी (+ 57%) में उल्लेखनीय वृद्धि हुई थी। ये डेटा कैपेसिटाबाइन द्वारा साइटोक्रोम P450 आइसोनिजाइम 2C9 के निषेध के कारण "संभावित रूप से" बातचीत का सुझाव देते हैं। कैपेसिटाबाइन के साथ Coumarin-व्युत्पन्न मौखिक थक्कारोधी लेने वाले मरीजों को रक्तचाप मापदंडों में किसी भी असामान्यता के लिए नियमित रूप से निगरानी की जानी चाहिए। जमावट (INR या प्रोथ्रोम्बिन समय) ) और एंटीकोआगुलंट्स की खुराक को तदनुसार समायोजित किया जाना चाहिए (खंड 4.5 देखें)।
बिगड़ा हुआ जिगर समारोह। बिगड़ा हुआ यकृत समारोह वाले रोगियों में सुरक्षा और प्रभावकारिता पर डेटा की अनुपस्थिति में, यकृत मेटास्टेस की उपस्थिति या अनुपस्थिति की परवाह किए बिना, हल्के से मध्यम यकृत रोग वाले रोगियों में कैपेसिटाबाइन के उपयोग की बारीकी से निगरानी की जानी चाहिए।कैपेसिटाबाइन प्रशासन को बंद कर दिया जाना चाहिए यदि बिलीरुबिन में उपचार से संबंधित ऊंचाई 3.0 x ULN से अधिक हो या हेपेटिक एमिनोट्रांस्फरेज (ALT, AST) में उपचार से संबंधित ऊंचाई 2.5 x ULN से अधिक हो। कैपेसिटाबाइन मोनोथेरेपी उपचार फिर से शुरू किया जा सकता है जब बिलीरुबिन ≤3.0 x ULN तक कम हो जाता है या यकृत एमिनोट्रांस्फरेज़ ≤2.5 x ULN तक कम हो जाता है।
बिगड़ा हुआ गुर्दे समारोह। मध्यम गुर्दे की हानि (क्रिएटिनिन क्लीयरेंस 30-50 मिली / मिनट) वाले रोगियों में ग्रेड 3 या 4 प्रतिकूल प्रतिक्रिया की घटना समग्र आबादी की तुलना में अधिक है (खंड 4.2 और 4.3 देखें)।
डीहाइड्रोपाइरीमिडीन डिहाइड्रोजनेज (डीपीडी) की कमी: 5-एफयू से जुड़ी दुर्लभ, अप्रत्याशित और गंभीर विषाक्तता (जैसे, स्टामाटाइटिस, डायरिया, म्यूकोसाइटिस, न्यूट्रोपेनिया और न्यूरोटॉक्सिसिटी) डीपीडी गतिविधि में कमी से संबंधित है। डीपीडी की कम या कोई गतिविधि वाले रोगी, इसमें शामिल एक एंजाइम फ्लूरोरासिल के टूटने से, फ्लूरोरासिल के कारण गंभीर, जीवन-धमकी या घातक प्रतिकूल प्रतिक्रियाओं का खतरा बढ़ जाता है। हालांकि डीपीडी की कमी को ठीक से पहचाना नहीं जा सकता है, यह ज्ञात है कि कुछ उत्परिवर्तन वाले रोगी जीन लोकस के समयुग्मजी या मिश्रित हेटेरोज़ाइट्स होते हैं। डीपीवाईडी, जो डीपीडी एंजाइमेटिक गतिविधि की पूर्ण या लगभग पूर्ण अनुपस्थिति का कारण बनते हैं (जैसा कि प्रयोगशाला विश्लेषण द्वारा निर्धारित किया गया है), जीवन के लिए खतरा या घातक विषाक्तता का सबसे बड़ा जोखिम है और ज़ेलोडा के साथ इलाज नहीं किया जाना चाहिए (खंड 4.3 देखें)। डीपीडी गतिविधि की कुल अनुपस्थिति वाले रोगियों के लिए कोई भी खुराक सुरक्षित नहीं पाई गई।
आंशिक डीपीडी की कमी वाले रोगी (जैसे कि विषमयुग्मजी उत्परिवर्तन वाले) डीपीवाईडी) और जिसके लिए ज़ेलोडा के लाभ को इसके जोखिमों से अधिक माना जाता है (एक वैकल्पिक गैर-फ्लुओपाइरीमिडीन कीमोथेरेपी आहार की उपयुक्तता को ध्यान में रखते हुए) को अत्यधिक सावधानी के साथ इलाज किया जाना चाहिए और विषाक्तता के अनुसार खुराक समायोजन के साथ अक्सर निगरानी की जानी चाहिए। एक विशिष्ट परीक्षण द्वारा मापी गई आंशिक डीपीडी गतिविधि वाले रोगियों में एक विशिष्ट खुराक की सिफारिश करें।
अज्ञात डीपीडी की कमी वाले रोगियों में घातक विषाक्तता जैसे कि तीव्र ओवरडोज एपिसोड हो सकता है, जिन्हें कैपेसिटाबाइन के साथ इलाज किया जाता है (खंड 4.9 देखें)। तीव्र ग्रेड 2-4 विषाक्तता के मामले में, उपचार तुरंत रोक दिया जाना चाहिए। देखी गई विषाक्तता की शुरुआत, अवधि और गंभीरता के नैदानिक मूल्यांकन के आधार पर उपचार को स्थायी रूप से बंद करने पर विचार किया जाना चाहिए।
नेत्र संबंधी जटिलताएं: केराटाइटिस और कॉर्नियल विकारों जैसी नेत्र संबंधी जटिलताओं के लिए मरीजों की बारीकी से निगरानी की जानी चाहिए, खासकर यदि उनके पास नेत्र विकारों का पिछला इतिहास है। नेत्र विकारों का उपचार चिकित्सकीय रूप से उचित तरीके से शुरू किया जाना चाहिए।
गंभीर त्वचा प्रतिक्रियाएं: ज़ेलोडा स्टीवंस-जॉनसन सिंड्रोम और विषाक्त एपिडर्मल नेक्रोलिसिस जैसी गंभीर त्वचा प्रतिक्रियाओं को प्रेरित कर सकता है। उन रोगियों में जो एक गंभीर त्वचा प्रतिक्रिया का अनुभव करते हैं जो संभवतः ज़ेलोडा के उपचार से संबंधित हैं, इस दवा को स्थायी रूप से बंद कर दिया जाना चाहिए।
चूंकि इस दवा में एक सहायक के रूप में निर्जल लैक्टोज होता है, गैलेक्टोज असहिष्णुता के दुर्लभ वंशानुगत रूपों वाले रोगियों, लैप लैक्टेज एंजाइम की कमी और ग्लूकोज-गैलेक्टोज malabsorption को यह दवा नहीं लेनी चाहिए।
04.5 अन्य औषधीय उत्पादों और अन्य प्रकार की बातचीत के साथ बातचीत
इंटरेक्शन अध्ययन केवल वयस्कों में किया गया है।
अन्य दवाओं के साथ सहभागिता:
साइटोक्रोम P-450 2C9 सबस्ट्रेट्स: वारफारिन अध्ययनों के अलावा, कैपेसिटाबाइन और अन्य CYP2C9 सबस्ट्रेट्स के बीच कोई औपचारिक दवा-दवा बातचीत अध्ययन नहीं किया गया है। 2C9 सबस्ट्रेट्स (जैसे फ़िनाइटोइन) के साथ कैपेसिटाबाइन का प्रशासन करते समय सावधानी बरती जानी चाहिए। अन्य Coumarin-व्युत्पन्न थक्कारोधी और धारा 4.4 के साथ बातचीत भी देखें।
Coumarin-व्युत्पन्न थक्कारोधी: जमावट मापदंडों और / या रक्तस्राव में परिवर्तन की रिपोर्ट रोगियों में कैपेसिटाबाइन और कौमारिन-व्युत्पन्न एंटीकोआगुलंट्स, जैसे कि वारफारिन और फेनप्रोकोमोन के साथ सहवर्ती रूप से इलाज किए गए रोगियों में हुई है। कैपेसिटाबाइन थेरेपी की शुरुआत के कुछ दिनों से लेकर कई महीनों तक ये प्रतिक्रियाएं हुईं और कुछ मामलों में, कैपेसिटाबाइन थेरेपी को बंद करने के एक महीने के भीतर। क्लिनिकल फार्माकोकाइनेटिक इंटरेक्शन अध्ययन में, वारफारिन की एक 20 मिलीग्राम खुराक के प्रशासन के बाद, कैपेसिटाबाइन के साथ उपचार में एस-वारफारिन एयूसी में 57% की वृद्धि हुई, जिसमें INR में 91% की वृद्धि हुई। चूंकि आर-वारफारिन के चयापचय में बदलाव नहीं किया गया था, इन आंकड़ों से पता चलता है कि कैपेसिटाबाइन आइसोनिजाइम 2C9 को कम करता है, लेकिन आइसोनिजाइम 1A2 और 3A4 पर कोई प्रभाव नहीं पड़ता है। कैमारिन-व्युत्पन्न एंटीकोआगुलंट्स को कैपेसिटाबाइन के साथ लेने वाले रोगियों में परिवर्तन की संभावित घटना के लिए नियमित रूप से निगरानी की जानी चाहिए। जमावट पैरामीटर (पीटी या आईएनआर) और एंटीकोआगुलंट्स की खुराक को तदनुसार समायोजित किया जाना चाहिए।
फ़िनाइटोइन: प्लाज्मा फ़िनाइटोइन सांद्रता में वृद्धि कैपेसिटाबाइन और फ़िनाइटोइन के सहवर्ती उपयोग के दौरान दर्ज की गई है, जिसके परिणामस्वरूप व्यक्तिगत मामलों में फ़िनाइटोइन नशा के लक्षण दिखाई देते हैं। फ़िनाइटोइन के बढ़े हुए प्लाज्मा सांद्रता की किसी भी घटना के लिए कैपेसिटाबाइन के साथ फ़िनाइटोइन लेने वाले रोगियों की नियमित रूप से निगरानी की जानी चाहिए।
फोलिक एसिड / फोलिक एसिड: कैपेसिटाबाइन और फोलिनिक एसिड के संयोजन से जुड़े एक अध्ययन से पता चला है कि कैपेसिटाबाइन और इसके मेटाबोलाइट्स के फार्माकोकाइनेटिक्स पर फोलिनिक एसिड का कोई महत्वपूर्ण प्रभाव नहीं है। हालांकि, फोलिनिक एसिड कैपेसिटाबाइन के फार्माकोडायनामिक्स पर प्रभाव पैदा करता है जिसकी विषाक्तता फोलिनिक एसिड द्वारा बढ़ाई जा सकती है: इंटरमिटेंट रेजिमेंस में कैपेसिटाबाइन मोनोथेरेपी की अधिकतम सहनशील खुराक (एमटीडी) प्रति दिन 3000 मिलीग्राम / एम 2 है, जबकि जब कैपेसिटाबाइन फोलिनिक एसिड से जुड़ा था ( 30 मिलीग्राम पीओ दो बार दैनिक) अधिकतम सहनशील खुराक प्रति दिन केवल 2000 मिलीग्राम / एम 2 तक गिर गई। 5-एफयू / एलवी से कैपेसिटाबाइन-आधारित आहार पर स्विच करते समय विषाक्तता में वृद्धि प्रासंगिक हो सकती है। फोलिनिक एसिड और फोलिक एसिड के बीच समानता के कारण बढ़ी हुई विषाक्तता फोलेट की कमी के उपचार में फोलिक एसिड के पूरक के साथ भी प्रासंगिक हो सकती है। .
सोरिवुडिन और एनालॉग्स: डायहाइड्रोपाइरीमिडीन डिहाइड्रोजनेज के सोरिवुडिन निषेध के परिणामस्वरूप सोरिवुडिन और 5-एफयू के बीच एक नैदानिक रूप से महत्वपूर्ण दवा-दवा बातचीत की सूचना मिली है। यह अंतःक्रिया, जिससे फ्लोरोपाइरीमिडीन विषाक्तता बढ़ जाती है, संभावित रूप से घातक है। इस कारण से कैपेसिटाबाइन को सोरिवुडिन या इसके रासायनिक रूप से संबंधित एनालॉग्स, जैसे कि ब्रिवुडिन (खंड 4.3 देखें) के साथ सहवर्ती रूप से प्रशासित नहीं किया जाना चाहिए। सोरिवुडिन या इसके रासायनिक रूप से संबंधित एनालॉग्स, जैसे कि ब्रिवुडिन, और कैपेसिटाबाइन थेरेपी की शुरुआत के साथ उपचार के अंत के बीच कम से कम 4 सप्ताह की आराम अवधि देखी जानी चाहिए।
एंटासिड्स: कैपेसिटाबाइन के फार्माकोकाइनेटिक्स पर एल्यूमीनियम हाइड्रॉक्साइड और मैग्नीशियम हाइड्रॉक्साइड युक्त एक एंटासिड के प्रभाव की जांच की गई। कैपेसिटाबाइन और एक मेटाबोलाइट (5 "-DFCR) के प्लाज्मा सांद्रता में मामूली वृद्धि हुई थी; 3 प्रमुख मेटाबोलाइट्स (5 "-DFUR, 5-FU और FBAL) पर कोई प्रभाव नहीं पड़ा।
एलोप्यूरिनॉल: एलोप्यूरिनॉल के साथ 5-एफयू की बातचीत देखी गई है, 5-एफयू की संभावित कम प्रभावकारिता के साथ एलोप्यूरिनॉल और कैपेसिटाबाइन के सहवर्ती उपयोग से बचा जाना चाहिए।
इंटरफेरॉन अल्फा: कैपेसिटाबाइन की अधिकतम सहनशील खुराक (एमटीडी) 2000 मिलीग्राम / एम 2 प्रति दिन थी जब इंटरफेरॉन अल्फ़ा -2 ए (3 एमआईयू / एम 2 प्रति दिन) के साथ संयोजन में लिया गया था, जबकि प्रति दिन 3000 मिलीग्राम / एम 2 की तुलना में जब कैपेसिटाबाइन अकेले प्रशासित किया गया था।
रेडियोथेरेपी: आंतरायिक आहार का उपयोग करते हुए कैपेसिटाबाइन मोनोथेरेपी की अधिकतम सहनशील खुराक (एमटीडी) प्रति दिन 3000 मिलीग्राम / एम 2 है, जबकि रेक्टल कैंसर के लिए रेडियोथेरेपी के साथ संयुक्त होने पर, कैपेसिटाबाइन की अधिकतम सहनशील खुराक (एमटीडी) प्रति दिन 2000 मिलीग्राम / एम 2 है। 6 सप्ताह के रेडियोथेरेपी उपचार चक्र के संयोजन के साथ सोमवार से शुक्रवार तक या तो निरंतर खुराक या दैनिक खुराक।
ऑक्सिप्लिप्टिन: कैपेसिटाबाइन या इसके मेटाबोलाइट्स, मुक्त प्लैटिनम या कुल प्लैटिनम के संपर्क में कोई नैदानिक रूप से महत्वपूर्ण अंतर नहीं था जब कैपेसिटाबाइन को ऑक्सिप्लिप्टिन के साथ या ऑक्सिप्लिप्टिन और बेवाकिज़ुमैब के संयोजन में प्रशासित किया गया था।
बेवाकिज़ुमाब: ऑक्सिप्लिप्टिन की उपस्थिति में केपेसिटाबाइन या इसके मेटाबोलाइट्स के फार्माकोकाइनेटिक मापदंडों पर बेवाकिज़ुमैब का कोई नैदानिक रूप से महत्वपूर्ण प्रभाव नहीं था।
भोजन के साथ बातचीत
सभी नैदानिक अध्ययनों में, रोगियों को भोजन के बाद 30 मिनट के भीतर कैपेसिटाबाइन लेने की सलाह दी गई थी।चूंकि वर्तमान सुरक्षा और प्रभावकारिता डेटा भोजन के साथ औषधीय उत्पाद के प्रशासन पर आधारित है, यह अनुशंसा की जाती है कि कैपेसिटाबाइन को भोजन के साथ प्रशासित किया जाए। भोजन के साथ प्रशासन कैपेसिटाबाइन के अवशोषण की दर को कम करता है (खंड 5.2 देखें)।
04.6 गर्भावस्था और स्तनपान
प्रसव उम्र की महिलाएं / पुरुषों और महिलाओं में गर्भनिरोधक
कैपेसिटाबाइन के साथ उपचार के दौरान प्रसव क्षमता वाली महिलाओं को गर्भावस्था के जोखिम से बचने की सलाह दी जानी चाहिए। यदि कैपेसिटाबाइन के साथ उपचार के दौरान गर्भावस्था होती है, तो रोगी को भ्रूण को संभावित जोखिम के बारे में सूचित किया जाना चाहिए। उपचार के दौरान गर्भनिरोधक की एक प्रभावी विधि का उपयोग किया जाना चाहिए।
गर्भावस्था
गर्भवती महिलाओं में कैपेसिटाबाइन के साथ कोई अध्ययन नहीं किया गया है; हालांकि, यह माना जा सकता है कि गर्भवती महिलाओं को प्रशासित होने पर कैपेसिटाबाइन भ्रूण को नुकसान पहुंचा सकती है। जानवरों में प्रजनन विषाक्तता के अध्ययन में, कैपेसिटाबाइन के प्रशासन के परिणामस्वरूप भ्रूण की घातकता और टेराटोजेनिसिटी हुई। ये परिणाम फ्लोरोपाइरीमिडीन डेरिवेटिव के अपेक्षित प्रभाव हैं। कैपेसिटाबाइन गर्भावस्था में contraindicated है।
खाने का समय
यह अज्ञात है कि मानव दूध में कैपेसिटाबाइन उत्सर्जित होता है या नहीं। स्तनपान कराने वाले चूहे के दूध में केपेसिटाबाइन और इसके मेटाबोलाइट्स की महत्वपूर्ण मात्रा पाई गई। केपेसिटाबाइन उपचार अवधि के दौरान स्तनपान बंद कर दिया जाना चाहिए।
उपजाऊपन
ज़ेलोडा और प्रजनन क्षमता पर इसके प्रभाव का कोई डेटा नहीं है। ज़ेलोडा के प्रमुख अध्ययनों में बच्चे पैदा करने की क्षमता वाली महिलाएं और पुरुष केवल तभी शामिल थे जब वे गर्भावस्था से बचने के लिए अध्ययन की अवधि के लिए और उसके बाद उचित अवधि के लिए पर्याप्त गर्भनिरोधक का उपयोग करने के इच्छुक थे।
पशु अध्ययनों में प्रजनन क्षमता पर प्रभाव देखा गया (खंड 5.3 देखें)।
04.7 मशीनों को चलाने और उपयोग करने की क्षमता पर प्रभाव
कैपेसिटाबाइन का मशीनों को चलाने या उपयोग करने की क्षमता पर मामूली या मध्यम प्रभाव पड़ता है। कैपेसिटाबाइन चक्कर आना, थकान और मतली पैदा कर सकता है।
04.8 अवांछित प्रभाव
सुरक्षा प्रोफ़ाइल का सारांश
कैपेसिटाबाइन की समग्र सुरक्षा प्रोफ़ाइल अकेले कैपेसिटाबाइन के साथ इलाज किए गए 3000 से अधिक रोगियों के डेटा पर आधारित है या कई संकेतों में विभिन्न कीमोथेरेपी रेजीमेंन्स के साथ संयोजन में कैपेसिटाबाइन के साथ इलाज किया गया है। मेटास्टेटिक स्तन कैंसर, मेटास्टेटिक कोलोरेक्टल कैंसर, और एडजुवेंट कोलन कैंसर के साथ रोगी आबादी में कैपेसिटाबाइन मोनोथेरेपी की सुरक्षा प्रोफाइल समान हैं। मुख्य अध्ययनों के विवरण के लिए खंड 5.1 देखें, जिसमें अध्ययन डिजाइन और प्रमुख प्रभावोत्पादकता परिणाम शामिल हैं।
सबसे अधिक रिपोर्ट की गई और / या चिकित्सकीय रूप से प्रासंगिक उपचार-संबंधी प्रतिकूल दवा प्रतिक्रियाएं (एडीआर) गैस्ट्रोइंटेस्टाइनल गड़बड़ी (विशेष रूप से दस्त, मतली, उल्टी, पेट दर्द, स्टामाटाइटिस), हाथ-पैर सिंड्रोम (पामर-प्लांटर एरिथ्रोडायस्थेसिया), थकान, अस्थि, एनोरेक्सिया, कार्डियोटॉक्सिसिटी, वृक्क समारोह का बिगड़ना जहां कार्य पहले से ही बिगड़ा हुआ था और घनास्त्रता / एम्बोलिज्म।
सारणीबद्ध रूप में प्रतिकूल प्रतिक्रियाओं का सारांश
अन्वेषक द्वारा संभावित रूप से या दूर से कैपेसिटाबाइन के प्रशासन से संबंधित एडीआर को अकेले कैपेसिटाबाइन लेने के लिए तालिका 4 में सूचीबद्ध किया गया है और कई संकेतों में विभिन्न कीमोथेरेपी नियमों के संयोजन में कैपेसिटाबाइन लेने के लिए तालिका 5 में सूचीबद्ध किया गया है। एडीआर को उनकी आवृत्ति के अनुसार वर्गीकृत करने के लिए निम्नलिखित शब्दों का उपयोग किया जाता है: बहुत सामान्य (≥ 1/10), सामान्य (≥ 1/100,
कैपेसिटाबाइन मोनोथेरेपी:
तालिका 4 में 1900 से अधिक रोगियों (अध्ययन M66001, SO14695 और SO14796) सहित तीन मुख्य अध्ययनों से सुरक्षा डेटा के एक पूलित विश्लेषण के आधार पर कैपेसिटाबाइन मोनोथेरेपी के उपयोग से जुड़े एडीआर को सूचीबद्ध किया गया है। एडीआर को "समग्र विश्लेषण से प्राप्त समग्र घटना" के अनुसार विशिष्ट आवृत्ति समूह में शामिल किया गया था।
तालिका 4 संबंधित एडीआर का सारांश कैपेसिटाबाइन मोनोथेरेपी के इलाज वाले मरीजों में रिपोर्ट किया गया।
संयोजन चिकित्सा में कैपेसिटाबाइन:
तालिका ५ में ३००० से अधिक रोगियों के सुरक्षा डेटा के आधार पर कई संकेतों में विभिन्न कीमोथेरेपी के संयोजन में कैपेसिटाबाइन के उपयोग से संबंधित एडीआर सूचीबद्ध हैं। एडीआर को उच्चतम घटना के आधार पर विशिष्ट आवृत्ति समूह (बहुत सामान्य या सामान्य) में शामिल किया गया है। मुख्य नैदानिक अध्ययनों में देखा गया है और केवल अगर कैपेसिटाबाइन मोनोथेरेपी के साथ देखे गए लोगों के लिए अतिरिक्त है या यदि कैपेसिटाबाइन मोनोथेरेपी की तुलना में उच्च आवृत्ति समूह से संबंधित है (तालिका 4 देखें)। संयोजन चिकित्सा में कैपेसिटाबाइन के लिए रिपोर्ट किए गए असामान्य एडीआर कैपेसिटाबाइन मोनोथेरेपी या संयोजन औषधीय उत्पादों (साहित्य और / या संबंधित एसपीसी में) के साथ मोनोथेरेपी के लिए रिपोर्ट किए गए एडीआर के अनुरूप हैं।
एडीआर के कुछ संयोजन औषधीय उत्पाद के साथ अक्सर देखी जाने वाली प्रतिक्रियाएं हैं (उदाहरण के लिए डोकैटेक्सेल या ऑक्सिप्लिप्टिन के साथ परिधीय संवेदी न्यूरोपैथी, बेवाकिज़ुमैब के साथ उच्च रक्तचाप); हालांकि, कैपेसिटाबाइन थेरेपी से प्रेरित बिगड़ने को बाहर नहीं किया जा सकता है।
तालिका 5 अकेले कैपेसिटाबाइन के साथ देखे गए या अकेले कैपेसिटाबाइन की तुलना में उच्च आवृत्ति समूह में देखे गए लोगों के अलावा संयोजन चिकित्सा में कैपेसिटाबाइन के इलाज वाले मरीजों में एडीआर का सारांश रिपोर्ट किया गया।
+ प्रत्येक पद के लिए, आवृत्ति की गणना सभी ग्रेडों के एडीआर के आधार पर की गई थी। "+" से चिह्नित शब्दों के लिए, आवृत्ति की गणना ग्रेड 3-4 एडीआर के आधार पर की गई थी। एडीआर को निर्णायक संयोजन चिकित्सा नैदानिक परीक्षणों में देखी गई उच्चतम घटनाओं के आधार पर शामिल किया गया था।
प्रतिकूल प्रतिक्रियाओं के चयन का विवरण
हाथ-पैर सिंड्रोम (खंड 4.4 देखें):
कैपेसिटाबाइन मोनोथेरेपी (बृहदान्त्र कैंसर में सहायक चिकित्सा अध्ययन, मेटास्टेटिक कोलोरेक्टल कैंसर और स्तन कैंसर के उपचार सहित) के अध्ययन में, 1250 मिलीग्राम / एम 2 केपेसिटाबाइन के साथ दिन में दो बार 1 से 14 हर तीन सप्ताह में, किसी भी ग्रेड के हाथ-पैर सिंड्रोम ५३% से ६०% तक की आवृत्ति के साथ देखा गया है; मेटास्टेटिक स्तन कैंसर के उपचार के लिए कैपेसिटाबाइन / डोकेटेक्सेल आर्म में आवृत्ति 63% थी। कैपेसिटाबाइन के साथ संयोजन चिकित्सा में, कैपेसिटाबाइन 1000 मिलीग्राम / एम 2 के साथ दिन में दो बार 1 से 14 दिनों में हर तीन सप्ताह में, हाथ-पैर सिंड्रोम के किसी भी ग्रेड को 22% और 30% की आवृत्ति के साथ देखा गया था।
14 नैदानिक परीक्षणों पर एक मेटा-विश्लेषण के भाग के रूप में, कई संकेतों (बृहदान्त्र, कोलोरेक्टल, गैस्ट्रिक और स्तन कैंसर) में विभिन्न कीमोथेरेपी के संयोजन में कैपेसिटाबाइन मोनोथेरेपी या कैपेसिटाबाइन के साथ इलाज किए गए 4,700 से अधिक रोगियों के डेटा के साथ, हाथ-पैर सिंड्रोम कैपेसिटाबाइन उपचार की शुरुआत से 239 दिनों (95% सीआई: 201, 288) के मध्य के बाद 2066 रोगियों (43%) में कोई भी ग्रेड हुआ। संयुक्त सभी अध्ययनों में "निम्न सहसंयोजकों और हाथ-पैर सिंड्रोम के विकास के जोखिम के बीच सांख्यिकीय रूप से महत्वपूर्ण संबंध था: कैपेसिटाबाइन (ग्राम) की प्रारंभिक खुराक में वृद्धि, कैपेसिटाबाइन (0.1 * किग्रा) की संचयी खुराक में कमी, सापेक्ष वृद्धि पहले 6 हफ्तों में खुराक की तीव्रता, अध्ययन उपचार की अवधि में वृद्धि (सप्ताह), बढ़ती उम्र (10 साल की वृद्धि), महिला लिंग, और अच्छी आधारभूत ईसीओजी प्रदर्शन स्थिति (0 बनाम ≥1)।
अतिसार (खंड 4.4 देखें):
कैपेसिटाबाइन दस्त की शुरुआत को प्रेरित कर सकता है, जिसे 50% रोगियों में देखा गया है।
कैपेसिटाबाइन के साथ इलाज किए गए 4,700 से अधिक रोगियों के डेटा के साथ 14 नैदानिक अध्ययनों के मेटा-विश्लेषण के परिणामों से पता चला है कि संयुक्त सभी अध्ययनों में "निम्नलिखित सहसंयोजकों के बीच सांख्यिकीय रूप से महत्वपूर्ण संबंध और दस्त के विकास के जोखिम में वृद्धि हुई थी: प्रारंभिक खुराक में वृद्धि कैपेसिटाबाइन (ग्राम), अध्ययन उपचार की अवधि में वृद्धि (सप्ताह), बढ़ती उम्र (10 साल की वृद्धि) और महिला लिंग। निम्नलिखित सहसंयोजकों और दस्त के विकास के जोखिम में कमी के बीच एक सांख्यिकीय रूप से महत्वपूर्ण संबंध देखा गया: कैपेसिटाबाइन (0.1 * किग्रा) की संचयी खुराक में वृद्धि और पहले 6 हफ्तों में सापेक्ष खुराक की तीव्रता में वृद्धि।
कार्डियोटॉक्सिसिटी (खंड 4.4 देखें):
टेबल्स 4 और 5 में वर्णित एडीआर के अलावा, "949 रोगियों (मेटास्टेटिक कोलोरेक्टल कैंसर में 2 चरण III और 5 चरण II के अध्ययन) और मेटास्टेटिक स्तन कैंसर सहित 7 नैदानिक अध्ययनों से नैदानिक सुरक्षा डेटा के एकत्रित विश्लेषण के आधार पर), निम्नलिखित एडीआर 0.1% से कम की घटनाओं के साथ अकेले कैपेसिटाबाइन के उपयोग के साथ देखे गए हैं: कार्डियोमायोपैथी, दिल की विफलता, अचानक मृत्यु और वेंट्रिकुलर एक्सट्रैसिस्टोल।
एन्सेफैलोपैथी:
तालिका 4 और 5 में वर्णित एडीआर के अलावा, 7 नैदानिक अध्ययनों से नैदानिक सुरक्षा डेटा के पूर्वोक्त विश्लेषण के आधार पर, अकेले कैपेसिटाबाइन का उपयोग भी एन्सेफेलोपैथी से जुड़ा था, जिसमें 0.1% से कम की घटना होती है।
विशेष आबादी
उन्नत आयु के रोगी (देखें खंड 4.2 ):
कैपेसिटाबाइन मोनोथेरेपी के साथ इलाज किए गए 60 वर्ष की आयु के रोगियों में सुरक्षा डेटा का विश्लेषण और कैपेसिटाबाइन और डोकेटेक्सेल के चिकित्सीय संयोजन के साथ इलाज किए गए रोगियों के विश्लेषण ने ग्रेड 3 और 4 प्रतिकूल प्रतिक्रियाओं की बढ़ती घटनाओं को दिखाया, उपचार से संबंधित और उपचार से संबंधित 60 वर्ष से कम आयु के रोगियों की तुलना में गंभीर प्रतिकूल प्रतिक्रियाएं। इसके अलावा, 60 वर्ष से कम आयु के रोगियों की तुलना में अधिक लगातार प्रतिकूल प्रतिक्रियाओं के कारण कैपेसिटाबाइन और डोकेटेक्सेल के साथ इलाज किए गए 60 वर्ष की आयु के रोगियों ने समय से पहले उपचार बंद कर दिया।
कैपेसिटाबाइन के साथ इलाज किए गए 4,700 से अधिक रोगियों के डेटा के साथ 14 नैदानिक अध्ययनों के मेटा-विश्लेषण के परिणामों से पता चला है कि संयुक्त सभी अध्ययनों में उम्र में उन्नति (10-वर्ष की वृद्धि) और एक बढ़ा हुआ जोखिम के बीच "सांख्यिकीय रूप से महत्वपूर्ण संबंध" था। हाथ-पैर के सिंड्रोम और दस्त के विकास और न्यूट्रोपेनिया के विकास के जोखिम को कम करने के लिए।
लिंग
कैपेसिटाबाइन के साथ इलाज किए गए 4,700 से अधिक रोगियों के डेटा के साथ 14 नैदानिक परीक्षणों के मेटा-विश्लेषण के परिणामों से पता चला है कि संयुक्त सभी अध्ययनों में "महिला सेक्स के बीच सांख्यिकीय रूप से महत्वपूर्ण संबंध और सिंड्रोम के विकास के जोखिम में वृद्धि हुई थी। हाथ-पैर और दस्त, और न्यूट्रोपेनिया के विकास का एक कम जोखिम।
गुर्दे की हानि वाले रोगी (देखें खंड 4.2, 4.4 और 5.2):
बेसलाइन पर गुर्दे की हानि के साथ कैपेसिटाबाइन मोनोथेरेपी (कोलोरेक्टल कैंसर) के इलाज वाले मरीजों में सुरक्षा डेटा का विश्लेषण सामान्य गुर्दे वाले मरीजों की तुलना में ग्रेड 3 और 4 उपचार से संबंधित प्रतिकूल प्रतिक्रियाओं की बढ़ती घटनाओं को दर्शाता है (गुर्दे की हानि के बिना रोगियों में 36%) एन = २६८ बनाम ४१% हल्की हानि में n = २५७ और ५४% मध्यम n = ५९ में क्रमशः) (खंड ५.२ देखें)। खुराक में कमी की दर (44%) में मामूली बिगड़ा गुर्दे समारोह बनाम 33% और 32% रोगियों में हल्के या बिना गुर्दे की हानि वाले रोगियों में देखा गया और उपचार के समय से पहले विच्छेदन में वृद्धि (पहले दो के दौरान 21% रुकावट) चक्र) बनाम 5% और 8% कम या कोई गुर्दे की हानि वाले रोगियों में।
संदिग्ध प्रतिकूल प्रतिक्रियाओं की रिपोर्टिंग
औषधीय उत्पाद के प्राधिकरण के बाद होने वाली संदिग्ध प्रतिकूल प्रतिक्रियाओं की रिपोर्ट करना महत्वपूर्ण है क्योंकि यह औषधीय उत्पाद के लाभ/जोखिम संतुलन की निरंतर निगरानी की अनुमति देता है। स्वास्थ्य देखभाल पेशेवरों को राष्ट्रीय रिपोर्टिंग प्रणाली www .agenziafarmaco.gov के माध्यम से किसी भी संदिग्ध प्रतिकूल प्रतिक्रिया की रिपोर्ट करने के लिए कहा जाता है। .it / it / जिम्मेदार।
04.9 ओवरडोज
तीव्र ओवरडोज के प्रकट होने में मतली, उल्टी, दस्त, म्यूकोसाइटिस, गैस्ट्रोइंटेस्टाइनल जलन और रक्तस्राव, साथ ही अस्थि मज्जा अवसाद शामिल हैं। ओवरडोज का नैदानिक प्रबंधन पारंपरिक चिकित्सा और सहायक चिकित्सा हस्तक्षेप के माध्यम से होना चाहिए ताकि मौजूद नैदानिक अभिव्यक्तियों को ठीक किया जा सके और किसी भी संभावित जटिलताओं को रोका जा सके।
05.0 औषधीय गुण
05.1 फार्माकोडायनामिक गुण
भेषज समूह: साइटोस्टैटिक (एंटीमेटाबोलाइट)।
एटीसी कोड: L01BC06।
कैपेसिटाबाइन एक गैर-साइटोटॉक्सिक फ्लोरोपाइरीमिडीन कार्बामेट है जो साइटोटोक्सिक फॉर्म 5-फ्लूरोरासिल (5-एफयू) के मौखिक रूप से प्रशासित अग्रदूत के रूप में कार्य करता है। कैपेसिटाबाइन कई एंजाइमी चरणों के माध्यम से सक्रिय होता है (खंड ५.२ देखें)। 5-एफयू में अंतिम रूपांतरण में शामिल एंजाइम, थाइमिडीन फॉस्फोराइलेज (थाइपेस), ट्यूमर के ऊतकों में पाया जाता है, लेकिन सामान्य ऊतकों में भी, हालांकि आम तौर पर कम सांद्रता में। मानव xenograft ट्यूमर मॉडल में, कैपेसिटाबाइन को दिखाया गया है docetaxel के साथ संयोजन में सहक्रियात्मक प्रभाव, जो docetaxel द्वारा थाइमिडीन फॉस्फोरिलेज़ के हाइपरगुलेशन से संबंधित हो सकता है।
एनाबॉलिक मार्ग में 5-एफयू के चयापचय को डीऑक्सीयूरिडिल एसिड की थाइमिडाइल एसिड की मिथाइलेशन प्रतिक्रिया को अवरुद्ध करने के लिए देखा गया है, इस प्रकार डीऑक्सीराइबोन्यूक्लिक एसिड (डीएनए) के संश्लेषण में हस्तक्षेप होता है। 5-एफयू को शामिल करने से आरएनए और प्रोटीन संश्लेषण का निषेध भी होता है। चूंकि डीएनए और आरएनए कोशिका विभाजन और वृद्धि के लिए आवश्यक हैं, 5-एफयू के परिणामस्वरूप थाइमिडीन की कमी हो सकती है जो असंतुलित वृद्धि और कोशिका मृत्यु का कारण बनती है। डीएनए और आरएनए की कमी के प्रभाव विशेष रूप से उन कोशिकाओं में चिह्नित होते हैं जो तेजी से बढ़ते हैं और 5-एफयू तेजी से चयापचय करते हैं।
कोलन और कोलोरेक्टल कैंसर:
कोलन कैंसर के सहायक उपचार में कैपेसिटाबाइन मोनोथेरेपी
स्टेज III (ड्यूक्स सी) कोलन कैंसर के रोगियों में एक बहुकेंद्र, यादृच्छिक, नियंत्रित चरण III नैदानिक परीक्षण से डेटा, कोलन कैंसर (एक्स-एसीटी स्टडी, एम 66001) के रोगियों में सहायक चिकित्सा के लिए कैपेसिटाबाइन के उपयोग का समर्थन करता है। इस अध्ययन में, 1987 रोगियों को कैपेसिटाबाइन (1250 मिलीग्राम / एम 2 दिन में दो बार 2 सप्ताह के लिए, इसके बाद 1 सप्ताह की छुट्टी, 24 सप्ताह के लिए 3 सप्ताह के चक्र के रूप में) या 5-एफयू और ल्यूकोवोरिन (मेयो क्लिनिक अनुसूची: 20 मिलीग्राम / एम 2 IV ल्यूकोवोरिन) के साथ इलाज के लिए यादृच्छिक किया गया था। इसके बाद 425 mg/m2 IV 5-FU बोलस, 1 से 5 दिनों में, 24 सप्ताह के लिए हर 28 दिनों में) कैपेसिटाबाइन प्रति प्रोटोकॉल आबादी (एचआर) में रोग-मुक्त अस्तित्व में कम से कम 5-एफयू / एलवी IV के बराबर था। ०.९२; ९५% सीआई: ०.८०-१.०६) रोग मुक्त अस्तित्व और समग्र अस्तित्व ने ०.८८ का एचआर दिखाया (९५% सीआई: ०.७७-१.०१; पी = ०.०६८) और ०.८६ (९५% सीआई: ०.७४-१.०१; पी = ०.०६०) क्रमशः। विश्लेषण के समय औसत अनुवर्ती 6.9 वर्ष था। पहले से नियोजित बहुभिन्नरूपी कॉक्स विश्लेषण में, 5-एफयू / एलवी बोलस से अधिक कैपेसिटाबाइन की श्रेष्ठता का प्रदर्शन किया गया था। मॉडल में शामिल करने के लिए सांख्यिकीय विश्लेषण में निम्नलिखित कारकों को पूर्वनिर्धारित किया गया था: आयु, सर्जरी से यादृच्छिकरण तक का समय, लिंग, बेसलाइन सीईए स्तर, बेसलाइन लिम्फ नोड्स और देश। यादृच्छिक आबादी में, कैपेसिटाबाइन को रोग-मुक्त अस्तित्व (एचआर: 0.849; 95% सीआई: 0.739-0.976; पी = 0.0212) और समग्र अस्तित्व (एचआर) दोनों के मामले में 5-एफयू / एलवी से बेहतर दिखाया गया था। : ०.८२८; ९५% सीआई: ०.७०५-०.९७१; पी = ०.०२०३)।
पेट के कैंसर के सहायक उपचार में संयोजन चिकित्सा
स्टेज III (ड्यूक्स सी) कोलन कैंसर के रोगियों में एक बहुकेंद्र, यादृच्छिक, नियंत्रित, चरण III नैदानिक परीक्षण से डेटा, कोलन कैंसर के रोगियों में सहायक उपचार के लिए ऑक्सिप्लिप्टिन (XELOX) के साथ संयोजन में कैपेसिटाबाइन के उपयोग का समर्थन करता है (अध्ययन NO16968)। इस अध्ययन में, 944 रोगियों को ऑक्सिप्लिप्टिन (130 मिलीग्राम / एम 2 अंतःशिरा जलसेक के रूप में) के साथ संयोजन में कैपेसिटाबाइन (2 सप्ताह के लिए प्रतिदिन दो बार 1000 मिलीग्राम / एम 2, इसके बाद 1 सप्ताह की छुट्टी, 24 सप्ताह के लिए 3 सप्ताह के पाठ्यक्रम के रूप में) के साथ इलाज के लिए यादृच्छिक किया गया था। प्रत्येक 3 सप्ताह में 1 दिन पर 2 घंटे के लिए); 942 रोगियों को बोलस 5-एफयू और ल्यूकोवोरिन के साथ इलाज के लिए यादृच्छिक किया गया था। आईटीटी आबादी में डीएफएस के लिए प्राथमिक विश्लेषण में, ज़ेलॉक्स को 5-एफयू / एलवी से काफी बेहतर दिखाया गया था ( एचआर = ०.८०, ९५% सीआई = [०.६९; ०.९३]; पी = ०.००४५)। XELOX आर्म में 3 साल की DFS दर 71% थी, जबकि 5-FU / LV आर्म में 67% थी। RFS के सेकेंडरी एंडपॉइंट के लिए किया गया विश्लेषण, XELOX आर्म में 0.78 (95% CI = [0.67; 0.92]; p = 0.0024) के HR के साथ 5-FU / LV के साथ इलाज किए गए परिणामों की तुलना में इन परिणामों का समर्थन करता है। XELOX ने 0.87 (95% CI = [0.72, 1.05]; p = 0.1486) के HR के साथ OS के संदर्भ में श्रेष्ठता की प्रवृत्ति का प्रदर्शन किया, जो मृत्यु के जोखिम में 13% की कमी का अनुवाद करता है। XELOX के लिए 5 साल की OS दर 78% बनाम 5-FU / LV के लिए 74% थी। प्रभावशीलता डेटा ओएस के लिए 59 महीने और डीएफएस के लिए 57 महीने के औसत अवलोकन समय पर आधारित हैं। प्रतिकूल घटनाओं के लिए अध्ययन वापसी दर 5-एफयू / एलवी मोनोथेरेपी शाखा की तुलना में एक्सईएलओएक्स शाखा (21%) में अधिक थी। (9%) आईटीटी आबादी में।
मेटास्टेटिक कोलोरेक्टल कैंसर में कैपेसिटाबाइन मोनोथेरेपी
दो समान रूप से डिज़ाइन किए गए, बहुकेंद्र, यादृच्छिक, नियंत्रित चरण III नैदानिक परीक्षणों (SO14695: SO14796) से डेटा मेटास्टेटिक कोलोरेक्टल कैंसर के प्रथम-पंक्ति उपचार के लिए कैपेसिटाबाइन के उपयोग का समर्थन करता है। इन अध्ययनों में, 603 रोगियों को कैपेसिटाबाइन (1250 मिलीग्राम) के साथ इलाज के लिए यादृच्छिक किया गया था। / एम२ २ सप्ताह के लिए प्रतिदिन दो बार, उसके बाद १ सप्ताह का आराम, और ३ सप्ताह के चक्रों में प्रशासित। ६०४ रोगियों को ५-एफयू और ल्यूकोवोरिन के साथ उपचार के लिए यादृच्छिक किया गया (रेजिमेन मेयो: २० मिलीग्राम / एम२ iv ल्यूकोवोरिन उसके बाद ४२५ मिलीग्राम / एम 2 अंतःशिरा बोलस 5-एफयू, 1 से 5 दिनों में, हर 28 दिनों में)। अन्वेषक) थे: 25.7% (कैपेसिटाबाइन) बनाम 16.7% (मेयो रेजिमेन); पी
मेटास्टेटिक कोलोरेक्टल कैंसर के प्रथम-पंक्ति उपचार में संयोजन चिकित्सा
मेटास्टेटिक कोलोरेक्टल कैंसर के प्रथम-पंक्ति उपचार के लिए एक बहुकेंद्र, यादृच्छिक, नियंत्रित चरण III नैदानिक परीक्षण (NO16966) से डेटा ऑक्सिप्लिप्टिन के साथ संयोजन में या ऑक्सिप्लिप्टिन और बेवाकिज़ुमैब के संयोजन में कैपेसिटाबाइन के उपयोग का समर्थन करता है। अध्ययन में दो भाग शामिल थे: एक प्रारंभिक दो -आर्म भाग जिसमें 634 रोगियों को दो अलग-अलग उपचार आहारों, अर्थात् XELOX या FOLFOX-4, और उसके बाद के 2x2 फैक्टोरियल भाग में यादृच्छिक किया गया था जिसमें 1401 रोगियों को चार अलग-अलग उपचार आहारों में यादृच्छिक किया गया था। उपचार, अर्थात XELOX प्लस प्लेसबो, FOLFOX-4 प्लस प्लेसबो, ज़ेलॉक्स प्लस बेवाकिज़ुमैब और फ़ोलफ़ॉक्स -4 प्लस बेवाकिज़ुमैब उपचार के नियमों के लिए तालिका 6 देखें।
तालिका 6 अध्ययन NO16966 (mCRC) में उपचार के नियम
समग्र तुलना में, FOLFOX-4 युक्त हथियारों की तुलना में XELOX युक्त हथियारों की गैर-हीनता को पात्र रोगी आबादी में प्रगति-मुक्त अस्तित्व और इलाज के इरादे से आबादी (तालिका 7 देखें) के संदर्भ में प्रदर्शित किया गया था। परिणाम दर्शाते हैं कि समग्र अस्तित्व के संदर्भ में XELOX FOLFOX-4 के बराबर है (तालिका 7 देखें)। XELOX plus bevacizumab बनाम FOLFOX-4 plus bevacizumab की तुलना में एक "पूर्व-नियोजित खोजपूर्ण विश्लेषण शामिल था। इन उपचार उपसमूहों की तुलना करते समय, XELOX plus bevacizumab प्रगति-मुक्त अस्तित्व के मामले में FOLFOX-4 प्लस bevacizumab के समान था (HR1.01; ९७.५% सीआई: ०.८४ - १.२२) इंटेंट-टू-ट्रीट आबादी में प्राथमिक विश्लेषण के समय औसत अनुवर्ती १.५ वर्ष था; अनुवर्ती के एक अतिरिक्त वर्ष के बाद किए गए विश्लेषणों से प्राप्त डेटा भी इसमें शामिल हैं तालिका 7. उपचार के दौरान पीएफएस के विश्लेषण ने सामान्य पीएफएस और ओएस के विश्लेषण के परिणामों की पुष्टि नहीं की: एक्सईएलओएक्स बनाम एफओएलएफओएक्स -4 का खतरा अनुपात 1.24 था जिसमें 97.5% सीआई: 1.07 - 1.44 था। हालांकि संवेदनशीलता विश्लेषण से पता चलता है कि अंतर आहार योजना और ट्यूमर मूल्यांकन समय उपचार के दौरान पीएफएस विश्लेषण को प्रभावित करते हैं, इस परिणाम के लिए कोई निश्चित स्पष्टीकरण नहीं मिला।
तालिका 7 अध्ययन संख्या १६९६६ के गैर-हीनता विश्लेषण के लिए प्रमुख प्रभावकारिता परिणाम
* पीपीई = पात्र रोगियों की जनसंख्या; ** आईटीटी = इलाज के इरादे से आबादी।
चरण III में, यादृच्छिक, नियंत्रित अध्ययन (सीएआईआरओ), प्रथम-पंक्ति उपचार के लिए इरिनोटेकन के साथ संयोजन में प्रत्येक 3 सप्ताह में 1000 मिलीग्राम / एम 2 की प्रारंभिक खुराक पर कैपेसिटाबाइन का उपयोग करने के प्रभाव की जांच की गई। कैंसर। अनुक्रमिक (एन = 410) या संयोजन (एन = 410) उपचार प्राप्त करने के लिए 820 रोगियों को यादृच्छिक बनाया गया था। अनुक्रमिक उपचार में कैपेसिटाबाइन के साथ प्रथम-पंक्ति उपचार (14 दिनों के लिए प्रतिदिन दो बार १२५० मिलीग्राम/एम२), इरिनोटेकन के साथ दूसरी-पंक्ति उपचार (१ दिन पर ३५० मिलीग्राम/एम२), और कैपेसिटाबाइन के साथ एक तीसरी-पंक्ति संयोजन शामिल है। (१०००) मिलीग्राम / एम २ 14 दिनों के लिए दो बार दैनिक) और ऑक्सिप्लिप्टिन (१३० मिलीग्राम / एम २ दिन १)। संयोजन उपचार में कैपेसिटाबाइन के साथ पहली पंक्ति का उपचार शामिल था (१४ दिनों के लिए १४० मिलीग्राम / एम २ प्रतिदिन दो बार ) इरिनोटेकन (२५० मिलीग्राम / एम २) के साथ संयुक्त दिन १) (XELIRI) और कैपेसिटाबाइन के साथ दूसरी पंक्ति (१४ दिनों के लिए प्रतिदिन दो बार १००० मिलीग्राम / एम २) प्लस ऑक्सिप्लिप्टिन (१३० मिलीग्राम / एम २ दिन १)। ३ सप्ताह के अंतराल पर दिए गए। प्रथम-पंक्ति उपचार में, इंटेंट-टू-ट्रीट आबादी में औसत प्रगति-मुक्त अस्तित्व कैपेसिटाबाइन मोनोथेरेपी के लिए 5.8 महीने (95% सीआई; 5.1 - 6.2 महीने) और XELIRI के लिए 7.8 महीने (95% सीआई: 7.0 - 8.3 महीने; पी = 0.0002) था। यह XELIRI (क्रमशः XELIRI और प्रथम-पंक्ति कैपेसिटाबाइन के लिए 26% और 11%) के साथ प्रथम-पंक्ति उपचार के दौरान गैस्ट्रोइंटेस्टाइनल विषाक्तता और न्यूट्रोपेनिया की बढ़ती घटनाओं से जुड़ा था।
मेटास्टेटिक कोलोरेक्टल कैंसर के रोगियों में तीन यादृच्छिक अध्ययनों में, XELIRI आहार की तुलना 5-FU + irinotecan (FOLFIRI) से की गई थी। XELIRI रेजिमेंस में कैपेसिटाबाइन 1000 mg / m2 को तीन सप्ताह के चक्र के 1 से 14 दिनों में दिन में दो बार irinotecan 250 mg / m2 के साथ मिलाकर 1 दिन में शामिल किया गया था। बड़े अध्ययन (BICC-C) में, रोगियों को ओपन-लेबल के लिए यादृच्छिक किया गया था। FOLFIRI (n = 144), बोलस 5-FU (mIFL) (n = 145) या XELIRI (n = 141) के साथ उपचार और आगे डबल-ब्लाइंड सेलेकॉक्सिब या प्लेसिबो के लिए यादृच्छिक। FOLFIRI के लिए माध्य PFS 7.6 महीने, mIFL के लिए 5.9 महीने (FOLFIRI के साथ तुलना के लिए p = 0.004) और XELIRI के लिए 5.8 महीने (p = 0.015) था। FOLFIRI के लिए मेडियन OS 23.1 महीने, mIFL (p = 0.09) के लिए 17.6 महीने और XELIRI (p = 0.27) के लिए 18.9 महीने था। XELIRI के साथ इलाज किए गए मरीजों ने FOLFIRI के साथ इलाज किए गए लोगों की तुलना में अत्यधिक गैस्ट्रोनिन्टेस्टिनल विषाक्तता का अनुभव किया (48% और 14% डायरिया के लिए) XELIRI और FOLFIRI, क्रमशः)।
EORTC अध्ययन में, रोगियों को FOLFIRI (n = 41) या XELIRI (n = 44) के साथ ओपन-लेबल उपचार के लिए यादृच्छिक किया गया और आगे डबल-ब्लाइंड सेलेकॉक्सिब या प्लेसिबो के लिए यादृच्छिक किया गया। FOLFIRI (PFS 5.9 बनाम 9.6 महीने और OS 14.8 बनाम 19.9 महीने) की तुलना में XELIRI के लिए माध्य PFS और समग्र अस्तित्व (OS) कम थे; इसके अलावा, XELIRI रेजिमेन (41% XELIRI; 5.1% FOLFIRI) प्राप्त करने वाले रोगियों में अतिसार की अत्यधिक दर की सूचना मिली है।
Skof . द्वारा प्रकाशित अध्ययन में और अन्य।, रोगियों को FOLFIRI या XELIRI प्राप्त करने के लिए यादृच्छिक किया गया था। समग्र प्रतिक्रिया दर XELIRI बांह में ४९% और FOLFIRI बांह में ४८% थी (p = ०.७६)। उपचार के अंत में, XELIRI बांह के 37% रोगियों और FOLFIRI बांह के 26% रोगियों में बीमारी का कोई सबूत नहीं था (p = 0.56)। विषाक्तता उपचार के बीच समान थी, न्यूट्रोपेनिया के अपवाद के साथ, जिसे आमतौर पर FOLFIRI के साथ इलाज किए गए रोगियों में रिपोर्ट किया गया था।
मोंटगनानी एट अल। उन्होंने उपरोक्त तीन अध्ययनों से प्राप्त परिणामों का उपयोग "एमसीआरसी के उपचार में चिकित्सीय आहार FOLFIRI और XELIRI की तुलना में यादृच्छिक अध्ययनों का वैश्विक विश्लेषण" प्रदान करने के लिए किया। FOLFIRI उपचार (HR 0.76; 95% CI: 0.62-0.95; p) से रोग बढ़ने के जोखिम में उल्लेखनीय कमी आई है।
एक यादृच्छिक नैदानिक परीक्षण से डेटा (सौग्लाकोस .) और अन्य।, 2012) FOLFIRI + bevacizumab और XELIRI + bevacizumab के बीच तुलना ने उपचार के बीच PFS और OS के संदर्भ में कोई महत्वपूर्ण अंतर नहीं दिखाया। मरीजों को FOLFIRI प्लस bevacizumab (आर्म A, n = 167) या XELIRI प्लस bevacizumab (आर्म B, n = 166) के साथ इलाज के लिए यादृच्छिक किया गया। आर्म बी के लिए, XELIRI ने 14 दिनों के लिए प्रतिदिन दो बार कैपेसिटाबाइन 1000 मिलीग्राम / एम 2 का उपयोग किया + 1 दिन में इरिनोटेकन 250 मिलीग्राम / एम 2। FOLFIRI-Bev के साथ उपचार और क्रमशः XELIRI-Bev के साथ उपचार के लिए, औसत प्रगति-मुक्त अस्तित्व (PFS) ), समग्र अस्तित्व, और प्रतिक्रिया दर इस प्रकार थी: 10.0 महीने और 8.9 महीने (पी = 0.64); २५.७ महीने और २७.५ महीने (पी = ०.५५); ४५.५% और ३९.८% (पी = ०.३२)। XELIRI + bevacizumab के साथ इलाज किए गए मरीजों ने FOLFIRI + bevacizumab के साथ इलाज किए गए रोगियों की तुलना में दस्त, फिब्राइल न्यूट्रोपेनिया और हाथ-पैर की त्वचा की प्रतिक्रियाओं की काफी अधिक घटनाओं की सूचना दी, जिसमें उपचार में देरी, खुराक में कमी और उपचार में रुकावट आई।
एक चरण II, बहुकेंद्र, यादृच्छिक, नियंत्रित अध्ययन (एआईओ केआरके 0604) से डेटा उपचार के लिए इरिनोटेकन और बेवाकिज़ुमैब के संयोजन में हर 3 सप्ताह में 800 मिलीग्राम / एम 2 की शुरुआती खुराक पर कैपेसिटाबाइन के उपयोग का समर्थन करता है। मेटास्टेटिक कोलोरेक्टल कैंसर के रोगी।
120 रोगियों को एक संशोधित XELIRI रेजिमेन के साथ दो सप्ताह के लिए प्रतिदिन दो बार केपेसिटाबाइन 800 मिलीग्राम / एम 2 के साथ यादृच्छिक किया गया था, इसके बाद 7 दिन आराम किया गया था), इरिनोटेकन (200 मिलीग्राम / एम 2 हर 3 सप्ताह में 1 दिन पर 30 मिनट के जलसेक के रूप में), और बेवाकिज़ुमैब (7.5 मिलीग्राम / किग्रा हर 3 सप्ताह में 1 दिन पर 30 से 90 मिनट के लिए संक्रमित); 127 रोगियों को केपेसिटाबाइन (1000 मिलीग्राम / एम 2 दो सप्ताह के लिए दो बार दैनिक आराम के 7 दिनों के बाद), ऑक्सिप्लिप्टिन (130 मिलीग्राम / एम 2 दिन में 2 घंटे के जलसेक के रूप में हर 3 सप्ताह में 1 दिन) और बेवाकिज़ुमैब (7.5 मिलीग्राम) के साथ इलाज के लिए यादृच्छिक किया गया था। / किग्रा हर 3 सप्ताह में 1 दिन 30 से 90 मिनट के लिए संक्रमित)। २६.२ महीने की अध्ययन आबादी के लिए औसत अनुवर्ती अवधि के बाद, उपचार की प्रतिक्रियाएं इस प्रकार थीं:
तालिका 8 एआईओ केआरके अध्ययन के लिए प्रभावकारिता परिणाम
मेटास्टेटिक कोलोरेक्टल कैंसर की दूसरी पंक्ति के उपचार में संयोजन चिकित्सा
चरण III, बहुकेंद्रीय, यादृच्छिक, नियंत्रित नैदानिक परीक्षण (NO16967) से डेटा मेटास्टेटिक कोलोरेक्टल कैंसर के दूसरे-पंक्ति उपचार के लिए ऑक्सिप्लिप्टिन के साथ संयोजन में कैपेसिटाबाइन के उपयोग का समर्थन करता है। इस अध्ययन में मेटास्टेटिक कोलोरेक्टल कैंसर वाले 627 रोगी जिन्हें पिछला उपचार प्राप्त हुआ था इरिनोटेकन के साथ फ्लोरोपाइरीमिडीन-आधारित रेजिमेन के साथ संयोजन में, क्योंकि प्रथम-पंक्ति उपचार को XELOX या FOLFOX-4 के साथ उपचार के लिए यादृच्छिक किया गया था। XELOX और FOLFOX-4 (प्लेसबो या बेवाकिज़ुमैब को शामिल किए बिना) की खुराक के लिए, तालिका 6 देखें। प्रोटोकॉल और इंटेंट-टू-ट्रीट आबादी (तालिका 9 देखें) में प्रगति-मुक्त अस्तित्व के संदर्भ में XELOX को FOLFOX-4 से गैर-अवर साबित किया गया था। परिणाम बताते हैं कि XELOX समग्र अस्तित्व के मामले में FOLFOX -4 के बराबर है। (तालिका 9 देखें) प्राथमिक विश्लेषण के समय मंझला अनुवर्ती आबादी में इरादा-से-इलाज था 2.1 साल में; अनुवर्ती ६ महीनों के बाद किए गए विश्लेषणों के डेटा को भी तालिका ९ में शामिल किया गया है।
तालिका 9 अध्ययन के गैर-हीनता विश्लेषण के लिए प्रमुख प्रभावकारिता परिणाम NO16967
* पीपीपी = प्रति प्रोटोकॉल जनसंख्या; ** आईटीटी = इलाज के इरादे से आबादी।
उन्नत गैस्ट्रिक कैंसर:
उन्नत गैस्ट्रिक कैंसर वाले रोगियों में एक बहुकेंद्र, यादृच्छिक, नियंत्रित चरण III नैदानिक परीक्षण से डेटा उन्नत गैस्ट्रिक कैंसर (एमएल 17032) के प्रथम-पंक्ति उपचार में कैपेसिटाबाइन के उपयोग का समर्थन करता है। इस अध्ययन में, 160 रोगियों को यादृच्छिक बनाया गया था। कैपेसिटाबाइन के साथ उपचार ( 1000 मिलीग्राम / एम 2 2 सप्ताह के लिए प्रतिदिन दो बार 7 दिनों के आराम के बाद) और सिस्प्लैटिन (80 मिलीग्राम / एम 2 हर 3 सप्ताह में 2 घंटे के जलसेक के रूप में)। कुल 156 रोगियों को 5-एफयू (800 मिलीग्राम) के साथ इलाज के लिए यादृच्छिक किया गया था / एम २ प्रति दिन, दिन १ से दिन ५ तक हर ३ सप्ताह में निरंतर जलसेक के रूप में) और सिस्प्लैटिन (८० मिलीग्राम / एम २ हर ३ सप्ताह में १ दिन पर २ घंटे के जलसेक के रूप में)। सिस्प्लैटिन के साथ संयोजन में कैपेसिटाबाइन ने गैर-हीनता का प्रदर्शन किया है प्रति-प्रोटोकॉल विश्लेषण (एचआर ०.८१; ९५% सीआई: ०.६३-१.०४) में प्रगति-मुक्त अस्तित्व के संदर्भ में सिस्प्लैटिन के साथ संयोजन में ५-एफयू। 5.0 महीने (5-एफयू + सिस्प्लैटिन) की तुलना में मेडियन प्रोग्रेस-फ्री सर्वाइवल 5.6 महीने (कैपेसिटाबाइन + सिस्प्लैटिन) था। उत्तरजीविता की अवधि (समग्र अस्तित्व) के लिए जोखिम अनुपात प्रगति-मुक्त अस्तित्व के लिए जोखिम अनुपात के समान था (एचआर ०.८५; ९५% सीआई: ०.६४-१.१३)। जीवित रहने की औसत अवधि 9.3 महीने (5-एफयू + सिस्प्लैटिन) की तुलना में 10.5 महीने (कैपेसिटाबाइन + सिस्प्लैटिन) थी।
चरण III, बहुकेंद्रीय, यादृच्छिक, नैदानिक परीक्षण से डेटा, उन्नत गैस्ट्रिक कैंसर वाले रोगियों में कैपेसिटाबाइन की तुलना 5-एफयू और ऑक्सिप्लिप्टिन और सिस्प्लैटिन से करते हैं, उन्नत गैस्ट्रिक कैंसर (REAL-2) के प्रथम-पंक्ति उपचार में कैपेसिटाबाइन के उपयोग का समर्थन करते हैं। अध्ययन में, 1002 रोगियों को 2x2 फैक्टोरियल डिज़ाइन के साथ निम्नलिखित 4 भुजाओं में से एक में यादृच्छिक किया गया:
-ईसीएफ: एपिरूबिसिन (प्रत्येक 3 सप्ताह में 1 दिन में 50 मिलीग्राम / एम 2), सिस्प्लैटिन (60 मिलीग्राम / एम 2 दिन में 2 घंटे के जलसेक के रूप में 1 हर 3 सप्ताह में) और 5-एफयू (200 मिलीग्राम / एम 2 दैनिक प्रशासित) केंद्रीय कैथेटर के माध्यम से जलसेक जारी है)।
-ईसीएक्स: एपिरूबिसिन (प्रत्येक 3 सप्ताह में 1 दिन में 50 मिलीग्राम / एम 2), सिस्प्लैटिन (60 मिलीग्राम / एम 2 दिन में 2 घंटे के जलसेक के रूप में हर 3 सप्ताह में 1 दिन) और कैपेसिटाबाइन (625 मिलीग्राम / एम 2 उपचार के रूप में दो बार दैनिक) निरंतर)।
- ईओएफ: एपिरूबिसिन (प्रत्येक 3 सप्ताह में 1 दिन में 50 मिलीग्राम / एम 2), ऑक्सिप्लिप्टिन (130 मिलीग्राम / एम 2 दिन में 2 घंटे के जलसेक के रूप में हर 3 सप्ताह में 1 दिन) और 5-एफयू (200 मिलीग्राम / एम 2 प्रतिदिन प्रशासित) केंद्रीय कैथेटर के माध्यम से जलसेक जारी है)।
- ईओएक्स: एपिरूबिसिन (प्रत्येक 3 सप्ताह में 1 दिन में 50 मिलीग्राम / एम 2), ऑक्सिप्लिप्टिन (130 मिलीग्राम / एम 2 दिन में 2 घंटे के जलसेक के रूप में हर 3 सप्ताह में 1 दिन) और कैपेसिटाबाइन (625 मिलीग्राम / एम 2 दिन में दो बार उपचार के रूप में) निरंतर)।
प्रति-प्रोटोकॉल आबादी में प्राथमिक प्रभावकारिता विश्लेषण ने 5-एफयू-आधारित रेजिमेंस (एचआर 0.86; 95% सीआई: 0.8-0.0, 99) और ऑक्सिप्लिप्टिन युक्त रेजिमेंस की तुलना में कैपेसिटाबाइन युक्त रेजिमेंस के लिए समग्र अस्तित्व में गैर-हीनता का प्रदर्शन किया। सिस्प्लैटिन-आधारित रेजिमेंस (एचआर ०.९२; ९५% सीआई: ०.८०-१.१) के लिए। कैपेसिटाबाइन-आधारित रेजिमेंस में मेडियन समग्र अस्तित्व 10.9 महीने और 5-एफयू वाले 9.6 महीने थे। सिस्प्लैटिन-आधारित रेजिमेंस में मेडियन समग्र अस्तित्व 10.0 महीने और ऑक्सिप्लिप्टिन-आधारित रेजिमेंस में 10.4 महीने था।
कैपेसिटाबाइन का उपयोग उन्नत गैस्ट्रिक कैंसर के उपचार में ऑक्सिप्लिप्टिन के साथ संयोजन में भी किया गया है। अकेले कैपेसिटाबाइन के साथ अध्ययन से संकेत मिलता है कि कैपेसिटाबाइन उन्नत गैस्ट्रिक कैंसर में गतिविधि प्रदर्शित करता है।
उन्नत गैस्ट्रिक, कोलन और कोलोरेक्टल कैंसर: मेटा-विश्लेषण
छह नैदानिक अध्ययनों का एक मेटा-विश्लेषण (अध्ययन SO14695, SO14796, M66001, NO16966, NO16967, M17032) अकेले 5-FU के विकल्प के रूप में और गैस्ट्रोइंटेस्टाइनल कैंसर के संयोजन उपचार में कैपेसिटाबाइन के उपयोग का समर्थन करता है। पूल किए गए विश्लेषण में 3097 रोगी शामिल हैं कैपेसिटाबाइन युक्त रेजिमेंस के साथ इलाज किया गया और 3074 रोगियों को 5-एफयू युक्त रेजिमेंस के साथ इलाज किया गया। 5-एफयू युक्त रेजिमेंस के साथ इलाज करने वालों में कैपेसिटाबाइन युक्त रेजिमेंस और 683 दिन (95% सीआई: 646; 715) के साथ इलाज किए गए रोगियों में औसत समग्र अस्तित्व 703 दिन (95% सीआई: 671; 745) था। समग्र अस्तित्व के लिए खतरा अनुपात ०.९४ (९५% सीआई: ०.८९; १.००, पी = ०.०४८९) था, यह दर्शाता है कि कैपेसिटाबाइन युक्त आहार ५-एफयू युक्त गैर-अवर हैं।
स्तन कैंसर
स्थानीय रूप से उन्नत या मेटास्टेटिक स्तन कैंसर में कैपेसिटाबाइन और डोकेटेक्सेल के साथ संयोजन चिकित्सा
चरण III, बहुकेंद्र, यादृच्छिक, नियंत्रित नैदानिक परीक्षण से डेटा साइटोटोक्सिक कीमोथेरेपी की विफलता के बाद स्थानीय रूप से उन्नत या मेटास्टेटिक स्तन कैंसर के रोगियों के उपचार के लिए डोकेटेक्सेल के साथ संयोजन में कैपेसिटाबाइन के उपयोग का समर्थन करता है जिसमें "एंथ्रासाइक्लिन" शामिल है। इस अध्ययन में, 255 रोगियों को कैपेसिटाबाइन (1250 मिलीग्राम / एम 2 दिन में दो बार 2 सप्ताह के लिए) के साथ इलाज के लिए यादृच्छिक किया गया था, इसके बाद 1 सप्ताह की आराम अवधि और डोकेटेक्सेल 75 मिलीग्राम / एम 2 हर 3 सप्ताह में 1 घंटे के अंतःशिरा जलसेक के रूप में)। अकेले डोकैटेक्सेल के साथ इलाज के लिए 256 रोगियों को यादृच्छिक किया गया था (प्रत्येक 3 सप्ताह में 1 घंटे के अंतःशिरा जलसेक के रूप में 100 मिलीग्राम / एम 2)। कैपेसिटाबाइन + डोकेटेक्सेल संयोजन भुजा (पी = 0.0126) में उत्तरजीविता बेहतर थी। 352 दिनों (अकेले डोकेटेक्सेल) की तुलना में मेडियन सर्वाइवल 442 दिन (कैपेसिटाबाइन + डोकेटेक्सेल) था। संपूर्ण यादृच्छिक आबादी (अन्वेषक मूल्यांकन) में समग्र उद्देश्य प्रतिक्रिया दर थे: 41.6% (कैपेसिटाबाइन + डोकेटेक्सेल) बनाम 29.7% (अकेले डोकेटेक्सेल); पी = 0.0058। कैपेसिटाबाइन + डोकेटेक्सेल संयोजन शाखा में प्रगति रोग का समय बेहतर था ( पी
टैक्सेन और एन्थ्रासाइक्लिन युक्त कीमोथेरेपी की विफलता के बाद कैपेसिटाबाइन मोनोथेरेपी और जहां एन्थ्रासाइक्लिन थेरेपी का संकेत नहीं दिया गया है
दो बहुकेंद्रीय चरण II नैदानिक परीक्षणों के डेटा उन रोगियों के उपचार के लिए कैपेसिटाबाइन मोनोथेरेपी के उपयोग का समर्थन करते हैं जो कीमोथेरेपी की विफलता के बाद प्रगति कर रहे हैं जिसमें टैक्सेन और एक एन्थ्रासाइक्लिन शामिल हैं, या जिनके लिए कोई अतिरिक्त चिकित्सा संकेत नहीं दिया गया है। एन्थ्रासाइक्लिन। इन अध्ययनों में, कुल 236 रोगियों में से कैपेसिटाबाइन के साथ इलाज किया गया (1250 मिलीग्राम / एम 2 दिन में दो बार 2 सप्ताह के लिए और 1 सप्ताह की आराम अवधि के बाद)। समग्र उद्देश्य प्रतिक्रिया दर (अन्वेषक मूल्यांकन) 20% (पहला अध्ययन) और 25% (दूसरा अध्ययन) औसत समय था प्रगति ९३ और ९८ दिन थी, औसत उत्तरजीविता ३८४ और ३७३ दिन थी।
सभी संकेत:
अकेले कैपेसिटाबाइन के साथ इलाज किए गए 4,700 से अधिक रोगियों के डेटा के साथ या कई संकेतों (कोलन, कोलोरेक्टल, गैस्ट्रिक और स्तन कैंसर) में विभिन्न कीमोथेरेपी के संयोजन के साथ 14 नैदानिक परीक्षणों का एक मेटा-विश्लेषण ने कैपेसिटाबाइन-उपचारित रोगियों में समग्र अस्तित्व को अधिक लंबे समय तक दिखाया। उन रोगियों की तुलना में विकसित हाथ-पैर सिंड्रोम जिन्होंने नहीं किया: औसत समग्र अस्तित्व 1100 दिन (95% सीआई: 1007, 1200) बनाम 691 दिन (95% सीआई: 638; 754) 0.61 के खतरनाक अनुपात के साथ (95% सीआई: 0.56 , 0.66)।
बाल चिकित्सा जनसंख्या:
यूरोपियन मेडिसिन एजेंसी ने कोलन और रेक्टल एडेनोकार्सिनोमा, गैस्ट्रिक एडेनोकार्सिनोमा और स्तन कैंसर में बाल चिकित्सा आबादी के सभी उपवर्गों में ज़ेलोडा के साथ अध्ययन करने के दायित्व से छूट दी है ("बाल चिकित्सा उपयोग के बारे में जानकारी के लिए खंड 4.2 देखें)।
05.2 फार्माकोकाइनेटिक गुण
कैपेसिटाबाइन के फार्माकोकाइनेटिक्स का मूल्यांकन 502-3514 मिलीग्राम / एम 2 / दिन की खुराक सीमा पर किया गया था। कैपेसिटाबाइन के पैरामीटर, 5 "-डीऑक्सी-5-फ्लोरोसाइटिडाइन (5" -डीएफसीआर) और 5 "-डीऑक्सी-5-फ्लोरोरिडीन (5" डीएफयूआर) 1 और 14 दिनों में समान थे। 14 वें दिन 5-एफयू का एयूसी 30-35% अधिक था। कैपेसिटाबाइन की खुराक में कमी सक्रिय मेटाबोलाइट के गैर-रैखिक फार्माकोकाइनेटिक्स के कारण अधिक खुराक-आनुपातिक तरीके से 5-एफयू के प्रणालीगत जोखिम को कम करती है। ।
अवशोषण
मौखिक प्रशासन के बाद, कैपेसिटाबाइन पूरी तरह से और तेजी से अवशोषित हो जाता है; बाद में यह पूरी तरह से 5 "-DFCR और 5" -DFUR मेटाबोलाइट्स में परिवर्तित हो जाता है। भोजन के साथ प्रशासन कैपेसिटाबाइन की अवशोषण दर को कम करता है, लेकिन केवल 5 "-DFUR के एयूसी और बाद के मेटाबोलाइट 5-एफयू के एयूसी पर मामूली प्रभाव का कारण बनता है। भोजन के बाद प्रशासित 14 दिन पर 1250 मिलीग्राम / एम 2 की खुराक पर, कैपेसिटाबाइन की अधिकतम प्लाज्मा सांद्रता (एमसीजी / एमएल में सीएमएक्स), 5 "-डीएफसीआर, 5" -डीएफयूआर, 5-एफयू और एफबीएएल क्रमशः 4.67 - 3.05 - 12.1 - 0.95 और 5.46 थे। अधिकतम प्लाज्मा सांद्रता तक पहुंचने का समय (टीमैक्स घंटे में) 1.50 - 2.00 - 2.00 - 2.00 और 3.34 था। एमसीजी में एयूसी0- मान • एच / एमएल 7.75 - 7.24 - 24.6 - 2.03 और 36.3 थे।
वितरण
मानव प्लाज्मा अध्ययन किया गया कृत्रिम परिवेशीय ने दिखाया कि कैपेसिटाबाइन, 5 "डीएफसीआर, 5" -डीएफयूआर और 5-एफयू प्रोटीन से बंधे हैं, मुख्य रूप से एल्ब्यूमिन, क्रमशः 54%, 10%, 62% और 10% के प्रतिशत में।
जैव परिवर्तन
कैपेसिटाबाइन को पहले हेपेटिक कार्बोक्साइलेस्टरेज़ द्वारा 5 "-डीएफसीआर में मेटाबोलाइज़ किया जाता है, जिसे बाद में साइटिडीन डेमिनमिनस द्वारा 5" -डीएफयूआर में बदल दिया जाता है, जो मुख्य रूप से यकृत और ट्यूमर के ऊतकों में स्थित होता है। इसके बाद थाइमिडीन फॉस्फोरिलेज (थाइपेस) द्वारा "5 का और उत्प्रेरक सक्रियण" -डीएफयूआर होता है। उत्प्रेरक सक्रियण में शामिल एंजाइम ट्यूमर के ऊतकों में मौजूद होते हैं, लेकिन स्वस्थ ऊतकों में भी होते हैं, हालांकि आम तौर पर कम मात्रा में। 5-एफयू में कैपेसिटाबाइन का अनुक्रमिक एंजाइमेटिक बायोट्रांसफॉर्मेशन नियोप्लास्टिक ऊतकों के भीतर उच्च सांद्रता की ओर जाता है। कोलोरेक्टल कैंसर में, 5-एफयू पीढ़ी ट्यूमर स्ट्रोमल कोशिकाओं में बड़े पैमाने पर स्थानीयकृत प्रतीत होती है। कोलोरेक्टल कैंसर के रोगियों को केपेसिटाबाइन के मौखिक प्रशासन के बाद, कोलोरेक्टल कैंसर में आसन्न ऊतकों में 5-एफयू एकाग्रता का अनुपात 3.2 (0.9 से 8.0 तक) था। ट्यूमर से प्लाज्मा में 5-एफयू सांद्रता का अनुपात 21.4 (3.9 से 59.9, n = 8 तक) था, जबकि स्वस्थ ऊतक में प्लाज्मा का अनुपात 8.9 था (3.0 से 25.8, n = 8 की भिन्नता के साथ)। थाइमिडीन फॉस्फोरिलेज़ गतिविधि को मापा गया और प्राथमिक कोलोरेक्टल कैंसर में आसन्न सामान्य ऊतक में रिपोर्ट किए गए मूल्यों की तुलना में 4 गुना अधिक पाया गया। इम्यूनोहिस्टोकेमिस्ट्री अध्ययनों के आधार पर, थाइमिडीन फॉस्फोरिलेज़ ट्यूमर स्ट्रोमल कोशिकाओं में बड़े पैमाने पर स्थानीयकृत प्रतीत होता है।
5-FU को बाद में एंजाइम डाइहाइड्रोपाइरीमिडीन डिहाइड्रोजनेज (DPD) द्वारा डाइहाइड्रो-5-फ्लूरोरासिल (FUH2) में अपचयित किया जाता है जो कि बहुत कम विषैला होता है। डाइहाइड्रोपाइरीमिडेस 5-फ्लोरो-यूरीडोप्रोपियोनिक एसिड (FUPA) प्राप्त करने के लिए पाइरीमिडीन रिंग पर कार्य करता है। अंत में, β -ureido-propionase FUPA को α-fluoro-β-alanine (FBAL) में बदल देता है जो मूत्र में समाप्त हो जाता है। डायहाइड्रोपाइरीमिडीन डिहाइड्रोजनेज (DPD) की गतिविधि महत्वपूर्ण सीमित कारक है। डीपीडी की कमी "कैपेसिटाबाइन की विषाक्तता को बढ़ा सकती है (खंड 4.3 और 4.4 देखें)।
निकाल देना
कैपेसिटाबाइन, 5 "-डीएफसीआर, 5" -डीएफयूआर, 5-एफयू और एफबीएएल का उन्मूलन आधा जीवन (घंटों में टी 1/2) 0.85 - 1.11 - 0.66 - 0.76 और 3.23 कैपेसिटाबाइन और इसके मेटाबोलाइट्स मुख्य रूप से मूत्र में समाप्त हो जाते हैं। कैपेसिटाबाइन की प्रशासित खुराक का 95.5% मूत्र में बरामद किया गया था। मल का उत्सर्जन न्यूनतम (2.6%) है। मूत्र में उत्सर्जित प्रमुख मेटाबोलाइट एफबीएलए है, जो प्रशासित खुराक का 57% है। प्रशासित खुराक का लगभग 3% मूत्र में अपरिवर्तित दवा के रूप में उत्सर्जित होता है।
एसोसिएशन थेरेपी
डोसेटेक्सेल या पैक्लिटैक्सेल के फार्माकोकाइनेटिक्स पर कैपेसिटाबाइन के प्रभावों का मूल्यांकन करने वाले चरण I के अध्ययन से पता चला है कि डोकेटेक्सेल या पैक्लिटैक्सेल (सीमैक्स और एयूसी) के फार्माकोकाइनेटिक्स पर कैपेसिटाबाइन का कोई प्रभाव नहीं है और डोकेटेक्सेल या पैक्लिटैक्सेल का कोई प्रभाव नहीं है। 5 "-DFUR के फार्माकोकाइनेटिक्स।
विशेष रूप से रोगी आबादी में फार्माकोकाइनेटिक्स
कोलोरेक्टल कैंसर के 505 रोगियों में प्रतिदिन दो बार 1250 मिलीग्राम / एम 2 की खुराक पर प्रशासित कैपेसिटाबाइन के साथ उपचार के बाद जनसंख्या फार्माकोकाइनेटिक विश्लेषण किया गया था। बेसलाइन पर यकृत मेटास्टेस की उपस्थिति या अनुपस्थिति, कर्णॉफ्स्की प्रदर्शन स्थिति, कुल बिलीरुबिन, सीरम एल्ब्यूमिन, एएसएटी और ALAT ने 5 "-DFUR, 5-FU और FBAL के फार्माकोकाइनेटिक्स को सांख्यिकीय रूप से महत्वपूर्ण रूप से प्रभावित नहीं किया।
जिगर मेटास्टेस के कारण बिगड़ा हुआ जिगर समारोह वाले रोगी: एक फार्माकोकाइनेटिक अध्ययन से पता चला है कि कैपेसिटाबाइन की जैवउपलब्धता और 5-एफयू के संपर्क में कैंसर के रोगियों में यकृत मेटास्टेस के कारण हल्के से मध्यम यकृत हानि वाले रोगियों की तुलना में यकृत हानि के बिना रोगियों में फार्माकोकाइनेटिक डेटा के गंभीर यकृत हानि वाले रोगियों में वृद्धि हो सकती है।
बिगड़ा हुआ गुर्दे समारोह वाले रोगी: हल्के से गंभीर गुर्दे की हानि वाले कैंसर रोगियों में किए गए फार्माकोकाइनेटिक अध्ययन के परिणामों के आधार पर, इस बात का कोई सबूत नहीं है कि क्रिएटिनिन निकासी मूल दवा और 5-एफयू के फार्माकोकाइनेटिक्स को प्रभावित करती है। क्रिएटिनिन क्लीयरेंस "5 तक प्रणालीगत जोखिम" -DFUR (एयूसी में 35% वृद्धि जब क्रिएटिनिन क्लीयरेंस 50% कम हो जाता है) और एफबीएएल (एयूसी में 114% वृद्धि जब क्रिएटिनिन क्लीयरेंस 50% कम हो जाता है) को प्रभावित करने के लिए पाया गया था। %)। एफबीएएल एक मेटाबोलाइट है जिसमें कोई एंटीप्रोलिफेरेटिव गतिविधि नहीं होती है।
वरिष्ठ नागरिकों: जनसंख्या के आधार पर विभिन्न आयु (27 से 86 वर्ष) के रोगियों पर किए गए फार्माकोकाइनेटिक विश्लेषण और जिनमें से 234 (46%) रोगी 65 वर्ष या उससे अधिक आयु के थे, आयु 5 "- DFUR और 5-FU के फार्माकोकाइनेटिक्स को प्रभावित नहीं करती है। FBAL का AUC उम्र के साथ बढ़ता है (उम्र में 20% की वृद्धि से FBAL के AUC में 15% की वृद्धि होती है)। यह वृद्धि संभवतः गुर्दे के कार्य में बदलाव के कारण होती है।
जातीय कारक: कैपेसिटाबाइन के मौखिक प्रशासन के बाद 14 दिनों के लिए प्रतिदिन दो बार 825 मिलीग्राम / एम 2, जापानी रोगियों (एन = 18) में कोकेशियान रोगियों (एन = 22) की तुलना में लगभग 36% कम सीएमएक्स और 24% कम एयूसी केपेसिटाबाइन था। जापानी रोगियों में भी कोकेशियान रोगियों की तुलना में FBAL के लिए लगभग 25% कम Cmax और 34% कम AUC था। इन अंतरों की नैदानिक प्रासंगिकता अज्ञात है। अन्य मेटाबोलाइट्स (5 "DFCR, 5" DFUR और 5-FU) के संपर्क में कोई महत्वपूर्ण अंतर नहीं थे।
05.3 प्रीक्लिनिकल सुरक्षा डेटा
बार-बार खुराक विषाक्तता अध्ययनों में, सिनोमोलगस बंदरों और चूहों को मौखिक कैपेसिटाबाइन के दैनिक प्रशासन ने गैस्ट्रोइंटेस्टाइनल, हेमेटोपोएटिक और लिम्फैटिक विषाक्त प्रभावों का उत्पादन किया जो फ्लूरोपाइरीमिडीन के विशिष्ट हैं। ये विषाक्तता प्रतिवर्ती थे। कैपेसिटाबाइन के कारण अपक्षयी / प्रतिगामी परिवर्तनों की विशेषता वाली त्वचा की विषाक्तता देखी गई है। कैपेसिटाबाइन ने यकृत और सीएनएस विषाक्तता का कोई सबूत नहीं दिखाया। कार्डियोवास्कुलर विषाक्तता (जैसे पीआर अंतराल और क्यूटी अंतराल का लम्बा होना) को सिनोमोलगस बंदर में अंतःशिरा प्रशासन (100 मिलीग्राम / किग्रा) के बाद पाया गया है, लेकिन बार-बार खुराक (1379 मिलीग्राम / एम 2 / दिन) के बाद नहीं। ) मौखिक रूप से।
दो साल के माउस कैंसरजन्यता अध्ययन में कैपेसिटाबाइन के कारण कैंसरजन्यता का कोई सबूत नहीं मिला।
मानक प्रजनन अध्ययनों में, कैपेसिटाबाइन लेने वाली मादा चूहों ने प्रजनन संबंधी गड़बड़ी का प्रदर्शन किया; हालांकि दवा के निलंबन की अवधि के बाद यह प्रभाव प्रतिवर्ती था। इसके अलावा, 13 सप्ताह के अध्ययन के दौरान नर चूहों के प्रजनन अंगों में एट्रोफिक और अपक्षयी परिवर्तन पाए गए; हालाँकि, दवा वापसी की अवधि के बाद ये प्रभाव प्रतिवर्ती थे (खंड 4.6 देखें)।
चूहों में भ्रूणोटॉक्सिसिटी और टेराटोजेनिसिटी पर किए गए अध्ययनों ने भ्रूण के पुनर्जीवन और टेराटोजेनिसिटी में खुराक से संबंधित वृद्धि दिखाई।उच्च खुराक पर बंदरों में गर्भपात और भ्रूण की घातकता देखी गई, लेकिन टेराटोजेनिकिटी का कोई सबूत नहीं था।
कैपेसिटाबाइन उत्परिवर्तजन नहीं था कृत्रिम परिवेशीय बैक्टीरिया के लिए (एम्स परीक्षण) या स्तनधारी कोशिकाओं के लिए (चीनी हम्सटर V79 / HPRT जीन उत्परिवर्तन परीक्षण)। हालांकि, अन्य न्यूक्लियोसाइड एनालॉग्स (यानी 5-एफयू) की तरह, कैपेसिटाबाइन मानव लिम्फोसाइटों में क्लैस्टोजेनिक था (कृत्रिम परिवेशीय) और परीक्षण में सकारात्मक रुझान दिखाया (विवो में) माउस अस्थि मज्जा में माइक्रोन्यूक्लि की।
06.0 फार्मास्युटिकल जानकारी
०६.१ अंश:
टैबलेट कोर:
निर्जल लैक्टोज,
क्रोस्कॉर्मेलोसे सोडियम,
हाइपोमेलोज,
माइक्रोक्रिस्टलाइन सेलुलोज,
भ्राजातु स्टीयरेट।
गोली कोटिंग:
हाइपोमेलोज,
टाइटेनियम डाइऑक्साइड (E171),
पीला और लाल आयरन ऑक्साइड (E172),
तालक
06.2 असंगति
संबद्ध नहीं।
06.3 वैधता की अवधि
3 वर्ष।
06.4 भंडारण के लिए विशेष सावधानियां
30 डिग्री सेल्सियस से ऊपर स्टोर न करें।
06.5 तत्काल पैकेजिंग की प्रकृति और पैकेज की सामग्री
प्रकृति: पीवीसी / पीवीडीसी ब्लिस्टर।
सामग्री: 120 फिल्म-लेपित गोलियां (10 गोलियों के 12 छाले)।
06.6 उपयोग और संचालन के लिए निर्देश
कोई विशेष निर्देश नहीं।
07.0 विपणन प्राधिकरण धारक
रोश पंजीकरण लिमिटेड
6 फाल्कन वे
शायर पार्क
वेल्विन गार्डन सिटी
AL7 1TW
यूके
08.0 विपणन प्राधिकरण संख्या
ईयू / 1/00/163/002
035219029
09.0 प्राधिकरण के पहले प्राधिकरण या नवीनीकरण की तिथि
पहले प्राधिकरण की तिथि: 2 फरवरी 2001
अंतिम नवीनीकरण की तिथि: 2 फरवरी, 2006
10.0 पाठ के संशोधन की तिथि
सितंबर 2015