सक्रिय तत्व: रिटक्सिमैब
चमड़े के नीचे इंजेक्शन के लिए MabThera 1400 मिलीग्राम समाधान
मबथेरा पैकेज इंसर्ट पैक आकार के लिए उपलब्ध हैं:- MabThera 100 मिलीग्राम जलसेक के लिए समाधान के लिए ध्यान केंद्रित
- मबथेरा 500 मिलीग्राम जलसेक के समाधान के लिए ध्यान केंद्रित करें
- चमड़े के नीचे इंजेक्शन के लिए MabThera 1400 मिलीग्राम समाधान
संकेत मबथेरा का उपयोग क्यों किया जाता है? ये किसके लिये है?
मबथेरा क्या है?
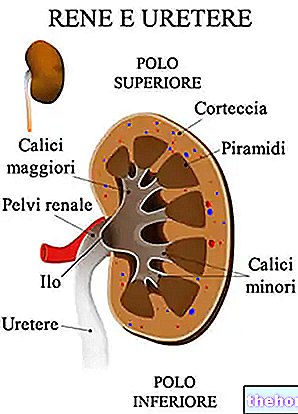
MabThera में सक्रिय पदार्थ 'रीटक्सिमैब' होता है, एक प्रकार का प्रोटीन जिसे 'मोनोक्लोनल एंटीबॉडी' कहा जाता है। रिट्क्सिमैब एक प्रकार की श्वेत रक्त कोशिका की सतह से बंधता है जिसे "बी लिम्फोसाइट्स" कहा जाता है। जब रीटक्सिमैब इन कोशिकाओं की सतह से बंध जाता है, तो यह उनकी मृत्यु का कारण बनता है।
मबथेरा ड्रिप के रूप में दी जाने वाली दवा के रूप में उपलब्ध है (मैबथेरा 100 मिलीग्राम या मैबथेरा 500 मिलीग्राम, जलसेक के लिए समाधान के लिए ध्यान केंद्रित करें) और त्वचा के नीचे इंजेक्शन द्वारा दी जाने वाली दवा के रूप में (मैबथेरा 1400 मिलीग्राम, चमड़े के नीचे इंजेक्शन के लिए समाधान)।
मबथेरा किसके लिए प्रयोग किया जाता है
MabThera का उपयोग वयस्कों में गैर-हॉजकिन के लिंफोमा के इलाज के लिए किया जाता है,
- लिम्फोइड ऊतक की एक बीमारी (जो प्रतिरक्षा प्रणाली का हिस्सा है) जो बी लिम्फोसाइट्स नामक एक प्रकार की सफेद रक्त कोशिका को प्रभावित करती है।
MabThera अकेले या अन्य दवाओं ("कीमोथेरेपी") के साथ दिया जा सकता है।
उपचार की शुरुआत में, आपको हमेशा मबथेरा को ड्रिप (अंतःशिरा जलसेक) के रूप में दिया जाएगा।
इसके बाद आपको त्वचा के नीचे इंजेक्शन द्वारा मबथेरा दिया जाएगा। आपका मैबथेरा इंजेक्शन कब शुरू करना है, यह आपका डॉक्टर तय करेगा।
प्रारंभिक उपचार पूरा होने के बाद, जिन रोगियों की चिकित्सा प्रभावी साबित होती है, उन्हें 2 साल तक रखरखाव उपचार के रूप में MabThera का उपयोग किया जा सकता है।
मबथेरा का सेवन कब नहीं करना चाहिए
मबथेरा न लें:
- यदि आपको रीटक्सिमैब से एलर्जी है, तो रीटक्सिमैब के समान अन्य प्रोटीन या इस दवा के किसी भी अन्य तत्व (धारा 6 में सूचीबद्ध);
- यदि आपको हाइलूरोनिडेस (एक एंजाइम जो इंजेक्शन वाले सक्रिय पदार्थ के अवशोषण को बढ़ाने में मदद करता है) से एलर्जी है,
- यदि आपको "चल रहे गंभीर सक्रिय संक्रमण है,
- यदि आपके पास कमजोर प्रतिरक्षा प्रणाली है।
यदि यह ऊपर सूचीबद्ध किसी भी मामले में आता है तो मबथेरा न लें। यदि आप अनिश्चित हैं, तो मबथेरा दिए जाने से पहले अपने डॉक्टर, फार्मासिस्ट या नर्स से परामर्श करें।
उपयोग के लिए सावधानियां मबथेरा लेने से पहले आपको क्या जानना चाहिए
मबथेरा दिए जाने से पहले अपने डॉक्टर, फार्मासिस्ट या नर्स से बात करें:
- यदि आपको लगता है कि आपको "हेपेटाइटिस संक्रमण" है या पहले भी हो चुका है, क्योंकि कुछ मामलों में मैबथेरा हेपेटाइटिस बी को फिर से सक्रिय कर सकता है, जो बहुत ही दुर्लभ मामलों में घातक हो सकता है। पिछले हेपेटाइटिस बी संक्रमण वाले मरीजों की सावधानीपूर्वक जांच की जाएगी इस संक्रमण के लक्षणों के लिए आपका डॉक्टर;
- यदि आप कभी हृदय रोग (उदाहरण के लिए एनजाइना, धड़कन या दिल की विफलता) से पीड़ित हैं या आपको सांस लेने में समस्या हुई है।
यदि इनमें से कोई भी आप पर लागू होता है, या यदि आप सुनिश्चित नहीं हैं, तो मैबथेरा दिए जाने से पहले अपने डॉक्टर, फार्मासिस्ट या नर्स से बात करें।मबथेरा लेते समय आपके डॉक्टर को आप पर विशेष ध्यान देने की आवश्यकता हो सकती है।
बच्चे और किशोर
यदि आप या आपके बच्चे की आयु 18 वर्ष से कम है, तो यह दवा दिए जाने से पहले अपने डॉक्टर, फार्मासिस्ट या नर्स से बात करें, क्योंकि बच्चों और किशोरों में मबथेरा के उपयोग के बारे में अधिक जानकारी उपलब्ध नहीं है।
कौन सी दवाएं या खाद्य पदार्थ Mabthera के प्रभाव को बदल सकते हैं?
अपने डॉक्टर, फार्मासिस्ट या नर्स को बताएं कि क्या आप ले रहे हैं, हाल ही में लिया है या कोई अन्य दवाएं ले सकते हैं, जिसमें गैर-पर्चे और हर्बल दवाएं शामिल हैं, क्योंकि मैबथेरा अन्य दवाओं के काम करने के तरीके को प्रभावित कर सकता है। वे मैबथेरा के संचालन में हस्तक्षेप कर सकते हैं।
विशेष रूप से, अपने डॉक्टर को बताएं:
- अगर आप हाई ब्लड प्रेशर की दवा ले रहे हैं। आपको मबथेरा दिए जाने से 12 घंटे पहले इसे लेना बंद करने के लिए कहा जा सकता है, क्योंकि कुछ लोगों को इस दवा को लेने के दौरान रक्तचाप में गिरावट आती है;
- यदि आपने कभी ऐसी दवाएं ली हैं जो प्रतिरक्षा प्रणाली को प्रभावित करती हैं - जैसे कि कीमोथेरेपी या इम्यूनोसप्रेसिव दवाएं।
यदि इनमें से कोई भी आप पर लागू होता है, या यदि आप अनिश्चित हैं, तो मबथेरा दिए जाने से पहले अपने डॉक्टर, फार्मासिस्ट या नर्स से बात करें।
चेतावनियाँ यह जानना महत्वपूर्ण है कि:
गर्भावस्था और स्तनपान
यदि आप गर्भवती हैं, तो सोचें कि आप गर्भवती हो सकती हैं या गर्भवती होने की योजना बना रही हैं, कृपया अपने डॉक्टर या नर्स को बताएं। ऐसा इसलिए है क्योंकि मबथेरा नाल को पार कर बच्चे को प्रभावित कर सकता है। यदि संभावना है कि आप मबथेरा लेते समय गर्भवती हो जाएंगी और MabThera के साथ अंतिम उपचार के बाद के १२ महीनों में आपको गर्भनिरोधक के एक प्रभावी तरीके का उपयोग करना होगा। आपको MabThera के साथ उपचार के दौरान और न ही MabThera के साथ अंतिम उपचार के 12 महीने बाद तक स्तनपान नहीं कराना चाहिए। ऐसा इसलिए है क्योंकि MabThera स्तन के दूध में जा सकता है।
ड्राइविंग और मशीनों का उपयोग
यह ज्ञात नहीं है कि मबथेरा उपकरण या मशीनों को चलाने या उपयोग करने की आपकी क्षमता को प्रभावित करेगा या नहीं।
खुराक और उपयोग की विधि मबथेरा का उपयोग कैसे करें: खुराक
इसे कैसे प्रशासित किया जाता है
मबथेरा आपको इस उपचार के उपयोग में अनुभवी डॉक्टर या नर्स द्वारा दिया जाएगा। यदि आप किसी भी दुष्प्रभाव का अनुभव करते हैं, तो वे आपको दवा दिए जाने के दौरान आपकी बारीकी से निगरानी करेंगे।
उपचार की शुरुआत में, आपको हमेशा मबथेरा को ड्रिप (अंतःशिरा जलसेक) के रूप में दिया जाएगा।
इसके बाद आपको त्वचा के नीचे इंजेक्शन द्वारा मबथेरा दिया जाएगा। (उपचर्म इंजेक्शन) लगभग 5 मिनट तक चलता है।
आपका मैबथेरा इंजेक्शन कब शुरू करना है, यह आपका डॉक्टर तय करेगा।
त्वचा के नीचे इंजेक्शन पेट के क्षेत्र में किया जाता है, शरीर में कहीं और नहीं, उन क्षेत्रों से परहेज करते हुए जहां त्वचा लाल, खरोंच, कोमल या सख्त होती है, या जहां तिल या निशान होते हैं।
MabThera के प्रत्येक प्रशासन से पहले दी जाने वाली दवाएं
आपको मबथेरा दिए जाने से पहले, संभावित दुष्प्रभावों को रोकने या कम करने के लिए आपको अन्य दवाएं (पूर्व-दवा) दी जाएंगी। आप कितनी बार और कितनी बार उपचार प्राप्त करेंगे
- MabThera आपको कीमोथेरेपी वाले दिन ही दिया जाएगा। यह आमतौर पर हर 3 सप्ताह में 8 बार तक दिया जाता है।
- यदि आप उपचार के लिए अच्छी प्रतिक्रिया देते हैं, तो मैबथेरा आपको दो साल तक हर 2 से 3 महीने में रखरखाव उपचार के रूप में दिया जा सकता है। दवा के प्रति आपकी प्रतिक्रिया के आधार पर आपका डॉक्टर इसे बदल सकता है।
यदि इस दवा के उपयोग के बारे में आपके कोई और प्रश्न हैं, तो अपने डॉक्टर, फार्मासिस्ट या नर्स से पूछें।
मबथेरा के दुष्प्रभाव क्या हैं?
सभी दवाओं की तरह, यह दवा दुष्प्रभाव पैदा कर सकती है, हालांकि हर किसी को यह नहीं मिलता है।
अधिकांश दुष्प्रभाव हल्के या मध्यम होते हैं, लेकिन कुछ मामलों में वे गंभीर हो सकते हैं और उपचार की आवश्यकता होती है। शायद ही कभी, इनमें से कुछ प्रतिक्रियाएं घातक रही हों।
दवा के इंजेक्शन स्थल पर प्रतिक्रियाएं
कई रोगियों को मबथेरा के इंजेक्शन स्थल पर कुछ स्थानीय साइड इफेक्ट का अनुभव होता है। इनमें शामिल हैं: दर्द, सूजन, चोट लगना, रक्तस्राव, त्वचा का लाल होना, खुजली और दाने।
यदि ये प्रतिक्रियाएं गंभीर हैं तो आपका डॉक्टर मैबथेरा के साथ इलाज बंद करने का निर्णय ले सकता है।
संक्रमणों
अपने चिकित्सक को तुरंत बताएं यदि आपको संक्रमण के कोई भी लक्षण हैं, जिनमें शामिल हैं:
- बुखार, खांसी, गले में खराश, पेशाब करते समय जलन, बेहोशी या अस्वस्थ महसूस करना;
- स्मृति हानि, बिगड़ा हुआ सोच, चलने में कठिनाई या दृष्टि की हानि। यह एक बहुत ही दुर्लभ और गंभीर "मस्तिष्क संक्रमण के कारण हो सकता है जो घातक साबित हुआ है (प्रगतिशील मल्टीफोकल ल्यूकोएन्सेफालोपैथी या पीएमएल)।
मबथेरा से उपचार के दौरान आपको संक्रमण अधिक आसानी से हो सकता है। ये अक्सर सर्दी-जुकाम होते हैं, लेकिन निमोनिया या यूरिनरी ट्रैक्ट इन्फेक्शन के मामले सामने आए हैं। इन संक्रमणों को "अन्य दुष्प्रभाव" के तहत सूचीबद्ध किया गया है।
अन्य दुष्प्रभावों में शामिल हैं:
बहुत ही सामान्य दुष्प्रभाव (10 लोगों में 1 से अधिक को प्रभावित कर सकते हैं):
- जीवाणु संक्रमण या वायरल संक्रमण, ब्रोंकाइटिस
- सफेद रक्त कोशिकाओं की कम संख्या, बुखार के साथ या बिना, या रक्त प्लेटलेट्स
- अस्वस्थता (मतली)
- खोपड़ी पर गंजापन के क्षेत्र, ठंड लगना, सिरदर्द
- कम प्रतिरक्षा सुरक्षा - 'इम्युनोग्लोबुलिन' (IgG) नामक एंटीबॉडी के निम्न रक्त स्तर के कारण जो शरीर को संक्रमण से बचाने में मदद करते हैं।
सामान्य दुष्प्रभाव (10 में से 1 व्यक्ति को प्रभावित कर सकता है):
- रक्त संक्रमण (सेप्सिस), निमोनिया, दाद, सर्दी, ब्रोन्कियल ट्यूब संक्रमण, फंगल संक्रमण, अज्ञात मूल के संक्रमण, साइनस सूजन, हेपेटाइटिस बी
- लाल रक्त कोशिकाओं (एनीमिया) और सभी रक्त कोशिकाओं की कम संख्या
- एलर्जी प्रतिक्रियाएं (अतिसंवेदनशीलता)
- उच्च रक्त शर्करा, वजन घटना, चेहरे और शरीर की सूजन, रक्त में एलडीएच एंजाइम का बढ़ा हुआ स्तर, रक्त में कैल्शियम का निम्न स्तर
- त्वचा में असामान्य संवेदनाएं जैसे सुन्नता, झुनझुनी, चुभन, जलन, खिंचाव वाली त्वचा की भावना, स्पर्श की भावना में कमी
- बेचैनी की भावना, सोने में कठिनाई
- रक्त वाहिकाओं के फैलाव के परिणामस्वरूप चेहरे और त्वचा के अन्य क्षेत्रों की लाली
- चक्कर आना, घबराहट
- आंसू उत्पादन में वृद्धि, आंसू वाहिनी की समस्याएं, आंख की सूजन (नेत्रश्लेष्मलाशोथ)
- कानों में बजना, कानों में दर्द
- दिल की समस्याएं, जैसे दिल का दौरा, तेज या अनियमित दिल की धड़कन
- उच्च या निम्न रक्तचाप (विशेषकर खड़े होने पर रक्तचाप का कम होना)
- वायुमार्ग में मांसपेशियों में जकड़न के कारण घरघराहट (ब्रोंकोस्पज़म), सूजन, फेफड़ों, गले या साइनस में जलन, घरघराहट, नाक बहना
- उल्टी, दस्त, पेट दर्द, गले और मुंह में जलन या छाले, निगलने में कठिनाई, कब्ज, अपच
- भोजन के सेवन में कठिनाई, अपर्याप्त भोजन का सेवन जिसके परिणामस्वरूप वजन कम होता है
- पित्ती, पसीना बढ़ जाना, रात को पसीना आना
- मांसपेशियों की समस्याएं जैसे मांसपेशियों का अकड़ना, मांसपेशियों या जोड़ों में दर्द, पीठ और गर्दन में दर्द
- ट्यूमर दर्द
- थकान और अस्वस्थता की सामान्य भावना, कंपकंपी, फ्लू के लक्षण
- बहु-अंग विफलता।
असामान्य दुष्प्रभाव (100 लोगों में से 1 को प्रभावित कर सकते हैं):
- रक्त के थक्के जमने की समस्या, लाल रक्त कोशिकाओं के उत्पादन में कमी और लाल रक्त कोशिकाओं के विनाश में वृद्धि (अप्लास्टिक हेमोलिटिक एनीमिया), लिम्फ नोड्स की सूजन या वृद्धि
- कम मूड और सामान्य गतिविधियों में रुचि या खुशी की कमी, घबराहट
- आपके स्वाद की भावना के साथ समस्याएं, जैसे स्वाद में परिवर्तन
- हृदय की समस्याएं, जैसे हृदय गति कम होना या सीने में दर्द (एनजाइना)
- अस्थमा, शरीर के अंगों को ऑक्सीजन की अपर्याप्त आपूर्ति
- पेट में सूजन।
बहुत दुर्लभ दुष्प्रभाव (10,000 लोगों में से 1 को प्रभावित कर सकते हैं):
- रक्त में कुछ प्रकार के एंटीबॉडी में अस्थायी वृद्धि (इम्युनोग्लोबुलिन - आईजीएम कहा जाता है), मृत कैंसर कोशिकाओं के टूटने के कारण रक्त में रासायनिक परिवर्तन
- हाथ और पैर की नसों को नुकसान, चेहरे का पक्षाघात
- दिल की धड़कन रुकना
- रक्त वाहिकाओं की सूजन, जिनमें त्वचा के लक्षण पैदा करने वाले भी शामिल हैं
- सांस की विफलता
- गैस्ट्रोइंटेस्टाइनल दीवार को नुकसान (वेध)
- फफोले के साथ त्वचा की गंभीर समस्याएं जो घातक हो सकती हैं
- किडनी खराब।
- गंभीर दृष्टि हानि (कपाल तंत्रिका क्षति का संकेत)।
ज्ञात नहीं (जिस आवृत्ति के साथ ये दुष्प्रभाव हो सकते हैं वह ज्ञात नहीं है):
- सफेद रक्त कोशिकाओं में देरी से कमी
- जलसेक के तुरंत बाद प्लेटलेट्स की संख्या में कमी - प्रतिवर्ती है, लेकिन दुर्लभ मामलों में घातक हो सकती है
- सुनने की हानि, अन्य इंद्रियों की हानि।
मैबथेरा डॉक्टर द्वारा निर्धारित प्रयोगशाला परीक्षणों के परिणामों में भिन्नता भी पैदा कर सकता है।
यदि आप MabThera को अन्य दवाओं के साथ ले रहे हैं, तो कुछ दुष्प्रभाव अन्य दवाओं के कारण हो सकते हैं।
साइड इफेक्ट की रिपोर्टिंग
यदि आपको कोई साइड इफेक्ट मिलता है, तो अपने डॉक्टर, फार्मासिस्ट या नर्स से बात करें। इसमें कोई भी संभावित दुष्प्रभाव शामिल हैं जो इस पत्रक में सूचीबद्ध नहीं हैं। आप परिशिष्ट V में सूचीबद्ध राष्ट्रीय रिपोर्टिंग सिस्टम के माध्यम से सीधे साइड इफेक्ट की रिपोर्ट कर सकते हैं। साइड इफेक्ट्स जो आप मदद कर सकते हैं इस दवा की सुरक्षा के बारे में अधिक जानकारी प्रदान करें।
समाप्ति और अवधारण
इस दवा को बच्चों की नजर और पहुंच से दूर रखें।
एक्सप के बाद कार्टन पर बताई गई समाप्ति तिथि के बाद इस दवा का उपयोग न करें। समाप्ति तिथि उस महीने के अंतिम दिन को संदर्भित करती है।
एक रेफ्रिजरेटर (2 डिग्री सेल्सियस - 8 डिग्री सेल्सियस) में स्टोर करें। स्थिर नहीं रहो।
कंटेनर को प्रकाश से बचाने के लिए बाहरी कार्टन में रखें। अपशिष्ट जल या घरेलू कचरे के माध्यम से कोई भी दवा न फेंके। अपने फार्मासिस्ट से उन दवाओं को फेंकने के लिए कहें जिनका आप अब उपयोग नहीं करते हैं। इससे पर्यावरण की रक्षा करने में मदद मिलेगी।
MabThera 1400 mg में क्या होता है, चमड़े के नीचे इंजेक्शन के लिए समाधान
- सक्रिय संघटक रीतुसीमाब है। प्रत्येक शीशी में 1400 मिलीग्राम / 11.7 एमएल रीटक्सिमैब होता है। प्रत्येक मिलीलीटर में 120 मिलीग्राम रीटक्सिमैब होता है।
- अन्य अवयव पुनः संयोजक मानव हाइलूरोनिडेस (आरएचयूपीएच 20), एल-हिस्टिडाइन, एल-हिस्टिडाइन हाइड्रोक्लोराइड मोनोहाइड्रेट, α, α-ट्रेहलोज डाइहाइड्रेट, एल-मेथियोनीन, पॉलीसॉर्बेट 80, इंजेक्शन के लिए पानी हैं।
MabThera 1400 mg, चमड़े के नीचे इंजेक्शन के लिए समाधान कैसा दिखता है और पैक की सामग्री
MabThera एक रेडी-टू-यूज़, क्लियर टू ओपलेसेंट, रंगहीन से पीले रंग के तरल के रूप में आता है, जिसे क्लोजर पर एल्यूमीनियम के साथ ब्यूटाइल रबर स्टॉपर और एक प्लास्टिक डिस्क पिंक फ्लिप-ऑफ के साथ एक स्पष्ट कांच की शीशी में चमड़े के नीचे इंजेक्शन के लिए एक समाधान के रूप में आपूर्ति की जाती है। .
प्रत्येक शीशी में 1400 मिलीग्राम / 11.7 एमएल रीटक्सिमैब होता है। प्रत्येक पैक में एक शीशी होती है।
स्रोत पैकेज पत्रक: एआईएफए (इतालवी मेडिसिन एजेंसी)।सामग्री जनवरी 2016 में प्रकाशित हुई। हो सकता है कि मौजूद जानकारी अप-टू-डेट न हो।
सबसे अप-टू-डेट संस्करण तक पहुंचने के लिए, एआईएफए (इतालवी मेडिसिन एजेंसी) वेबसाइट तक पहुंचने की सलाह दी जाती है। अस्वीकरण और उपयोगी जानकारी।
01.0 औषधीय उत्पाद का नाम
मबठेरा १४०० एमजी सॉल्यूशन फॉर सबक्यूटेनियस इंजेक्शन
02.0 गुणात्मक और मात्रात्मक संरचना
प्रत्येक मिलीलीटर में 120 मिलीग्राम रीटक्सिमैब होता है।
प्रत्येक शीशी में 1400 मिलीग्राम / 11.7 एमएल रीटक्सिमैब होता है।
रिटक्सिमैब आनुवंशिक इंजीनियरिंग तकनीकों द्वारा प्राप्त एक काइमेरिक माउस / मानव मोनोक्लोनल एंटीबॉडी है, जिसमें "ग्लाइकोसिलेटेड इम्युनोग्लोबुलिन शामिल है जो मानव मूल के निरंतर क्षेत्रों IgG1 के साथ और प्रकाश श्रृंखला के चर क्षेत्र अनुक्रमों और murine मूल की भारी श्रृंखला के साथ है। एल" एंटीबॉडी एक स्तनधारी कोशिका निलंबन संस्कृति (चीनी हम्सटर अंडाशय) का उपयोग करके उत्पादित किया जाता है और विशिष्ट वायरल निष्क्रियता और हटाने की प्रक्रियाओं सहित एफ़िन क्रोमैटोग्राफी और आयन एक्सचेंज द्वारा शुद्ध किया जाता है।
Excipients की पूरी सूची के लिए, खंड ६.१ देखें।
03.0 फार्मास्युटिकल फॉर्म
इंजेक्शन योग्य घोल।
स्पष्ट से ओपेलेसेंट, रंगहीन से पीले रंग का तरल।
04.0 नैदानिक सूचना
04.1 चिकित्सीय संकेत
MabThera उपचर्म सूत्रीकरण वयस्कों के लिए संकेत दिया गया है गैर-हॉजकिन के लिंफोमा (एनएचएल) का उपचार:
MabThera को कीमोथेरेपी के साथ संयोजन में चरण III-IV कूपिक लिंफोमा वाले पहले से अनुपचारित रोगियों के उपचार के लिए संकेत दिया गया है।
MabThera रखरखाव चिकित्सा को कूपिक लिंफोमा रोगियों के उपचार के लिए संकेत दिया जाता है जो प्रेरण चिकित्सा का जवाब दे रहे हैं।
MabThera को CHOP कीमोथेरेपी (साइक्लोफॉस्फेमाइड, डॉक्सोरूबिसिन, विन्क्रिस्टाइन, प्रेडनिसोलोन) के संयोजन में CD20 पॉजिटिव डिफ्यूज़ लार्ज बी-सेल नॉन-हॉजकिन्स लिंफोमा वाले रोगियों के उपचार के लिए संकेत दिया गया है।
०४.२ खुराक और प्रशासन की विधि
MabThera को एक अनुभवी स्वास्थ्य देखभाल पेशेवर की सावधानीपूर्वक देखरेख में और ऐसे वातावरण में प्रशासित किया जाना चाहिए जहाँ पुनर्जीवन उपकरण आसानी से उपलब्ध हो (खंड 4.4 देखें)।
एक एंटीपीयरेटिक दवा और एक एंटीहिस्टामाइन के साथ पूर्व-दवा, उदाहरण के लिए पेरासिटामोल और डिपेनहाइड्रामाइन, हमेशा MabThera के प्रत्येक प्रशासन से पहले प्रशासित किया जाना चाहिए।
यदि गैर-हॉजकिन के लिंफोमा के उपचार के लिए ग्लूकोकार्टिकोइड युक्त कीमोथेरेपी के संयोजन में MabThera नहीं दिया जाता है, तो ग्लूकोकार्टिकोइड्स के साथ पूर्व-दवा पर विचार किया जाना चाहिए।
मात्रा बनाने की विधि
वयस्क रोगियों के उपचार के लिए MabThera उपचर्म सूत्रीकरण की अनुशंसित खुराक रोगी के शरीर की सतह के क्षेत्र की परवाह किए बिना एक निश्चित खुराक चमड़े के नीचे इंजेक्शन के रूप में प्रशासित 1400 मिलीग्राम है।
MabThera के चमड़े के नीचे इंजेक्शन शुरू करने से पहले, सभी रोगियों को हमेशा MabThera की एक पूरी खुराक पहले से ही अंतःशिरा जलसेक के रूप में दी जानी चाहिए, MabThera अंतःशिरा सूत्रीकरण (खंड 4.4 देखें) का उपयोग करके।
इस घटना में कि रोगियों को अन्य फॉर्मूलेशन पर स्विच करने से पहले अंतःशिरा जलसेक द्वारा MabThera की पूरी खुराक के साथ इलाज नहीं किया जा सकता है, उन्हें MabThera इंट्रावेनस फॉर्मूलेशन के साथ बाद के उपचार पाठ्यक्रमों को जारी रखने की आवश्यकता होगी जब तक कि उन्हें सफलतापूर्वक पूरी खुराक अंतःशिरा में नहीं दी जाती।
इसलिए, MabThera उपचर्म सूत्रीकरण पर स्विच करना केवल दूसरे या बाद के उपचार चक्रों में ही हो सकता है।
यह सुनिश्चित करने के लिए दवा के लेबल पर जानकारी की जांच करना महत्वपूर्ण है कि रोगी को निर्धारित अनुसार सही फॉर्मूलेशन (अंतःशिरा या चमड़े के नीचे) प्रशासित किया जा रहा है।
MabThera उपचर्म सूत्रीकरण अंतःशिरा प्रशासन के लिए अभिप्रेत नहीं है और इसे केवल चमड़े के नीचे इंजेक्शन द्वारा प्रशासित किया जाना चाहिए।
कूपिक गैर-हॉजकिन का लिंफोमा
एसोसिएशन थेरेपी
कूपिक लिंफोमा के साथ पहले से अनुपचारित या रिलेप्स / अपवर्तक रोगियों के प्रेरण उपचार के लिए कीमोथेरेपी के संयोजन में मैबथेरा की अनुशंसित खुराक इस प्रकार है: मबथेरा इंट्रावेनस फॉर्मूलेशन के साथ पहला कोर्स 375 मिलीग्राम / एम 2 शरीर की सतह क्षेत्र, इसके बाद मेबथेरा उपकुशल फॉर्मूलेशन के साथ बाद के पाठ्यक्रम इंजेक्शन 8 चक्रों तक प्रति चक्र 1400 मिलीग्राम की एक निश्चित खुराक पर।
यदि लागू हो, तो कीमोथेरेपी के ग्लुकोकोर्तिकोइद घटक के प्रशासन के बाद, प्रत्येक कीमोथेरेपी चक्र के पहले दिन MabThera को प्रशासित किया जाना चाहिए।
रखरखाव चिकित्सा
• पहले अनुपचारित कूपिक लिंफोमा
मैबथेरा चमड़े के नीचे के फॉर्मूलेशन की अनुशंसित खुराक कूपिक लिंफोमा वाले पहले से अनुपचारित रोगियों के लिए रखरखाव उपचार के रूप में उपयोग की जाती है, जिन्होंने प्रेरण उपचार का जवाब दिया है:
1400 मिलीग्राम हर 2 महीने में एक बार (प्रेरण चिकित्सा की अंतिम खुराक के 2 महीने बाद) रोग बढ़ने तक या दो साल तक।
• अपवर्तित / दुर्दम्य कूपिक लिंफोमा
MabThera सबक्यूटेनियस फॉर्मूलेशन की अनुशंसित खुराक का उपयोग रिलैप्स / रिफ्रैक्टरी फॉलिक्युलर लिम्फोमा रोगियों के लिए रखरखाव उपचार के रूप में किया जाता है, जिन्होंने प्रेरण उपचार का जवाब दिया है:
1400 मिलीग्राम हर 3 महीने में एक बार (प्रेरण चिकित्सा की अंतिम खुराक के 3 महीने बाद शुरू) रोग बढ़ने तक या दो साल तक।
डिफ्यूज़ लार्ज बी-सेल नॉन-हॉजकिन्स लिंफोमा
MabThera का उपयोग CHOP कीमोथेरेपी के संयोजन में किया जाना चाहिए। अनुशंसित खुराक इस प्रकार है: पहला चक्र, MabThera अंतःशिरा सूत्रीकरण 375 mg / m2 शरीर की सतह क्षेत्र, इसके बाद MabThera उपचर्म सूत्रीकरण के साथ बाद के पाठ्यक्रम 1400 मिलीग्राम प्रति चक्र की निश्चित खुराक पर इंजेक्ट किए जाते हैं। कुल: 8 चक्र।
CHOP कीमोथेरेपी के ग्लुकोकोर्तिकोइद घटक के अंतःशिरा जलसेक के बाद प्रत्येक कीमोथेरेपी चक्र के पहले दिन MabThera को प्रशासित किया जाता है।
मैबथेरा की सुरक्षा और प्रभावकारिता को बड़े बी सेल गैर-हॉजकिन के लिंफोमा को फैलाने में अन्य कीमोथेरपी के साथ संयोजन में स्थापित नहीं किया गया है।
उपचार के दौरान खुराक समायोजन
मैबथेरा की कोई खुराक कम करने की सिफारिश नहीं की जाती है। जब मैबथेरा को कीमोथेरेपी के साथ दिया जाता है, तो कीमोथेराप्यूटिक दवाओं के लिए मानक खुराक में कमी लागू होनी चाहिए (देखें खंड 4.8 )।
विशेष आबादी
बाल चिकित्सा जनसंख्या
18 वर्ष से कम उम्र के बच्चों में मबथेरा की सुरक्षा और प्रभावकारिता स्थापित नहीं की गई है। कोई डेटा उपलब्ध नहीं है।
वरिष्ठ नागरिकों
बुजुर्ग रोगियों (> 65 वर्ष) में कोई खुराक समायोजन की आवश्यकता नहीं है।
प्रशासन का तरीका
चमड़े के नीचे इंजेक्शन:
MabThera उपचर्म सूत्रीकरण केवल लगभग 5 मिनट में चमड़े के नीचे इंजेक्शन द्वारा प्रशासित किया जाना चाहिए। हाइपोडर्मिक इंजेक्शन सुई को सुई के संभावित अवरोध से बचने के लिए प्रशासन से तुरंत पहले सिरिंज से जोड़ा जाना चाहिए।
MabThera चमड़े के नीचे के फॉर्मूलेशन को पेट की दीवार में चमड़े के नीचे इंजेक्ट किया जाना चाहिए, हमेशा उन क्षेत्रों से बचना चाहिए जहां त्वचा लाल, खरोंच, दर्दनाक या सख्त हो या जहां तिल या निशान हों।
चूंकि शरीर में अन्य साइटों पर उनके प्रशासन के संबंध में कोई डेटा उपलब्ध नहीं है, इसलिए इंजेक्शन पेट की दीवार तक ही सीमित होना चाहिए।
MabThera उपचर्म सूत्रीकरण के साथ उपचार के दौरान, अन्य दवाओं का उपचर्म प्रशासन अधिमानतः अन्य साइटों पर किया जाना चाहिए।
यदि इंजेक्शन बंद कर दिया जाता है, तो इसे उसी साइट पर फिर से शुरू किया जा सकता है या यदि आवश्यक हो, तो एक अलग साइट का उपयोग किया जा सकता है।
अंतःशिरा जलसेक द्वारा प्रशासन:
खुराक के निर्देशों और प्रशासन की विधि के बारे में जानकारी के लिए, कृपया जलसेक के समाधान के लिए मैबथेरा 100 मिलीग्राम और 500 मिलीग्राम ध्यान केंद्रित उत्पाद विशेषताओं का सारांश (एसएमपीसी) देखें।
04.3 मतभेद
सक्रिय पदार्थ या माउस प्रोटीन के लिए अतिसंवेदनशीलता, हाइलूरोनिडेस या धारा 6.1 में सूचीबद्ध किसी भी अन्य excipients के लिए।
सक्रिय, गंभीर संक्रमण (देखें खंड 4.4)।
गंभीर रूप से प्रतिरक्षित अवस्था में रोगी।
04.4 उपयोग के लिए विशेष चेतावनी और उचित सावधानियां
जैविक औषधीय उत्पादों की ट्रेसबिलिटी में सुधार करने के लिए, प्रशासित उत्पाद का व्यापार नाम रोगी के मेडिकल रिकॉर्ड में स्पष्ट रूप से दर्ज (या घोषित) होना चाहिए।
धारा ४.४ में दी गई जानकारी अनुमोदित संकेत में MabThera उपचर्म सूत्रीकरण के उपयोग से संबंधित है गैर-हॉजकिन का लिंफोमा उपचार. अन्य संकेतों के बारे में जानकारी के लिए, कृपया MabThera इंट्रावेनस फॉर्मूलेशन के SmPC को देखें।
चरण III-IV कूपिक लिंफोमा वाले रोगियों के लिए जो कि केमोरेसिस्टेंट हैं या कीमोथेरेपी के बाद अपने दूसरे या बाद के पतन में हैं, अकेले MabThera उपचर्म सूत्रीकरण के उपयोग की अनुशंसा नहीं की जाती है क्योंकि एक बार साप्ताहिक उपचर्म प्रशासन की सुरक्षा स्थापित नहीं की गई है।
प्रगतिशील मल्टीफोकल ल्यूकोएन्सेफालोपैथी
मैबथेरा का उपयोग प्रगतिशील मल्टीफोकल ल्यूकोएन्सेफालोपैथी (पीएमएल) के बढ़ते जोखिम से जुड़ा हो सकता है। किसी भी नए या बिगड़ते न्यूरोलॉजिकल लक्षणों या संकेतों के लिए मरीजों की नियमित अंतराल पर निगरानी की जानी चाहिए जो पीएमएल के संकेतक हो सकते हैं। यदि संदेह है। पीएमएल, आगे की खुराक होनी चाहिए जब तक पीएमएल से इंकार नहीं किया जाता है तब तक निलंबित कर दिया गया है। चिकित्सक को यह निर्धारित करने के लिए रोगी का मूल्यांकन करना चाहिए कि क्या लक्षण न्यूरोलॉजिकल डिसफंक्शन के संकेत हैं और यदि ऐसा है, तो यदि ये लक्षण पीएमएल के संकेतक हो सकते हैं। यदि चिकित्सकीय रूप से संकेत दिया जाए तो न्यूरोलॉजिकल परामर्श आवश्यक है।
यदि संदेह है, तो आगे के मूल्यांकन पर विचार किया जाना चाहिए, जिसमें एमआरआई अधिमानतः इसके विपरीत, जेसी वायरस डीएनए का पता लगाने के लिए मस्तिष्कमेरु द्रव (सीएसएफ) परीक्षा, और बार-बार न्यूरोलॉजिकल मूल्यांकन शामिल हैं।
चिकित्सकों को विशेष रूप से पीएमएल के लक्षणों के प्रति सतर्क रहना चाहिए जो रोगी को नोटिस नहीं कर सकते हैं (उदाहरण के लिए, संज्ञानात्मक, तंत्रिका संबंधी, या मानसिक लक्षण)। रोगी को अपने साथी या देखभाल करने वाले को उपचार के बारे में सूचित करने की भी सलाह दी जानी चाहिए, क्योंकि वे ऐसे लक्षण देख सकते हैं जिनसे रोगी अनजान है।
यदि कोई रोगी पीएमएल विकसित करता है, तो मैबथेरा का प्रशासन स्थायी रूप से बंद कर देना चाहिए।
पीएमएल के साथ इम्युनोकॉम्प्रोमाइज्ड रोगियों में प्रतिरक्षा प्रणाली के पुनर्गठन के बाद, स्थिरीकरण या सुधार पर ध्यान दिया जाता है। यह ज्ञात नहीं है कि पीएमएल का शीघ्र पता लगाने और मबथेरा थेरेपी को बंद करने से समान स्थिरीकरण या सुधार होगा।
प्रशासन / आसव से संबंधित प्रतिक्रियाएं
MabThera जलसेक / प्रशासन प्रतिक्रियाओं से जुड़ा हुआ है जो साइटोकिन्स और / या अन्य रासायनिक मध्यस्थों की रिहाई से संबंधित हो सकता है। साइटोकाइन रिलीज सिंड्रोम तीव्र अतिसंवेदनशीलता प्रतिक्रियाओं से चिकित्सकीय रूप से अप्रभेद्य हो सकता है।
साइटोकाइन रिलीज सिंड्रोम, ट्यूमर लसीस सिंड्रोम और एनाफिलेक्टिक / अतिसंवेदनशीलता प्रकार की प्रतिक्रियाओं सहित प्रतिक्रियाओं का यह सेट नीचे वर्णित है। ये प्रतिक्रियाएं विशेष रूप से मबथेरा के प्रशासन के मार्ग से संबंधित नहीं हैं और दोनों योगों के साथ देखी जा सकती हैं।
MabThera के पहले IV इन्फ्यूजन को शुरू करने के 30 मिनट से 2 घंटे तक के समय के साथ MabThera इंट्रावेनस फॉर्मूलेशन के पोस्ट-मार्केटिंग उपयोग के दौरान घातक परिणाम के साथ गंभीर जलसेक प्रतिक्रियाओं की सूचना दी गई है। इन प्रतिक्रियाओं को फुफ्फुसीय घटनाओं की विशेषता है और कुछ मामलों में तेजी से ट्यूमर लसीका और ट्यूमर लसीका सिंड्रोम के लक्षण, साथ ही बुखार, ठंड लगना, कंपकंपी, हाइपोटेंशन, पित्ती, एंजियोएडेमा और अन्य लक्षण शामिल हैं (देखें खंड 4.8 )।
गंभीर साइटोकिन रिलीज सिंड्रोम गंभीर डिस्पेनिया की विशेषता है, अक्सर ब्रोन्कोस्पास्म और हाइपोक्सिया के साथ-साथ बुखार, ठंड लगना, कंपकंपी, पित्ती और एंजियोएडेमा। यह सिंड्रोम ट्यूमर लाइसिस सिंड्रोम की कुछ विशेषताओं से जुड़ा हो सकता है, जैसे कि हाइपरयूरिसीमिया, हाइपरकेलेमिया, हाइपोकैल्सीमिया, हाइपरफॉस्फेटेमिया, तीव्र गुर्दे की विफलता, ऊंचा लैक्टेट डिहाइड्रोजनेज (एलडीएच) एकाग्रता, और तीव्र श्वसन विफलता और मृत्यु से जुड़ा हो सकता है। तीव्र श्वसन विफलता के साथ फुफ्फुसीय अंतरालीय घुसपैठ या फुफ्फुसीय एडिमा जैसी घटनाएं हो सकती हैं, जो छाती के एक्स-रे पर दिखाई देती हैं। सिंड्रोम अक्सर पहला जलसेक शुरू करने के एक से दो घंटे के भीतर होता है। फुफ्फुसीय अपर्याप्तता या फेफड़ों के ट्यूमर घुसपैठ के इतिहास वाले मरीजों को प्रतिकूल परिणामों का खतरा बढ़ सकता है और उन्हें अधिक सावधानी के साथ इलाज किया जाना चाहिए। गंभीर साइटोकिन रिलीज सिंड्रोम विकसित करने वाले रोगियों में, जलसेक तुरंत बंद कर दिया जाना चाहिए (धारा 4.2 देखें) और आक्रामक रोगसूचक उपचार दिया जाना चाहिए। चूंकि नैदानिक लक्षणों में प्रारंभिक सुधार के बाद बिगड़ना हो सकता है, इन रोगियों की निगरानी की जानी चाहिए। समाधान या बहिष्करण तक सावधानी से निगरानी की जानी चाहिए। ट्यूमर लाइसिस सिंड्रोम और फुफ्फुसीय घुसपैठ। लक्षणों और संकेतों के पूर्ण समाधान के बाद रोगियों के आगे के उपचार से शायद ही कभी गंभीर साइटोकिन रिलीज सिंड्रोम की पुनरावृत्ति हुई हो।
उच्च ट्यूमर बोझ वाले रोगियों या परिसंचारी नियोप्लास्टिक कोशिकाओं की उच्च संख्या (≥ 25 x 109 / एल) के साथ, जो विशेष रूप से गंभीर साइटोकिन रिलीज सिंड्रोम के बढ़ते जोखिम में हो सकते हैं, अत्यधिक सावधानी के साथ इलाज किया जाना चाहिए। पहले जलसेक के दौरान इन रोगियों की बहुत बारीकी से निगरानी की जानी चाहिए। इन रोगियों में पहले जलसेक के लिए कम जलसेक दर या पहले चक्र के दौरान दो दिनों में विभाजित खुराक का उपयोग करने पर विचार किया जाना चाहिए और प्रत्येक बाद के चक्र में यदि लिम्फोसाइट गिनती अभी भी है> 25 x 109 / एल।
प्रोटीन के अंतःशिरा प्रशासन के बाद रोगियों में एनाफिलेक्टिक और अन्य अतिसंवेदनशीलता प्रतिक्रियाओं की सूचना मिली है। साइटोकिन रिलीज सिंड्रोम के विपरीत, सच्ची अतिसंवेदनशीलता प्रतिक्रियाएं आमतौर पर जलसेक शुरू करने के कुछ मिनटों के भीतर होती हैं। MabThera के प्रशासन के दौरान एलर्जी की प्रतिक्रिया के मामले में, अतिसंवेदनशीलता प्रतिक्रियाओं के उपचार के लिए दवाएं, उदा। एपिनेफ्रीन (एड्रेनालाईन), एंटीहिस्टामाइन और ग्लुकोकोर्टिकोइड्स तत्काल उपयोग के लिए उपलब्ध होना चाहिए। एनाफिलेक्सिस की नैदानिक अभिव्यक्तियाँ साइटोकाइन रिलीज सिंड्रोम (ऊपर वर्णित) के नैदानिक अभिव्यक्तियों के समान दिखाई दे सकती हैं। अतिसंवेदनशीलता के लिए जिम्मेदार प्रतिक्रियाओं को साइटोकाइन रिलीज के लिए जिम्मेदार लोगों की तुलना में कम बार रिपोर्ट किया गया है।
कुछ मामलों में रिपोर्ट की गई अतिरिक्त प्रतिक्रियाएं रोधगलन, अलिंद फिब्रिलेशन, फुफ्फुसीय एडिमा और तीव्र प्रतिवर्ती थ्रोम्बोसाइटोपेनिया थीं।
MabThera के प्रशासन के दौरान हाइपोटेंशन हो सकता है, इसलिए MabThera जलसेक से 12 घंटे पहले एंटीहाइपरटेन्सिव दवाओं को बंद करने पर विचार किया जाना चाहिए।
किसी भी प्रकार के जलसेक के लिए प्रतिकूल प्रतिक्रिया (साइटोकिन रिलीज सिंड्रोम सहित हाइपोटेंशन और 10% रोगियों में ब्रोन्कोस्पास्म सहित) 77% रोगियों में देखा गया है जिनका इलाज MabThera अंतःशिरा सूत्रीकरण के साथ किया गया है, खंड 4.8 देखें। ये लक्षण आम तौर पर प्रतिवर्ती होते हैं। MabThera जलसेक और एंटीपीयरेटिक दवाओं, एंटीहिस्टामाइन और, कभी-कभी, ऑक्सीजन, अंतःशिरा खारा या ब्रोन्कोडायलेटर दवाओं और यदि आवश्यक हो तो ग्लुकोकोर्टिकोइड्स का प्रशासन। गंभीर प्रतिक्रियाओं के लिए साइटोकाइन रिलीज सिंड्रोम पर वर्णित देखें।
नैदानिक अध्ययनों में, MabThera उपचर्म सूत्रीकरण के साथ इलाज किए गए 50% से अधिक रोगियों में प्रशासन से संबंधित प्रतिक्रियाएं देखी गईं। चमड़े के नीचे इंजेक्शन के 24 घंटों के भीतर होने वाली प्रतिक्रियाएं मुख्य रूप से एरिथेमा, प्रुरिटस, दाने और इंजेक्शन साइट प्रतिक्रियाएं जैसे दर्द, सूजन और लाली थीं और आम तौर पर हल्के या मध्यम तीव्रता (ग्रेड 1 या 2) और एक क्षणिक प्रकृति की थीं।
मबथेरा एससी के इलाज वाले मरीजों में स्थानीय त्वचा प्रतिक्रियाएं बहुत आम थीं। नैदानिक परीक्षणों में। लक्षणों में दर्द, सूजन, दर्द, रक्तस्राव, एरिथेमा, प्रुरिटस और दाने शामिल हैं (धारा 4.8 देखें)। मबथेरा एससी के प्रशासन के 24 घंटे से अधिक समय बाद कुछ स्थानीय त्वचा प्रतिक्रियाएं हुईं। MabThera उपचर्म सूत्रीकरण के प्रशासन के बाद देखी गई अधिकांश स्थानीय त्वचा प्रतिक्रियाएं हल्की या मध्यम तीव्रता की थीं और विशिष्ट उपचार के बिना हल हो गईं।
MabThera के चमड़े के नीचे के इंजेक्शन शुरू करने से पहले, सभी रोगियों को हमेशा MabThera की एक पूरी खुराक पहले से ही अंतःशिरा जलसेक के रूप में दी जानी चाहिए, MabThera अंतःशिरा सूत्रीकरण का उपयोग करके। आमतौर पर, प्रशासन से संबंधित प्रतिक्रिया विकसित होने का सबसे अधिक जोखिम चक्र एक में देखा गया था। MabThera के अंतःशिरा जलसेक के साथ चिकित्सा शुरू करने से अंतःशिरा जलसेक को धीमा या रोककर प्रशासन के लिए प्रतिक्रियाओं के बेहतर प्रबंधन की अनुमति मिलेगी।
इस घटना में कि रोगियों को अन्य फॉर्मूलेशन पर स्विच करने से पहले अंतःशिरा जलसेक द्वारा MabThera की पूरी खुराक के साथ इलाज नहीं किया जा सकता है, उन्हें MabThera अंतःशिरा फॉर्मूलेशन के साथ बाद के उपचार पाठ्यक्रमों को जारी रखने की आवश्यकता होगी जब तक कि उन्हें सफलतापूर्वक पूर्ण खुराक नहीं दी जाती है। MabThera उपचर्म सूत्रीकरण पर स्विच केवल दूसरे या बाद के उपचार चक्रों में हो सकता है।
इंट्रावेनस फॉर्मूलेशन की तरह, MabThera सबक्यूटेनियस फॉर्मूलेशन को ऐसे वातावरण में प्रशासित किया जाना चाहिए जिसमें तत्काल पुनर्जीवन उपकरण उपलब्ध हों और एक अनुभवी स्वास्थ्य देखभाल पेशेवर की सावधानीपूर्वक निगरानी में। एक एंटीपीयरेटिक / एनाल्जेसिक दवा और एक एंटीहिस्टामाइन के साथ प्रीमेडिकेशन हमेशा MabThera की प्रत्येक खुराक से पहले प्रशासित किया जाना चाहिए। उपचर्म सूत्रीकरण ग्लूकोकार्टिकोइड्स के साथ पूर्व-दवा पर भी विचार किया जाना चाहिए।
मबथेरा के चमड़े के नीचे के प्रशासन के बाद, रोगियों को कम से कम 15 मिनट तक देखा जाना चाहिए। अतिसंवेदनशीलता प्रतिक्रियाओं के जोखिम वाले रोगियों में एक लंबी अवलोकन अवधि उपयुक्त हो सकती है।
मरीजों को सलाह दी जानी चाहिए कि यदि वे दवा लेने के बाद किसी भी समय गंभीर अतिसंवेदनशीलता या साइटोकाइन रिलीज सिंड्रोम के लक्षण विकसित करते हैं तो उन्हें तुरंत अपने उपचार चिकित्सक से संपर्क करना चाहिए।
कार्डिएक पैथोलॉजी
MabThera के साथ इलाज किए गए रोगियों में एनजाइना पेक्टोरिस, कार्डियक अतालता जैसे आलिंद स्पंदन और फाइब्रिलेशन, दिल की विफलता और / या मायोकार्डियल रोधगलन के मामले सामने आए हैं। इसलिए हृदय रोग और / या कार्डियोटॉक्सिक कीमोथेरेपी के इतिहास वाले रोगियों की सावधानीपूर्वक निगरानी की जानी चाहिए।
हेमटोलॉजिकल विषाक्तता
हालांकि मैबथेरा अपने आप में मायलोस्प्रेसिव नहीं है, लेकिन ऑटोलॉगस बोन मैरो प्लेटलेट न्यूट्रोफिल और अन्य जोखिम समूहों वाले रोगियों के उपचार पर विचार करते समय विशेष देखभाल की जानी चाहिए, जो कि मायलोटॉक्सिसिटी को प्रेरित किए बिना संभावित रूप से बिगड़ा हुआ अस्थि मज्जा समारोह है।
मबथेरा थेरेपी के दौरान न्यूट्रोफिल और प्लेटलेट काउंट सहित पूर्ण रक्त गणना नियमित रूप से की जानी चाहिए।
संक्रमणों
MabThera के साथ उपचार के दौरान गंभीर, यहां तक कि घातक संक्रमण भी हो सकता है (देखें खंड 4.8 )। MabThera का उपयोग गंभीर सक्रिय संक्रमण वाले रोगियों में नहीं किया जाना चाहिए (जैसे तपेदिक, सेप्सिस और अवसरवादी संक्रमण, खंड 4.3 देखें)।
आवर्तक या पुराने संक्रमण के इतिहास या अंतर्निहित स्थितियों के साथ रोगियों में मैबथेरा के उपयोग पर विचार करते समय चिकित्सकों को सतर्क रहना चाहिए जो रोगियों को गंभीर संक्रमण के लिए आगे बढ़ा सकते हैं (देखें खंड 4.8 )।
घातक फुलमिनेंट हेपेटाइटिस की रिपोर्ट सहित MabThera अंतःशिरा सूत्रीकरण प्राप्त करने वाले रोगियों में हेपेटाइटिस बी पुनर्सक्रियन के मामले सामने आए हैं। इनमें से अधिकांश रोगी साइटोटोक्सिक कीमोथेरेपी के संपर्क में भी थे। मबथेरा के साथ उपचार शुरू करने से पहले सभी रोगियों में हेपेटाइटिस बी वायरस (एचबीवी) के लिए स्क्रीनिंग की जानी चाहिए और कम से कम एचबीएसएजी और एचबीसीएबी परीक्षण शामिल होना चाहिए। इन परीक्षणों को स्थानीय दिशानिर्देशों के अनुसार अन्य उपयुक्त मार्करों के साथ पूरक किया जा सकता है। सक्रिय हेपेटाइटिस बी संक्रमण वाले मरीजों का इलाज मैबथेरा से नहीं किया जाना चाहिए। सकारात्मक हेपेटाइटिस बी सीरोलॉजी (HBsAg और HBcAb दोनों) वाले मरीजों का मूल्यांकन एक हेपेटोलॉजिस्ट चिकित्सक द्वारा किया जाना चाहिए और हेपेटाइटिस बी पुनर्सक्रियन को रोकने के लिए स्थानीय नैदानिक मानकों के अनुसार निगरानी और पालन किया जाना चाहिए।
NHL में MabThera के पोस्ट-मार्केटिंग उपयोग के दौरान PML के बहुत दुर्लभ मामले सामने आए हैं (देखें खंड 4.8)। अधिकांश रोगियों को कीमोथेरेपी के साथ संयोजन में या हेमटोपोइएटिक स्टेम सेल प्रत्यारोपण कार्यक्रम के भाग के रूप में रीतुसीमाब प्राप्त हुआ था।
प्रतिरक्षा
MabThera थेरेपी के बाद लाइव वायरल टीकों के साथ टीकाकरण की सुरक्षा का NHL रोगियों के लिए अध्ययन नहीं किया गया है और लाइव वायरस टीकों के साथ टीकाकरण की सिफारिश नहीं की जाती है। MabThera के साथ इलाज किए गए मरीजों को गैर-जीवित वायरस टीकाकरण प्राप्त हो सकता है। हालांकि, गैर-जीवित वायरस टीकों की प्रतिक्रिया दर घटाया जा सकता है।एक गैर-यादृच्छिक अध्ययन में, स्वस्थ स्वयंसेवकों के अनुपचारित नियंत्रण की तुलना में मोनोथेरेपी के रूप में MabThera अंतःशिरा सूत्रीकरण प्राप्त करने वाले निम्न-श्रेणी के एनएचएल वाले रोगियों में टेटनस बूस्टर एंटीजन (81% की तुलना में 16%) और कीहोल के साथ टीकाकरण की प्रतिक्रिया दर कम थी। लिम्पेट हेमोसायनिन (केएलएच) नियोएंटीजेंस (4% बनाम 69% जब मूल्यांकन किया जाता है> एंटीबॉडी टिटर में 2 गुना वृद्धि)।
एक एंटीजन पैनल के खिलाफ पूर्व-चिकित्सीय एंटीबॉडी टाइटर्स का मतलब (स्ट्रैपटोकोकस निमोनिया, इन्फ्लूएंजा ए, कण्ठमाला, रूबेला, चिकन पॉक्स) को मबथेरा के उपचार के बाद कम से कम 6 महीने तक बनाए रखा गया था।
त्वचा की प्रतिक्रियाएं
गंभीर त्वचा प्रतिक्रियाएं जैसे कि विषाक्त एपिडर्मल नेक्रोलिसिस (लियेल सिंड्रोम) और स्टीवंस-जॉनसन सिंड्रोम, कुछ घातक परिणाम के साथ सूचित किया गया है (धारा 4.8 देखें)। ऐसी घटनाओं के मामले में, मैबथेरा के उपयोग से संबंधित, उपचार को स्थायी रूप से बंद कर देना चाहिए।
04.5 अन्य औषधीय उत्पादों और अन्य प्रकार की बातचीत के साथ बातचीत
MabThera के साथ संभावित ड्रग इंटरैक्शन पर वर्तमान में सीमित डेटा है।
MabThera के साथ सह-प्रशासन का Fludarabine या cyclophosphamide के फार्माकोकाइनेटिक्स पर कोई प्रभाव नहीं पड़ता है। इसके अलावा, MabThera के फार्माकोकाइनेटिक्स पर Fludarabine और cyclophosphamide का कोई स्पष्ट प्रभाव नहीं है।
संधिशोथ के रोगियों में मेथोट्रेक्सेट के साथ सह-प्रशासन का MabThera के फार्माकोकाइनेटिक्स पर कोई प्रभाव नहीं पड़ा।
जिन रोगियों ने एंटी-माउस या एंटी-काइमेरिक एंटीबॉडी (HAMA / HACA) विकसित किया है, उन्हें अन्य नैदानिक या चिकित्सीय मोनोक्लोनल एंटीबॉडी के साथ इलाज करने पर एलर्जी या अतिसंवेदनशीलता प्रतिक्रियाएं हो सकती हैं।
04.6 गर्भावस्था और स्तनपान
पुरुष और महिला गर्भनिरोधक
चूंकि बी-सेल की कमी वाले रोगियों में रीटक्सिमैब का लंबे समय तक प्रतिधारण समय होता है, इसलिए प्रसव क्षमता वाली महिलाओं को उपचार के दौरान और मबथेरा उपचार के बाद 12 महीने तक प्रभावी गर्भनिरोधक विधियों का उपयोग करना चाहिए।
गर्भावस्था
IgG इम्युनोग्लोबुलिन को प्लेसेंटल बाधा को पार करने के लिए जाना जाता है।
MabThera के मातृ संपर्क के बाद मानव शिशुओं में बी सेल के स्तर का नैदानिक परीक्षणों में मूल्यांकन नहीं किया गया है। गर्भवती महिलाओं में अध्ययन से कोई पर्याप्त और अच्छी तरह से नियंत्रित डेटा नहीं है, हालांकि गर्भावस्था के दौरान MabThera के संपर्क में आने वाली माताओं से पैदा हुए शिशुओं में क्षणिक बी-सेल की कमी और लिम्फोसाइटोपेनिया की सूचना मिली है। जानवरों के अध्ययन में इसी तरह के प्रभाव देखे गए हैं (खंड 5.3 देखें)। इस कारण से गर्भवती महिलाओं को MabThera नहीं दिया जाना चाहिए, जब तक कि संभावित लाभ संभावित जोखिम से अधिक न हो।
खाने का समय
यह ज्ञात नहीं है कि मानव दूध में रीतुसीमाब उत्सर्जित होता है या नहीं। हालाँकि, क्योंकि मातृ आईजीजी मानव दूध में उत्सर्जित होता है और स्तनपान कराने वाले बंदरों के दूध में रीतुसीमाब का पता चला था, महिलाओं को मबथेरा के साथ उपचार के दौरान और मबथेरा के उपचार के बाद 12 महीने तक स्तनपान नहीं कराना चाहिए।
उपजाऊपन
पशु अध्ययनों ने प्रजनन अंगों पर रीटक्सिमैब या पुनः संयोजक मानव हाइलूरोनिडेस (आरएचयूपीएच 20) के किसी भी हानिकारक प्रभाव को प्रकट नहीं किया।
04.7 मशीनों को चलाने और उपयोग करने की क्षमता पर प्रभाव
मशीनों को चलाने और उपयोग करने की क्षमता पर MabThera के प्रभावों पर कोई अध्ययन नहीं किया गया है, हालांकि औषधीय गतिविधि और आज तक बताई गई प्रतिकूल प्रतिक्रियाओं से पता चलता है कि MabThera का वाहन चलाने या मशीनरी चलाने की क्षमता पर कोई या नगण्य प्रभाव नहीं है।
04.8 अवांछित प्रभाव
इस पैराग्राफ में दी गई जानकारी ऑन्कोलॉजी में मबथेरा के उपयोग से संबंधित है।
स्व-प्रतिरक्षित संकेतों के बारे में जानकारी के लिए, MabThera अंतःशिरा सूत्रीकरण के SmPC को देखें।
सुरक्षा प्रोफ़ाइल का सारांश
नैदानिक विकास कार्यक्रम के दौरान, स्थानीय त्वचा प्रतिक्रियाओं के अपवाद के साथ, MabThera उपचर्म सूत्रीकरण की सुरक्षा प्रोफ़ाइल अंतःस्रावी सूत्रीकरण की तुलना में थी।
इंजेक्शन साइट प्रतिक्रियाओं सहित स्थानीय त्वचा प्रतिक्रियाएं MabThera उपकुशल फॉर्मूलेशन के इलाज वाले मरीजों में बहुत आम थीं। चरण III के अध्ययन में सबरीन (बीओ२२३३४) स्थानीय त्वचा प्रतिक्रियाओं की रिपोर्ट मैबथेरा उपचर्म सूत्रीकरण के साथ इलाज किए गए २०% से अधिक रोगियों में की गई थी। MabThera सबक्यूटेनियस फॉर्मूलेशन आर्म में सबसे आम स्थानीय त्वचा प्रतिक्रियाएं इंजेक्शन साइट एरिथेमा (13%), इंजेक्शन साइट दर्द (7%), इंजेक्शन साइट एडिमा (4%) थीं। चमड़े के नीचे के प्रशासन के बाद देखी गई घटनाएं हल्की या मध्यम थीं, एक मरीज के अपवाद के साथ, जिसने माबथेरा उपचर्म सूत्रीकरण (साइकिल 2) के पहले प्रशासन के बाद ग्रेड 3 स्थानीय त्वचा प्रतिक्रिया (इंजेक्शन साइट रैश) की सूचना दी थी। MabThera उपचर्म सूत्रीकरण हाथ पहले उपचर्म प्रशासन चक्र (चक्र 2) के दौरान अधिक बार होता था, उसके बाद दूसरा चक्र होता था, और बाद के इंजेक्शन के साथ घटना घट जाती थी।
MabThera उपचर्म सूत्रीकरण के उपयोग में रिपोर्ट की गई प्रतिकूल प्रतिक्रियाएं
MabThera उपचर्म सूत्रीकरण के प्रशासन से संबंधित तीव्र प्रतिक्रियाओं के जोखिम का मूल्यांकन प्रेरण और रखरखाव चरण (SABRINE BO22334) और अकेले रखरखाव चरण (SparkThera BP22333) के दौरान कूपिक लिंफोमा वाले रोगियों में किए गए दो ओपन-लेबल नैदानिक अध्ययनों में किया गया था। अध्ययन में सबरीना गंभीर प्रशासन से संबंधित प्रतिक्रियाएं (ग्रेड ≥3) दो रोगियों (2%) में MabThera उपकुशल फॉर्मूलेशन के प्रशासन के बाद रिपोर्ट की गई थी। ये घटनाएँ इंजेक्शन साइट रैश और ग्रेड 3 ड्राई माउथ थीं।
स्पार्कथेरा अध्ययन में प्रशासन से संबंधित कोई गंभीर प्रतिक्रिया नहीं मिली।
MabThera अंतःशिरा सूत्रीकरण के उपयोग में रिपोर्ट की गई प्रतिकूल प्रतिक्रियाएं
गैर-हॉजकिन के लिंफोमा और पुरानी लिम्फोसाइटिक ल्यूकेमिया में अनुभव
गैर-हॉजकिन के लिंफोमा और क्रोनिक लिम्फोसाइटिक ल्यूकेमिया में MabThera की समग्र सुरक्षा प्रोफ़ाइल नैदानिक परीक्षणों और पोस्ट-मार्केटिंग निगरानी में रोगियों के डेटा पर आधारित है। इन रोगियों को MabThera के साथ मोनोथेरेपी (प्रेरण उपचार के रूप में या पोस्ट-इंडक्शन रखरखाव उपचार के रूप में) या कीमोथेरेपी के संयोजन में इलाज किया गया था।
MabThera प्राप्त करने वाले रोगियों में सबसे अधिक बार देखी जाने वाली प्रतिकूल दवा प्रतिक्रियाएं (ADRs) जलसेक प्रतिक्रियाएं थीं, जो पहले जलसेक के दौरान अधिकांश रोगियों में हुई थीं। जलसेक से संबंधित लक्षणों की घटना बाद के जलसेक के साथ काफी कम हो जाती है और आठ खुराक के बाद 1% से कम होती है मबथेरा का।
नैदानिक परीक्षणों में इलाज किए गए एनएचएल रोगियों के लगभग 30-55% और नैदानिक परीक्षणों में इलाज किए गए सीएलएल रोगियों के 30-50% में संक्रामक घटनाएं (मुख्य रूप से बैक्टीरिया और वायरल) हुईं।
सबसे अधिक बार रिपोर्ट की गई या देखी गई गंभीर प्रतिकूल दवा प्रतिक्रियाएं थीं:
• आसव प्रतिक्रियाएं (साइटोकिन रिलीज सिंड्रोम और ट्यूमर लाइसिस सिंड्रोम सहित, खंड 4.4 देखें)।
• संक्रमण (देखें खंड 4.4)।
• हृदय संबंधी विकार (देखें खंड 4.4)।
रिपोर्ट किए गए अन्य गंभीर एडीआर में हेपेटाइटिस बी पुनर्सक्रियन और पीएमएल शामिल हैं (देखें खंड 4.4)।
अकेले MabThera के साथ या कीमोथेरेपी के संयोजन में रिपोर्ट की गई ADRs की आवृत्तियों को तालिका 1 में संक्षेपित किया गया है। प्रत्येक आवृत्ति वर्ग के भीतर, घटती गंभीरता के क्रम में अवांछनीय प्रभाव प्रस्तुत किए जाते हैं। आवृत्ति को बहुत सामान्य (≥ 1 / 10) के रूप में परिभाषित किया जाता है, सामान्य ( 1 / 100,
एडीआर केवल पोस्ट-मार्केटिंग निगरानी के दौरान पहचाने जाते हैं और जिनके लिए आवृत्ति का अनुमान नहीं लगाया जा सकता है उन्हें आवृत्ति "ज्ञात नहीं" के तहत सूचीबद्ध किया जाता है।
तालिका के रूप में प्रतिकूल प्रतिक्रियाओं की सूची
तालिका 1 नैदानिक परीक्षणों में या NHL और CLL रोगियों में पोस्ट-मार्केटिंग निगरानी के दौरान MabThera के साथ मोनोथेरेपी / रखरखाव या कीमोथेरेपी के साथ संयोजन में रिपोर्ट की गई ADRs
नैदानिक परीक्षणों के दौरान निम्नलिखित शर्तों को प्रतिकूल घटनाओं के रूप में सूचित किया गया था, हालांकि, उन्हें "नियंत्रण हथियारों की तुलना में माबथेरा हथियारों में समान या कम घटना के साथ रिपोर्ट किया गया था: हेमेटोलॉजिकल विषाक्तता, न्यूट्रोपेनिक संक्रमण, मूत्र पथ संक्रमण, संवेदी गड़बड़ी, पायरेक्सिया।
MabThera इंट्रावेनस फॉर्मूलेशन के साथ नैदानिक अध्ययन में 50% से अधिक रोगियों में एक जलसेक प्रतिक्रिया के संकेत और लक्षण बताए गए हैं और मुख्य रूप से पहले जलसेक के दौरान, आमतौर पर पहले दो घंटों में देखे गए थे। इन लक्षणों में मुख्य रूप से बुखार, ठंड लगना और शामिल थे। कंपकंपी। अन्य लक्षणों में निस्तब्धता, एंजियोएडेमा, ब्रोन्कोस्पास्म, उल्टी, मतली, पित्ती / दाने, अस्टेनिया, सिरदर्द, गले में जलन, राइनाइटिस, प्रुरिटस, दर्द, टैचीकार्डिया, उच्च रक्तचाप, हाइपोटेंशन, डिस्पेनिया, अपच, अस्थमा और ट्यूमर के लक्षण शामिल हैं। गंभीर। 12% मामलों में जलसेक प्रतिक्रियाएं (जैसे ब्रोंकोस्पज़म, हाइपोटेंशन) हुई। कुछ मामलों में रिपोर्ट की गई अतिरिक्त प्रतिक्रियाएं रोधगलन, अलिंद फिब्रिलेशन, फुफ्फुसीय एडिमा और तीव्र प्रतिवर्ती थ्रोम्बोसाइटोपेनिया थीं। एनजाइना पेक्टोरिस या कंजेस्टिव हार्ट फेल्योर या गंभीर हृदय विकार (दिल की विफलता, मायोकार्डियल इंफार्क्शन, एट्रियल फाइब्रिलेशन), पल्मोनरी एडिमा, मल्टी-ऑर्गन फेल्योर, ट्यूमर लाइसिस सिंड्रोम, साइटोकाइन रिलीज सिंड्रोम, रीनल फेल्योर और रेस्पिरेटरी जैसी पहले से मौजूद हृदय स्थितियों का तेज होना कम या अज्ञात आवृत्ति के साथ विफलता की सूचना दी गई है। जलसेक संबंधी लक्षणों की घटनाओं में बाद में अंतःशिरा संक्रमण के साथ काफी कमी आई है और है
प्रतिकूल प्रतिक्रियाओं के चयन का विवरण
संक्रमणों
MabThera लगभग 70-80% रोगियों में बी सेल की कमी को प्रेरित करता है, लेकिन यह घटना केवल कुछ ही रोगियों में सीरम इम्युनोग्लोबुलिन में कमी के साथ जुड़ी हुई है।
स्थानीयकृत कैंडिडा के साथ-साथ हरपीज ज़ोस्टर संक्रमणों को "यादृच्छिक अध्ययनों में MabThera बांह में उच्च घटनाओं की सूचना दी गई थी। MabThera मोनोथेरेपी के साथ इलाज किए गए लगभग 4% रोगियों में गंभीर संक्रमण की सूचना मिली थी। सभी संक्रमणों की उच्च आवृत्ति। संक्रमण, ग्रेड 3 या सहित 4 संक्रमण, अवलोकन की तुलना में 2 साल तक MabThera के साथ रखरखाव उपचार के दौरान देखे गए हैं। 2 साल की उपचार अवधि में रिपोर्ट किए गए संक्रमणों के संदर्भ में कोई संचयी विषाक्तता नहीं थी। इसके अलावा, MabThera के साथ उपचार के दौरान अन्य गंभीर वायरल संक्रमण, दोनों नए, सक्रिय या तेज, रिपोर्ट किए गए हैं, जिनमें से कुछ घातक रहे हैं। अधिकांश रोगियों को केमोथेरेपी के साथ संयोजन में या हेमेटोपोएटिक स्टेम सेल प्रत्यारोपण के हिस्से के रूप में मैबथेरा प्राप्त हुआ। इन गंभीर वायरल संक्रमणों के उदाहरण हर्पीस वायरस (साइटोमेगालोवायरस, वैरिसेला ज़ोस्टर वायरस और हर्पीस सिम्प्लेक्स), जेसी वायरस (पीएमएल) और हेपेटाइटिस सी वायरस के कारण होने वाले संक्रमण हैं। नैदानिक परीक्षणों के दौरान घातक परिणाम वाले पीएमएल के मामले भी सामने आए हैं, जो बाद में हुए थे। रोग की प्रगति और पीछे हटना। हेपेटाइटिस बी के पुनर्सक्रियन के मामले सामने आए हैं, जिनमें से अधिकांश उन विषयों में हुए हैं जिन्होंने साइटोटोक्सिक कीमोथेरेपी के संयोजन में मैबथेरा प्राप्त किया था। कापोसी के सरकोमा की प्रगति देखी गई है। मबथेरा-उजागर रोगियों में पहले से मौजूद कपोसी के सरकोमा के साथ। अस्वीकृत संकेतों में मामले सामने आए और अधिकांश मरीज एचआईवी पॉजिटिव थे।
हेमटोलॉजिकल प्रतिकूल प्रतिक्रियाएं
MabThera को 4 सप्ताह के लिए प्रशासित मोनोथेरेपी के रूप में नैदानिक परीक्षणों में, रोगियों के एक अल्पसंख्यक में हेमेटोलॉजिकल असामान्यताएं हुईं और आमतौर पर हल्के और प्रतिवर्ती थे। 4.2% रोगियों में गंभीर (ग्रेड 3/4) न्यूट्रोपेनिया, 1.1% में एनीमिया और 1.7% में थ्रोम्बोसाइटोपेनिया की सूचना मिली थी। MabThera के साथ 2 साल तक रखरखाव उपचार के दौरान, ल्यूकोपेनिया (5% बनाम 2%, ग्रेड 3/4) और न्यूट्रोपेनिया (10% बनाम 4%, ग्रेड 3/4) "अवलोकन की तुलना में उच्च घटना" पर रिपोर्ट किया गया था। थ्रोम्बोसाइटोपेनिया की घटना कम थी (
हृदय संबंधी प्रतिकूल प्रतिक्रियाएं
अकेले MabThera के साथ नैदानिक परीक्षणों में, हाइपोटेंशन और उच्च रक्तचाप वाले 18.8% रोगियों में हृदय संबंधी प्रतिक्रियाएं सबसे अधिक बार रिपोर्ट की गई घटनाओं के रूप में बताई गई थीं। जलसेक के दौरान ग्रेड 3 या 4 अतालता (वेंट्रिकुलर और सुप्रावेंट्रिकुलर टैचीकार्डिया सहित) और एनजाइना पेक्टोरिस के मामले सामने आए हैं। रखरखाव उपचार के दौरान, ग्रेड 3/4 हृदय संबंधी विकारों की घटना उपचारित रोगियों के बीच तुलनीय थी। MabThera और अवलोकन के साथ। हृदय संबंधी घटनाएँ ग्रेड 3 और 4 कार्डियक अतालता की तुलना में MabThera के साथ इलाज किए गए 3% रोगियों में गंभीर प्रतिकूल घटनाओं (अलिंद फिब्रिलेशन, मायोकार्डियल रोधगलन, बाएं वेंट्रिकुलर विफलता और मायोकार्डियल इस्किमिया सहित) के रूप में रिपोर्ट किया गया था, विशेष रूप से सुप्रावेंट्रिकुलर अतालता जैसे टैचीकार्डिया और अलिंद स्पंदन / फाइब्रिलेशन था। CHOP समूह (3 रोगियों, 1.5%) की तुलना में R-CHOP समूह (14 रोगियों, 6.9%) में उच्च। MabThera जलसेक के संदर्भ में हुआ या बुखार, संक्रमण, तीव्र मायोकार्डियल जैसी पूर्व-स्थितियों से जुड़ा हुआ है रोधगलन, या पूर्व-श्वसन और हृदय रोग मौजूदा। अन्य ग्रेड 3 और 4 हृदय संबंधी घटनाओं की घटनाओं के संदर्भ में R-CHOP और CHOP समूहों के बीच कोई अंतर नहीं देखा गया, जिसमें हृदय की विफलता, मायोकार्डियल रोग और कोरोनरी धमनी रोग की अभिव्यक्तियाँ शामिल हैं।
श्वसन प्रणाली
बीचवाला फेफड़ों की बीमारी के मामले, कुछ घातक परिणाम के साथ रिपोर्ट किए गए हैं।
मस्तिष्क संबंधी विकार
उपचार की अवधि के दौरान (आठ चक्र तक आर-चॉप सहित प्रेरण उपचार चरण), आर-चॉप के साथ इलाज किए गए चार रोगियों (2%), सभी हृदय जोखिम वाले कारकों के साथ, उपचार के पहले कोर्स के दौरान अनुभवी सेरेब्रोवास्कुलर थ्रोम्बोम्बोलिक दुर्घटनाएं। अन्य थ्रोम्बोम्बोलिक घटनाओं की घटनाओं के संदर्भ में उपचार समूहों के बीच कोई अंतर नहीं था। इसके विपरीत, तीन रोगियों (1.5%) ने CHOP समूह में सेरेब्रोवास्कुलर घटनाओं का अनुभव किया, जो सभी अनुवर्ती अवधि के दौरान हुए। -अप।
पोस्टीरियर रिवर्सिबल एन्सेफैलोपैथी सिंड्रोम (PRES) / पोस्टीरियर रिवर्सिबल ल्यूकोएन्सेफालोपैथी सिंड्रोम (RPLS) के मामले सामने आए हैं। संकेतों और लक्षणों में दृश्य गड़बड़ी, सिरदर्द, दौरे और मानसिक स्थिति में परिवर्तन, संबद्ध उच्च रक्तचाप के साथ या बिना शामिल थे। PRES / RPLS के निदान के लिए मस्तिष्क इमेजिंग के साथ पुष्टि की आवश्यकता होती है। रिपोर्ट किए गए मामलों में PRES / RPLS के लिए जोखिम वाले कारकों की पहचान की गई थी, जिसमें रोगी की सहवर्ती बीमारी की स्थिति, उच्च रक्तचाप, इम्यूनोसप्रेसिव थेरेपी और / या कीमोथेरेपी शामिल है।
जठरांत्रिय विकार
गैर-हॉजकिन के लिंफोमा के उपचार के लिए मैबथेरा प्राप्त करने वाले रोगियों में कुछ मामलों में गैस्ट्रोइंटेस्टाइनल वेध देखा गया है। इनमें से ज्यादातर मामलों में, MabThera को कीमोथेरेपी के साथ प्रशासित किया गया था।
आईजीजी स्तर
नैदानिक अध्ययन में, रिलैप्स / रिफ्रैक्टरी फॉलिक्युलर लिंफोमा में रखरखाव उपचार में MabThera का मूल्यांकन करते हुए, माध्य IgG का स्तर सामान्य (LLN) की निचली सीमा से नीचे था (
त्वचा और चमड़े के नीचे के ऊतक विकार
विषाक्त एपिडर्मल नेक्रोलिसिस (लियेल सिंड्रोम) और स्टीवंस जॉनसन सिंड्रोम के मामले, कुछ घातक परिणाम के साथ, बहुत कम ही रिपोर्ट किए गए हैं।
रोगी उप-जनसंख्या - MabThera monotherapy
बुजुर्ग मरीज (≥ 65 वर्ष):
सभी ग्रेड और ग्रेड 3/4 एडीआर की घटना बुजुर्ग बनाम युवा रोगियों में समान थी (
भारी रोग:
"भारी बीमारी वाले रोगियों में ग्रेड 3/4 एडीआर की उच्च घटनाएं भारी बीमारी वाले रोगियों की तुलना में (25.6% बनाम 15.4%) थीं। सभी ग्रेड एडीआर की घटनाएं इन दो समूहों में समान थीं।
पीछे हटना:
MabThera के आगे के पाठ्यक्रमों के साथ वापसी के दौरान ADRs की रिपोर्ट करने वाले रोगियों का अनुपात प्रारंभिक प्रदर्शन (सभी ग्रेड और ग्रेड 3/4 ADRs) के दौरान ADRs की रिपोर्ट करने वाले रोगियों के अनुपात के समान था।
संदिग्ध प्रतिकूल प्रतिक्रियाओं की रिपोर्टिंग
औषधीय उत्पाद के प्राधिकरण के बाद होने वाली संदिग्ध प्रतिकूल प्रतिक्रियाओं की रिपोर्ट करना महत्वपूर्ण है क्योंकि यह औषधीय उत्पाद के लाभ / जोखिम संतुलन की निरंतर निगरानी की अनुमति देता है। स्वास्थ्य पेशेवरों को राष्ट्रीय रिपोर्टिंग प्रणाली के माध्यम से किसी भी संदिग्ध प्रतिकूल प्रतिक्रिया की रिपोर्ट करने के लिए कहा जाता है। "पता http: //www.agenziafarmaco.gov.it/it/responsabili।
04.9 ओवरडोज
स्वीकृत खुराक से अधिक MabThera अंतःशिरा सूत्रीकरण की खुराक के साथ मानव नैदानिक परीक्षणों से सीमित अनुभव है। मनुष्यों में अब तक परीक्षण किए गए मबथेरा की उच्चतम अंतःशिरा खुराक 5000 मिलीग्राम (2250 मिलीग्राम / एम 2) है, जिसे क्रोनिक लिम्फोसाइटिक ल्यूकेमिया वाले रोगियों में वृद्धिशील खुराक अध्ययन में परीक्षण किया गया है। कोई अतिरिक्त सुरक्षा संकेतों की पहचान नहीं की गई है।
ओवरडोज के लक्षणों का अनुभव करने वाले मरीजों को तुरंत जलसेक बंद कर देना चाहिए और सावधानीपूर्वक निगरानी की जानी चाहिए।
MabThera उपचर्म सूत्रीकरण के साथ किए गए नैदानिक अध्ययन SABRINA (BO22334) में, तीन रोगियों को गलती से बिना किसी प्रतिकूल प्रभाव के 2780 मिलीग्राम की अधिकतम खुराक तक रिट्क्सिमैब के उपचर्म सूत्रीकरण को अंतःशिरा रूप से प्रशासित किया गया था।
ओवरडोज के लक्षणों का अनुभव करने वाले या दवा की त्रुटि से पीड़ित मरीजों पर कड़ी निगरानी रखी जानी चाहिए।
पोस्ट मार्केटिंग के बाद मबथेरा ओवरडोज के पांच मामले सामने आए हैं। इनमें से तीन ने कोई प्रतिकूल घटना की सूचना नहीं दी। रिपोर्ट की गई दो प्रतिकूल घटनाएं फ्लू जैसे लक्षण थीं, जिसमें रिटक्सिमैब की 1.8 ग्राम खुराक और घातक परिणाम के साथ श्वसन विफलता, रीतुसीमाब की 2 ग्राम खुराक के साथ थी।
05.0 औषधीय गुण
05.1 फार्माकोडायनामिक गुण
भेषज समूह: एंटीनोप्लास्टिक एजेंट, मोनोक्लोनल एंटीबॉडी, एटीसी कोड: L01X C02
MabThera उपचर्म सूत्रीकरण में पुनः संयोजक मानव hyaluronidase (rHuPH20) होता है, एक एंजाइम जो सहवर्ती रूप से प्रशासित उपचर्म प्रशासित दवाओं के फैलाव और अवशोषण को बढ़ाने के लिए उपयोग किया जाता है।
Rituximab विशेष रूप से CD20 ट्रांसमेम्ब्रेन एंटीजन, एक गैर-ग्लाइकोसिलेटेड फॉस्फोप्रोटीन, जो प्री-बी लिम्फोसाइट्स और परिपक्व बी लिम्फोसाइटों पर पाया जाता है, से बांधता है। एंटीजन सभी बी-सेल गैर-हॉजकिन के लिम्फोमा के 95% पर व्यक्त किया जाता है।
CD20 सामान्य और नियोप्लास्टिक बी कोशिकाओं में पाया जाता है, लेकिन हेमटोपोइएटिक स्टेम सेल, प्रो-बी कोशिकाओं, सामान्य प्लाज्मा कोशिकाओं या अन्य सामान्य ऊतकों पर नहीं। एंटीबॉडी के लिए बाध्य होने पर एंटीजन को आंतरिक नहीं किया जाता है और कोशिका की सतह से जारी नहीं किया जाता है।CD20 एक मुक्त प्रतिजन के रूप में रक्त में प्रसारित नहीं होता है और इसलिए एंटीबॉडी बंधन के साथ प्रतिस्पर्धा नहीं करता है।
रीटक्सिमैब का फैब डोमेन बी लिम्फोसाइटों पर सीडी 20 एंटीजन से बांधता है और एफसी डोमेन बी सेल लसीस पैदा करने के उद्देश्य से प्रतिरक्षा प्रणाली के प्रभावकारी कार्यों को सक्रिय कर सकता है। प्रभावकारी-मध्यस्थता सेल लसीका के संभावित तंत्र में साइटोटोक्सिसिटी पूरक-निर्भर (सीडीसी) शामिल हैं ) C1q और एंटीबॉडी-निर्भर सेलुलर साइटोटोक्सिसिटी (ADCC) के लिए बाध्यकारी के माध्यम से ग्रैन्यूलोसाइट्स, मैक्रोफेज और NK कोशिकाओं की सतह पर एक या एक से अधिक Fcg रिसेप्टर्स द्वारा मध्यस्थता। बी लिम्फोसाइटों पर सीडी 20 एंटीजन के लिए रीटक्सिमैब को बांधना भी एपोप्टोसिस द्वारा कोशिका मृत्यु को प्रेरित करने के लिए दिखाया गया है।
मबथेरा की पहली खुराक के प्रशासन के बाद पेरिफेरल बी सेल की संख्या सामान्य से नीचे गिर गई। हेमेटोलॉजिकल कैंसर के लिए इलाज किए गए रोगियों में, बी-सेल रिकवरी उपचार के 6 महीने के भीतर शुरू हुई और आम तौर पर चिकित्सा के पूरा होने के बाद 12 महीनों के भीतर सामान्य स्तर पर लौट आई, हालांकि कुछ रोगियों में रिकवरी लंबी हो सकती है (23 महीने तक की वसूली के औसत के साथ) प्रेरण चिकित्सा के बाद)। रुमेटीइड गठिया के रोगियों में, परिधीय रक्त बी कोशिकाओं की तत्काल कमी देखी गई थी, प्रत्येक मेबथेरा के 1000 मिलीग्राम के दो जलसेक के बाद, 14 दिनों के अंतराल से अलग किया गया था। पेरिफेरल बी सेल की संख्या 24 सप्ताह से बढ़ने लगती है और अधिकांश रोगियों में 40 वें सप्ताह तक पुनर्संयोजन के लक्षण देखे जाते हैं, दोनों जब मैबथेरा को मोनोथेरेपी के रूप में दिया जाता है और जब मेथोट्रेक्सेट के साथ संयोजन में दिया जाता है।
गैर-हॉजकिन के लिंफोमा में MabThera उपचर्म सूत्रीकरण का नैदानिक अनुभव
गैर-हॉजकिन के लिंफोमा में MabThera उपचर्म सूत्रीकरण का नैदानिक अनुभव कूपिक लिंफोमा के रोगियों में चरण III अध्ययन (SABRINA BO22334) और कूपिक लिंफोमा वाले रोगियों पर आयोजित एक चरण Ib खुराक निर्धारण / पुष्टि अध्ययन (स्पार्कथेरा BP22333) से प्राप्त आंकड़ों पर आधारित है। .अध्ययन BP22333 के परिणाम खंड 5.2 में प्रस्तुत किए गए हैं।
अध्ययन बीओ२२३३४ (सबरीना)
फार्माकोकाइनेटिक प्रोफाइल की गैर-हीनता की जांच करने के साथ-साथ MabThera की प्रभावकारिता और सुरक्षा की जांच के लिए पहले से अनुपचारित कूपिक लिंफोमा वाले रोगियों में एक चरण III, दो-चरण, ओपन-लेबल, नियंत्रित, यादृच्छिक, बहुकेंद्र और अंतर्राष्ट्रीय नैदानिक अध्ययन किया गया था। CHOP या CVP रेजिमेन बनाम MabThera इंट्रावेनस फॉर्मूलेशन के साथ संयोजन में चमड़े के नीचे का फॉर्मूलेशन CHOP या CVP रेजिमेन के साथ संयोजन में।
पहले चरण का उद्देश्य रीटक्सिमैब एससी की खुराक का निर्धारण करना था जिसके परिणामस्वरूप मबथेरा इंट्रावेनस फॉर्मूलेशन की तुलना में मैबथेरा सबक्यूटेनियस फॉर्मूलेशन के सीरम सीट्रू स्तर थे, जब हर 3 सप्ताह में प्रेरण उपचार के हिस्से के रूप में प्रशासित किया जाता था (देखें खंड 5.2)। 1 पहले से अनुपचारित रोगी CD20 पॉजिटिव ग्रेड 1, 2 या 3a के साथ कूपिक लिंफोमा को नामांकित किया गया (n = 127)।
चरण 2 का लक्ष्य चरण 1 में परिभाषित 1400 मिलीग्राम की चमड़े के नीचे की खुराक का उपयोग करके अंतःशिरा रीटक्सिमैब की तुलना में माबथेरा उपचर्म सूत्रीकरण के उपयोग से संबंधित अतिरिक्त प्रभावकारिता और सुरक्षा डेटा प्रदान करना था। चरण 2 में, कूपिक लिंफोमा वाले रोगियों को नामांकित किया गया था। पहले अनुपचारित CD20 पॉजिटिव ग्रेड 1, 2, या 3a (n = 283)।
समग्र अध्ययन डिजाइन दोनों चरणों के लिए समान था और रोगियों को निम्नलिखित दो उपचार समूहों में यादृच्छिक किया गया था:
• MabThera उपचर्म सूत्रीकरण (n = 205): MabThera अंतःशिरा सूत्रीकरण का पहला चक्र प्लस CHOP या CVP कीमोथेरेपी के संयोजन में MabThera उपचर्म सूत्रीकरण के 7 चक्र, 8 चक्र तक, हर 3 सप्ताह में प्रशासित।
MabThera अंतःशिरा सूत्रीकरण का उपयोग शरीर की सतह क्षेत्र के 375 mg / m2 की मानक खुराक पर किया गया था।
MabThera उपचर्म सूत्रीकरण को 1400 मिलीग्राम की निश्चित खुराक पर प्रशासित किया गया था।
जिन रोगियों ने कम से कम आंशिक प्रतिक्रिया (पीआर) हासिल की, उन्हें मैबथेरा उपचर्म सूत्रीकरण के साथ रखरखाव चिकित्सा में शामिल किया गया, जिसे 24 महीने के लिए हर 8 सप्ताह में एक बार प्रशासित किया जाता है।
• MabThera अंतःशिरा सूत्रीकरण (n = 205): CHOP या CVP कीमोथेरेपी के संयोजन में MabThera अंतःशिरा सूत्रीकरण के 8 चक्र, 8 चक्र तक, हर 3 सप्ताह में प्रशासित।
MabThera अंतःशिरा सूत्रीकरण का उपयोग 375 mg / m2 की मानक खुराक पर किया गया था।
कम से कम एक पीआर हासिल करने वाले मरीजों को मबथेरा इंट्रावेनस फॉर्मूलेशन के साथ रखरखाव चिकित्सा में शामिल किया गया था, जिसे 24 महीने के लिए हर 8 सप्ताह में एक बार प्रशासित किया जाता था।
सबरीना अध्ययन के चरण 1 और 2 में 410 रोगियों के समग्र विश्लेषण में अनुमानित समग्र प्रतिक्रिया दर तालिका 2 में दिखाई गई है।
तालिका 2 सबरीना (BO22334) अनुमानित प्रतिक्रिया दर (जनसंख्या का इलाज करने का इरादा)
ओआरआर - समग्र प्रतिक्रिया दर
सीआरआर - पूर्ण प्रतिक्रिया दर
खोजपूर्ण विश्लेषण से पता चला कि बीएसए, कीमोथेरेपी और लिंग के लिए उपसमूह प्रतिक्रिया दर आईटीटी आबादी से काफी अलग नहीं थी।
प्रतिरक्षाजनकता
MabThera उपचर्म सूत्रीकरण के नैदानिक विकास कार्यक्रम से प्राप्त डेटा से संकेत मिलता है कि चमड़े के नीचे के प्रशासन के बाद एंटी-रिटक्सिमैब एंटीबॉडी (HACA) का गठन अंतःशिरा प्रशासन के बाद देखे गए के बराबर है। अध्ययन सबरीना (बीओ२२३३४) में एससी फॉर्मूलेशन उपचार समूह में उपचार-प्रेरित/बढ़ी हुई एंटी-रिटक्सिमैब एंटीबॉडी की घटना कम थी और iv उपचार समूह (२% बनाम १, क्रमशः) में देखी गई थी।%)। एंटी-आरएचयूपीएच20 एंटीबॉडीज की घटना ईव फॉर्मूलेशन के साथ उपचार समूह में 6% थी, जबकि एससी फॉर्मूलेशन के साथ उपचार समूह में 9% की तुलना में। और एंटी-आरएचयूपीएच 20 एंटीबॉडी के लिए सकारात्मक परीक्षण करने वाले रोगियों में से कोई भी एंटीबॉडी को निष्क्रिय करने के लिए सकारात्मक परीक्षण नहीं किया गया था।
एंटी-रिटक्सिमैब या एंटी-आरएचयूपीएच20 एंटीबॉडी की उपस्थिति का जाहिर तौर पर सुरक्षा या प्रभावकारिता पर कोई प्रभाव नहीं पड़ा।
जिन रोगियों में एंटी-आरएचयूपीएच 20 एंटीबॉडी पाए गए, उनका कुल प्रतिशत आम तौर पर दोनों समूहों में अनुवर्ती अवधि में स्थिर रहा। MabThera उपचर्म सूत्रीकरण के साथ उपचार के बाद HACA या एंटी-rHuPH20 एंटीबॉडी के विकास की नैदानिक प्रासंगिकता अज्ञात है।
एंटी-रिटक्सिमैब या एंटी-आरएचयूपीएच 20 एंटीबॉडी की उपस्थिति का स्पष्ट रूप से सुरक्षा या प्रभावकारिता [सबरीन] पर कोई प्रभाव नहीं पड़ा।
गैर-हॉजकिन के लिंफोमा में जलसेक के समाधान के लिए मैबथेरा का नैदानिक अनुभव
कूपिक लिंफोमा
प्रारंभिक उपचार, कीमोथेरेपी के संयोजन में
एक ओपन-लेबल, यादृच्छिक नैदानिक अध्ययन में, कूपिक लिंफोमा वाले कुल 322 पहले से अनुपचारित रोगियों को या तो सीवीपी कीमोथेरेपी (साइक्लोफॉस्फेमाइड 750 मिलीग्राम / एम 2, विन्क्रिस्टाइन 1.4 मिलीग्राम / एम 2 दिन 1 पर अधिकतम 2 मिलीग्राम तक और प्रेडनिसोलोन के लिए यादृच्छिक किया गया था। ४० मिलीग्राम / एम २ / दिन १-५) हर ३ सप्ताह में ८ चक्रों के लिए या मबथेरा ३७५ मिलीग्राम / एम २ सीवीपी (आर-सीवीपी) के साथ संयोजन में। MabThera को प्रत्येक उपचार चक्र के पहले दिन प्रशासित किया गया था। कुल ३२१ रोगियों (१६२ आर-सीवीपी, १५९ सीवीपी) ने चिकित्सा प्राप्त की और प्रभावकारिता के लिए उनका विश्लेषण किया गया। रोगियों का औसत अनुवर्ती ५३ महीने था। आर-सीवीपी के परिणामस्वरूप प्राथमिक समापन बिंदु, यानी समय के लिए सीवीपी पर एक महत्वपूर्ण लाभ हुआ। उपचार विफलता के लिए (27 महीने बनाम 6.6 महीने, पी
समग्र अस्तित्व के संबंध में उपचार समूहों के बीच अंतर ने एक महत्वपूर्ण नैदानिक अंतर दिखाया (पी = 0.029, केंद्र द्वारा स्तरीकृत लॉग-रैंक परीक्षण): आर-सीवीपी समूह में रोगियों के लिए 71.1% की तुलना में 53 महीने की जीवित रहने की दर 80.9% थी। सीवीपी समूह में।
गैर-सीवीपी कीमोथेरेपी रेजिमेंस (सीएचओपी, एमसीपी, सीएचवीपी / इंटरफेरॉन-α) के संयोजन में मैबथेरा का उपयोग करते हुए तीन अन्य यादृच्छिक परीक्षणों के परिणामों ने भी प्रतिक्रिया दर, समय-निर्भर मापदंडों और समग्र अस्तित्व में महत्वपूर्ण सुधार प्रदर्शित किए। । सभी चार अध्ययनों के सबसे महत्वपूर्ण परिणामों को तालिका 3 में संक्षेपित किया गया है।
तालिका 3 चार यादृच्छिक चरण III परीक्षणों से प्रमुख निष्कर्षों का सारांश, कूपिक लिंफोमा में विभिन्न कीमोथेरेपी के नियमों के साथ MabThera के लाभ का मूल्यांकन
ईएफएस - घटना मुक्त जीवन रक्षा।
टीटीपी - प्रगति या मृत्यु का समय। पीएफएस - प्रगति मुक्त जीवन रक्षा। टीटीएफ - उपचार की विफलता का समय। OS दरें - विश्लेषण के समय जीवित रहने की दर।
रखरखाव चिकित्सा
पहले अनुपचारित कूपिक लिंफोमा
एक संभावित, ओपन-लेबल, अंतर्राष्ट्रीय, बहुकेंद्र, चरण III के अध्ययन में, पहले से अनुपचारित उन्नत कूपिक लिंफोमा वाले 1193 रोगियों को R-CHOP (n = 881), R-CVP (n = 268) या R-FCM के साथ प्रेरण चिकित्सा प्राप्त हुई। n = ४४), अन्वेषक की पसंद के आधार पर। कुल १०७८ रोगियों ने प्रेरण चिकित्सा का जवाब दिया, जिनमें से १०१८ को मैबथेरा (एन = ५०५) या अवलोकन (एन = ५१३) के साथ रखरखाव चिकित्सा के लिए यादृच्छिक किया गया। दो उपचार समूह आधारभूत और रोग स्थिति रखरखाव की विशेषताओं के संबंध में अच्छी तरह से संतुलित थे। MabThera के साथ उपचार में MabThera का एक जलसेक शामिल था, जो रोग के बढ़ने तक या 2 साल तक हर 2 महीने में 375 mg / m2 शरीर की सतह क्षेत्र की खुराक पर प्रशासित होता है।
यादृच्छिकता से 25 महीने के औसत अवलोकन समय के बाद, मैबथेरा के साथ रखरखाव चिकित्सा ने लिम्फोमा के रोगियों में अवलोकन की तुलना में प्रगति-मुक्त अस्तित्व (पीएफएस) के जांचकर्ता-मूल्यांकन किए गए प्राथमिक अंतराल में नैदानिक रूप से प्रासंगिक और सांख्यिकीय रूप से महत्वपूर्ण सुधार किया। पहले इलाज न किए गए बालों के रोम (तालिका 4)।
MabThera रखरखाव उपचार से महत्वपूर्ण लाभ घटना-मुक्त अस्तित्व (EFS), अगले एंटी-लिम्फोमा उपचार (TNLT), अगली कीमोथेरेपी के लिए समय (TNCT) और समग्र प्रतिक्रिया दर जैसे माध्यमिक समापन बिंदुओं के लिए भी देखा गया था। (ORR) (तालिका) 4))। प्राथमिक विश्लेषण के परिणामों की लंबे समय तक अनुवर्ती (औसत अवलोकन समय: 48 महीने) के साथ पुष्टि की गई थी और 25 और 48 महीनों की अनुवर्ती अवधि के बीच तुलना को स्पष्ट करने के लिए तालिका 4 में जोड़ा गया था।
तालिका 4 रखरखाव चरण: MabThera प्रभावकारिता परिणामों का अवलोकन बनाम ४८ महीनों के मध्य अवलोकन समय के बाद अवलोकन (२५ महीनों के औसत अवलोकन समय के आधार पर प्राथमिक विश्लेषण परिणामों की तुलना में)
* रखरखाव / अवलोकन के अंत में; # ची-स्क्वेर्ड परीक्षणों से पी-मान।
कोष्ठक में मान 25 महीने (प्राथमिक विश्लेषण) के औसत अवलोकन समय के अनुरूप हैं। कोष्ठक के बाहर के मान 48 महीने (अद्यतन विश्लेषण) के औसत अवलोकन समय के अनुरूप हैं।
पीएफएस: प्रगति-मुक्त अस्तित्व; ईएफएस: घटना मुक्त अस्तित्व; ओएस: समग्र अस्तित्व; TNLT: अगले लिम्फोमा उपचार का समय; टीएनसीटी: अगले कीमोथेरेपी उपचार का समय; ओआरआर: समग्र प्रतिक्रिया दर: एनआर: नैदानिक कट-ऑफ के समय तक नहीं पहुंचा; या: अंतर अनुपात।
MabThera के साथ रखरखाव उपचार ने परीक्षण किए गए सभी पूर्वनिर्धारित उपसमूहों में लगातार लाभ प्रदान किया: लिंग (पुरुष, महिला), आयु (= 60 वर्ष), FLIPI स्कोर (= 3), इंडक्शन थेरेपी (R-CHOP, R-CVP या R-FCM) और प्रेरण चिकित्सा (सीआर, सीआरयू या पीआर) की प्रतिक्रिया की गुणवत्ता की परवाह किए बिना। रखरखाव उपचार के लाभ के खोजपूर्ण विश्लेषण ने बुजुर्ग रोगियों (> 70 वर्ष की आयु) में कम स्पष्ट प्रभाव दिखाया, हालांकि नमूना आकार छोटा था।
अपवर्तक / दुर्दम्य कूपिक लिंफोमा
एक संभावित, ओपन-लेबल, अंतर्राष्ट्रीय, बहुकेंद्र, चरण III के अध्ययन में, पहले चरण में CHOP (साइक्लोफॉस्फेमाइड, डॉक्सोरूबिसिन, विन्क्रिस्टाइन और प्रेडनिसोलोन; n = 231) के साथ इंडक्शन थेरेपी के लिए पहले चरण में रिलैप्स / रिफ्रैक्टरी फॉलिक्युलर लिंफोमा वाले 465 रोगियों को यादृच्छिक किया गया था। o MabThera प्लस चॉप (आर चॉप, एन = 234)। आधारभूत रोग विशेषताओं और स्थिति के संबंध में दो उपचार समूह अच्छी तरह से संतुलित थे। इंडक्शन थेरेपी के बाद पूर्ण या आंशिक छूट प्राप्त करने वाले कुल 334 रोगियों को MabThera रखरखाव चिकित्सा (n = 167) या अवलोकन (n = 167) के दूसरे चरण में यादृच्छिक किया गया। MabThera के साथ रखरखाव उपचार में 375 mg / m2 शरीर की सतह क्षेत्र में MabThera का एकल जलसेक शामिल था, जो हर 3 महीने में बीमारी के बढ़ने तक या दो साल तक दिया जाता था।
अंतिम प्रभावकारिता विश्लेषण में अध्ययन के दोनों हिस्सों में यादृच्छिक रूप से सभी रोगियों को शामिल किया गया था। प्रेरण चरण में यादृच्छिक रोगियों के लिए 31 महीने के औसत अवलोकन समय के बाद, आर-चॉप ने कूपिक लिम्फोमा वाले रोगियों के पूर्वानुमान में काफी सुधार किया। सीएचओपी के लिए रिलैप्स / अपवर्तक ( तालिका 5 देखें)।
तालिका 5 प्रेरण चरण: CHOP बनाम R-CHOP प्रभावकारिता परिणामों का अवलोकन (औसत अवलोकन समय 31 महीने)
1) अनुमानों की गणना खतरनाक अनुपातों के साथ की गई थी।
2) अन्वेषक द्वारा मूल्यांकन के अनुसार नवीनतम ट्यूमर प्रतिक्रिया। "प्रतिक्रिया" के लिए "प्राथमिक" सांख्यिकीय परीक्षण सीआर बनाम पीआर बनाम गैर-प्रतिक्रिया (पी) की प्रवृत्ति परीक्षण था
संकेताक्षर: लागू नहीं, उपलब्ध नहीं; ओआरआर: समग्र प्रतिक्रिया दर; सीआर: पूरा जवाब; पीआर: आंशिक प्रतिक्रिया।
अध्ययन के रखरखाव चरण के लिए यादृच्छिक रोगियों के लिए, औसत अवलोकन समय यादृच्छिकरण से रखरखाव तक 28 महीने था। MabThera के साथ रखरखाव उपचार के परिणामस्वरूप अकेले अवलोकन की तुलना में प्राथमिक समापन बिंदु, PFS (रैंडमाइज़ेशन से रखरखाव से लेकर विश्राम, रोग की प्रगति, या मृत्यु तक) में नैदानिक रूप से प्रासंगिक और सांख्यिकीय रूप से महत्वपूर्ण सुधार हुआ है (p
तालिका 6 रखरखाव चरण: MabThera प्रभावकारिता परिणामों का अवलोकन बनाम अवलोकन (28 महीने का औसत अवलोकन समय)
एनआर: नहीं पहुंचा; ए: केवल सीआर प्राप्त करने वाले रोगियों के लिए लागू।
इंडक्शन रेजिमेन (CHOP या R-CHOP) या इंडक्शन ट्रीटमेंट (CR या PR) (तालिका 6) की प्रतिक्रिया की गुणवत्ता की परवाह किए बिना विश्लेषण किए गए सभी उपसमूहों में MabThera रखरखाव उपचार के लाभ की पुष्टि की गई थी। MabThera रखरखाव उपचार ने CHOP (औसत PFS 37.5 महीने बनाम 11.6 महीने, p) के साथ प्रेरण चिकित्सा का जवाब देने वाले दोनों रोगियों में माध्य PFS को काफी लंबा कर दिया।
डिफ्यूज़ लार्ज बी-सेल नॉन-हॉजकिन्स लिंफोमा
एक यादृच्छिक, ओपन-लेबल अध्ययन में, कुल 399 पहले अनुपचारित बुजुर्ग रोगियों (60 से 80 वर्ष की आयु) को फैलाना बड़े बी-सेल लिंफोमा के साथ CHOP कीमोथेरेपी (साइक्लोफॉस्फेमाईड 750 मिलीग्राम / एम 2, डॉक्सोरूबिसिन 50 मिलीग्राम / एम 2) के मानक पाठ्यक्रम प्राप्त हुए। vincristine 1.4 mg / m2 से अधिकतम 2 mg 1 दिन पर दिया जाता है, और प्रेडनिसोलोन 40 mg / m2 / दिन 1-5) हर 3 सप्ताह में आठ चक्रों के लिए, या MabThera 375 mg / day m2 CHOP के सहयोग से दिया जाता है ( आर-चॉप)। MabThera को उपचार चक्र के पहले दिन प्रशासित किया गया था।
अंतिम प्रभावकारिता विश्लेषण में सभी यादृच्छिक रोगी (197 CHOP, 202 R-CHOP) शामिल थे और लगभग 31 महीनों की औसत अनुवर्ती अवधि थी। दो उपचार समूह विशेषताओं के संदर्भ में अच्छी तरह से संतुलित थे। और बेसलाइन पर रोग की स्थिति। अंतिम विश्लेषण ने पुष्टि की कि आर-चॉप उपचार घटना-मुक्त अस्तित्व की अवधि में नैदानिक रूप से प्रासंगिक और सांख्यिकीय रूप से महत्वपूर्ण सुधार से जुड़ा था (प्राथमिक प्रभावकारिता पैरामीटर; जहां घटनाएं मृत्यु, पुनरावृत्ति या लिम्फोमा की प्रगति, या नए एंटी-लिम्फोमा उपचार की शुरुआत थी। ) (पी = 0.0001)। घटना-मुक्त अस्तित्व की औसत अवधि का कपलान मेयर का अनुमान आर-चॉप शाखा में 35 महीने बनाम सीएचओपी शाखा में 13 महीने था, जो 41% की जोखिम में कमी का प्रतिनिधित्व करता है। 24 महीनों में, आर-चॉप आर्म में कुल जीवित रहने का अनुमान 68.2% था, जबकि सीएचओपी आर्म में 57.4% था। ६० महीने की औसत अनुवर्ती अवधि में किए गए समग्र उत्तरजीविता अवधि के बाद के विश्लेषण ने CHOP उपचार (p = ०.००७१) पर R-CHOP उपचार के लाभ की पुष्टि की, जो ३२% जोखिम में कमी का प्रतिनिधित्व करता है। ।
सभी माध्यमिक मापदंडों (प्रतिक्रिया दर, प्रगति-मुक्त अस्तित्व, रोग-मुक्त अस्तित्व, प्रतिक्रिया की अवधि) के विश्लेषण ने CHOP की तुलना में R-CHOP के साथ उपचार की प्रभावकारिता को सत्यापित किया। 8 चक्रों के बाद पूर्ण प्रतिक्रिया दर R-CHOP समूह में ७६.२% और CHOP समूह में ६२.४% (p = ०.००२८) थी। रोग बढ़ने का जोखिम 46% और पुनरावृत्ति का जोखिम 51% कम हो गया था।
सभी रोगी उपसमूहों में (लिंग, आयु, आयु-समायोजित आईपीआई, एन आर्बर चरण, ईसीओजी, β2-माइक्रोग्लोबुलिन, एलडीएच, एल्ब्यूमिन, बी लक्षण, भारी रोग, एक्सट्रानोडल साइट, अस्थि मज्जा भागीदारी), जोखिम अनुपात घटना-मुक्त अस्तित्व और समग्र उत्तरजीविता (R-CHOP बनाम CHOP) क्रमशः 0.83 और 0.95 से कम थी। R-CHOP आयु-समायोजित IPI के अनुसार उच्च और निम्न-जोखिम वाले दोनों रोगियों में बेहतर परिणाम से जुड़ा था।
नैदानिक प्रयोगशाला डेटा
माउस एंटी-प्रोटीन एंटीबॉडी परीक्षण (एचएएमए) से गुजरने वाले 67 रोगियों से कोई प्रतिक्रिया नहीं देखी गई। एचएसीए परीक्षण से गुजरने वाले 356 रोगियों में से 1.1% (4 रोगियों) ने सकारात्मक परीक्षण किया।
बाल चिकित्सा जनसंख्या
यूरोपीय मेडिसिन एजेंसी ने कूपिक लिंफोमा में बाल चिकित्सा आबादी के सभी सबसेट में MabThera के साथ अध्ययन के परिणाम प्रस्तुत करने के दायित्व को माफ कर दिया है। बाल चिकित्सा उपयोग के बारे में जानकारी के लिए खंड 4.2 देखें।
05.2 "फार्माकोकाइनेटिक गुण
अवशोषण
कूपिक लिंफोमा वाले रोगियों में, चमड़े के नीचे MabThera की एक खुराक के प्रशासन के बाद रीटक्सिमैब के फार्माकोकाइनेटिक्स। 375 mg/m2, 625 mg/m2 और 800 mg/m2 की तुलना अंतःशिरा MabThera से की गई। 375 मिलीग्राम / एम 2। चमड़े के नीचे के प्रशासन के बाद, रीटक्सिमैब धीमी अवशोषण प्रदर्शित करता है, प्रशासन के लगभग 3 दिनों के बाद अधिकतम सांद्रता तक पहुंचता है। जनसंख्या फार्माकोकाइनेटिक विश्लेषण से 71% की एक पूर्ण जैव उपलब्धता का अनुमान लगाया गया था। रिटक्सिमैब एक्सपोजर खुराक-आनुपातिक तरीके से 375 मिलीग्राम / एम 2 से 800 मिलीग्राम / एम 2 की खुराक सीमा से अधिक मात्रा में बढ़ गया। फार्माकोकाइनेटिक पैरामीटर, जैसे निकासी, वितरण की मात्रा और उन्मूलन आधा जीवन, दोनों योगों के लिए तुलनीय थे।
स्टूडियो बीपी२२३३३ (स्पार्कथेरा)
रखरखाव उपचार के हिस्से के रूप में कूपिक लिंफोमा वाले रोगियों में MabThera उपचर्म सूत्रीकरण की फार्माकोकाइनेटिक्स, सुरक्षा और सहनशीलता की जांच के लिए एक दो-चरण चरण Ib नैदानिक परीक्षण।
चरण 2 में, कूपिक लिंफोमा रोगियों, जो पहले प्रेरण चरण में MabThera अंतःशिरा निर्माण के लिए उत्तरदायी थे, MabThera अंतःशिरा निर्माण के कम से कम एक कोर्स के बाद, रखरखाव उपचार के दौरान चमड़े के नीचे इंजेक्शन द्वारा 1400 मिलीग्राम की एक निश्चित खुराक पर MabThera उपचर्म सूत्रीकरण दिया गया था।
तालिका 7 MabThera उपचर्म सूत्रीकरण और MabThera अंतःशिरा सूत्रीकरण के लिए अनुमानित माध्य Cmax के डेटा की तुलना को सारांशित करती है।
तालिका 7: अध्ययन BP22333 (स्पार्कथेरा): अवशोषण - MabThera sc के फार्माकोकाइनेटिक पैरामीटर। बनाम मबथेरा ई.वी.
MabThera उपचर्म सूत्रीकरण के लिए माध्य Tmax अंत में Tmax की तुलना में या अंतःस्राव निर्माण के लिए जलसेक के अंत की ओर लगभग 3 दिन था।
अध्ययन बीओ२२३३४ (सबरीना)
पहले इलाज न किए गए कूपिक लिंफोमा वाले रोगियों को कीमोथेरेपी के साथ संयोजन में MabThera अंतःशिरा सूत्रीकरण के पहले कोर्स के बाद, 3 सप्ताह के अंतराल पर प्रेरण चरण के दौरान 6 चक्रों के लिए 1400 मिलीग्राम की एक निश्चित खुराक पर MabThera उपचर्म सूत्रीकरण दिया गया था। चक्र ७ में, रीतुसीमाब सीरम सीमैक्स दो उपचार भुजाओं के बीच समान था, क्रमशः २५०.६३ एमसीजी / एमएल और २३६.८२ एमसीजी / एमएल के ज्यामितीय माध्य (सीवी%) मूल्यों के साथ अंतःशिरा (iv) फॉर्मूलेशन के लिए। और उपचर्म सूत्रीकरण ( sc), जिसके परिणामस्वरूप 0.941 (90% CI: 0.872, 1.015) का ज्यामितीय माध्य अनुपात (Cmax, sc / Cmax, iv) होता है।
वितरण / उन्मूलन
Ctrough का ज्यामितीय माध्य और नैदानिक अध्ययन BP22333 और BO22334 से प्राप्त AUC का ज्यामितीय माध्य तालिका 8 में संक्षेपित किया गया है।
तालिका 8: वितरण / उन्मूलन - चमड़े के नीचे MabThera बनाम अंतःशिरा MabThera . के फार्माकोकाइनेटिक पैरामीटर
मैबथेरा एससी के साथ इलाज किए गए कूपिक लिंफोमा वाले 403 रोगियों पर आयोजित "जनसंख्या फार्माकोकाइनेटिक विश्लेषण" में।और / या IV, अकेले MabThera के एकल या एकाधिक इन्फ्यूजन के साथ या कीमोथेरेपी के साथ संयोजन में, गैर-विशिष्ट निकासी (CL1), प्रारंभिक विशिष्ट निकासी (CL2) का अनुमान बी कोशिकाओं या ट्यूमर द्रव्यमान के संभावित योगदान के साथ, और केंद्रीय वितरण की कम्पार्टमेंट मात्रा (V1) क्रमशः 0.194 L / दिन, 0.535 L / दिन और 4.37 L / दिन थी। MabThera उपचर्म सूत्रीकरण का औसत अनुमानित टर्मिनल उन्मूलन आधा जीवन 29.7 दिनों के बराबर होता है (सीमा: 9.9 - 91.2 दिन) ) विश्लेषण के लिए सेट किए गए डेटा में ४०३ रोगियों से ६००३ मात्रात्मक नमूने शामिल थे, जिन्हें रीटक्सिमैब एससी प्रशासित किया गया था। और / या iv. नैदानिक अध्ययन में BP22333 (277 रोगियों से 3736 नमूने) और BO22334 (126 रोगियों से 2267 नमूने)। उनतीस (0.48%) खुराक के बाद के अवलोकन (सभी बीपी 22333 के अध्ययन से संबंधित) मात्रा का ठहराव की सीमा से नीचे थे। बेसलाइन बी सेल काउंट्स को छोड़कर कोई कोवरिएट्स लापता मान नहीं हैं। बेसलाइन ट्यूमर द्रव्यमान केवल अध्ययन BO22334 में उपलब्ध था।
विशेष आबादी
नैदानिक अध्ययन में बीओ२२३३४ शरीर की सतह क्षेत्र और चक्र ७ में रिपोर्ट की गई सांद्रता के अनुपात के बीच एक प्रभाव देखा गया था, जो कि हर ३ सप्ताह में रीटक्सिमैब १४०० मिलीग्राम के उपचर्म सूत्रीकरण के बीच और हर ३ सप्ताह में रीतुसीमाब ३७५ मिलीग्राम / एम २ के बीच के अनुपात के साथ होता है। निम्न, मध्यम और उच्च शरीर सतह क्षेत्र वाले रोगियों में क्रमशः २.२९, १.३१ और १.४१ के बराबर गर्त, (निम्न बीएसए १.७० एम२; १.७० एम२ २; उच्च बीएसए १.९० एम२)।
संबंधित एयूसी रिपोर्ट? 1.66, 1.17 और 1.32 के बराबर थे।
इस बात का कोई सबूत नहीं था कि रीटक्सिमैब के फार्माकोकाइनेटिक्स उम्र और लिंग के लिए चिकित्सकीय रूप से प्रासंगिक हैं।
केवल 13 रोगियों में रीटक्सिमैब के एंटीबॉडी का पता चला था और इसके परिणामस्वरूप स्थिर-राज्य निकासी में कोई नैदानिक रूप से प्रासंगिक वृद्धि नहीं हुई थी।
05.3 प्रीक्लिनिकल सुरक्षा डेटा
CD20 B सेल एंटीजन के लिए Rituximab अत्यधिक विशिष्ट पाया गया। Cynomolgus बंदर में विषाक्तता के अध्ययन से परिधीय रक्त और लिम्फ नोड ऊतक में B कोशिकाओं की अपेक्षित दवा की कमी के अलावा कोई प्रभाव नहीं पाया गया।
सिनोमोलगस बंदर में 100 मिलीग्राम / किग्रा (गर्भावस्था के दिनों में उपचार 20-50) तक की खुराक पर विकासवादी विषाक्तता अध्ययन किया गया है और यह दिखाया गया है कि रीटक्सिमैब के कारण भ्रूण विषाक्तता का कोई सबूत नहीं है। हालांकि, लिम्फोइड अंगों में, भ्रूण में बी कोशिकाओं की खुराक पर निर्भर दवा की कमी देखी गई, जिसे जन्म के बाद तक बनाए रखा गया था और प्रभावित नवजात जानवरों में आईजीजी के स्तर में कमी के साथ जुड़ा था। इन जानवरों में, बी सेल की संख्या सामान्य स्तर पर लौट आई। 6 के भीतर सामान्य मान जन्म के महीने और टीकाकरण प्रतिक्रियाओं को ख़राब नहीं किया।
उत्परिवर्तजनता के अध्ययन के लिए मानक परीक्षण नहीं किए गए हैं, क्योंकि ये अध्ययन इस अणु के लिए प्रासंगिक नहीं हैं। रीटक्सिमैब की कार्सिनोजेनिक क्षमता का आकलन करने के लिए दीर्घकालिक पशु अध्ययन नहीं किए गए हैं।
प्रजनन क्षमता पर रीतुसीमाब या rHuPH20 के प्रभावों को निर्धारित करने के लिए कोई विशेष अध्ययन नहीं किया गया है। सिनोमोलगस बंदर में किए गए सामान्य विषाक्तता अध्ययनों में, पुरुषों और महिलाओं में प्रजनन अंगों पर कोई प्रतिकूल प्रभाव नहीं देखा गया। इसके अलावा, rHuPH20 के लिए शुक्राणु की गुणवत्ता पर कोई प्रभाव नहीं पाया गया।
माउस भ्रूण-भ्रूण विकास अध्ययनों में, rHuPH20 के परिणामस्वरूप भ्रूण के वजन में कमी आई और मानव चिकित्सीय जोखिम से पर्याप्त रूप से प्रणालीगत जोखिम पर प्रत्यारोपण का नुकसान हुआ।
rHuPH20 के प्रणालीगत जोखिम के परिणामस्वरूप डिस्मॉर्फोजेनेसिस (यानी टेराटोजेनिसिटी) का कोई सबूत नहीं है।
06.0 फार्मास्युटिकल जानकारी
०६.१ अंश:
मानव पुनः संयोजक हयालूरोनिडेस (rHuPH20)
एल हिस्टडीन
एल-हिस्टिडाइन हाइड्रोक्लोराइड मोनोहाइड्रेट
ए, ए-ट्रेहलोज डाइहाइड्रेट
एल-मेथियोनीन
पॉलीसोर्बेट 80
इंजेक्शन के लिए पानी।
06.2 असंगति
MabThera सबक्यूटेनियस फॉर्मूलेशन और प्रोपलीन या पॉली कार्बोनेट सीरिंज, स्टेनलेस स्टील इंजेक्शन और ट्रांसफर नीडल्स या पॉलीइथाइलीन Luer कोन अटैचमेंट के बीच कोई असंगति नहीं देखी गई।
06.3 वैधता की अवधि
30 महीने
एक बार शीशी से सिरिंज में स्थानांतरित होने के बाद, MabThera उपचर्म सूत्रीकरण समाधान शारीरिक और रासायनिक रूप से 48 घंटों के लिए 2 ° C - 8 ° C पर और उसके बाद विसरित दिन के उजाले में 30 ° C पर 8 घंटे के लिए स्थिर रहता है।
सूक्ष्मजीवविज्ञानी दृष्टिकोण से उत्पाद का तुरंत उपयोग किया जाना चाहिए। यदि दवा का तुरंत उपयोग नहीं किया जाता है, तो नियंत्रित और मान्य सड़न रोकने वाली स्थितियों के तहत तैयारी होनी चाहिए। उपयोग में भंडारण समय और प्रशासन से पहले की शर्तें उपयोगकर्ता की जिम्मेदारी हैं।
06.4 भंडारण के लिए विशेष सावधानियां
एक रेफ्रिजरेटर (2 डिग्री सेल्सियस - 8 डिग्री सेल्सियस) में स्टोर करें। कंटेनर को प्रकाश से बचाने के लिए बाहरी कार्टन में रखें।
खोलने के बाद भंडारण की स्थिति के लिए, खंड 6.3 देखें।
06.5 तत्काल पैकेजिंग की प्रकृति और पैकेज की सामग्री
टाइप I ब्यूटाइल रबर स्टॉपर, एल्युमिनियम सील और गुलाबी प्रकार की प्लास्टिक डिस्क के साथ कांच की शीशी को साफ करता है भाड़ में जाओ, जिसमें 1400 मिलीग्राम / 11.7 एमएल मिलीग्राम रीटक्सिमैब होता है।
प्रत्येक पैक में एक शीशी होती है।
06.6 उपयोग और संचालन के लिए निर्देश
MabThera की आपूर्ति बाँझ, परिरक्षक मुक्त, गैर-पायरोजेनिक, एकल उपयोग शीशियों में की जाती है। सीरिंज और अन्य नुकीली वस्तुओं के उपयोग और निपटान के लिए निम्नलिखित बातों का कड़ाई से पालन किया जाना चाहिए:
• सुई और सीरिंज का कभी भी पुन: उपयोग नहीं करना चाहिए।
• सभी सुइयों और सीरिंज को एक शार्प कंटेनर (पंचर-प्रूफ डिस्पोजल कंटेनर) में रखें।
अप्रयुक्त दवा और इस दवा से प्राप्त कचरे को स्थानीय नियमों के अनुसार निपटाया जाना चाहिए।
07.0 विपणन प्राधिकरण धारक
रोश पंजीकरण लिमिटेड
6 फाल्कन वे
शायर पार्क
वेल्विन गार्डन सिटी
AL7 1TW
यूके
08.0 विपणन प्राधिकरण संख्या
ईयू / 1/98/067/003
033315033
09.0 प्राधिकरण के पहले प्राधिकरण या नवीनीकरण की तिथि
पहले प्राधिकरण की तिथि: 2 जून 1998
अंतिम नवीनीकरण की तिथि: 2 जून 2008
10.0 पाठ के संशोधन की तिथि
जनवरी 2015
11.0 रेडियो दवाओं के लिए, आंतरिक विकिरण मात्रा पर पूरा डेटा
12.0 रेडियो दवाओं के लिए, प्रायोगिक तैयारी और गुणवत्ता नियंत्रण पर अतिरिक्त विस्तृत निर्देश