डॉ. जियोवानी चेट्टा द्वारा संपादित
विशिष्ट प्रोटीन
ईसीएम में विशेष गैर-कोलेजन प्रोटीन की एक बड़ी (और अभी भी अच्छी तरह से परिभाषित नहीं) संख्या होती है, जिसमें आम तौर पर अन्य ईसीएम अणुओं और सेल सतह रिसेप्टर्स के लिए विशिष्ट बाध्यकारी साइटों के साथ कई डोमेन होते हैं। इस तरह, इन प्रोटीनों का प्रत्येक घटक समान और भिन्न अणुओं के बीच संपर्कों के "एम्पलीफायर" के रूप में कार्य करता है, एक अनंत जैव रासायनिक नेटवर्क बनाता है जो लाखों और लाखों की दूरी पर भी उत्पन्न, संशोधित, भिन्न और प्रचार करने में सक्षम है। जैव रासायनिक जानकारी (और ऊर्जावान)।
बाह्य मैट्रिक्स का एक महत्वपूर्ण विशिष्ट प्रोटीन फ़ाइब्रोनेक्टिन है, जो सभी कशेरुकियों में पाया जाने वाला एक उच्च आणविक भार ग्लाइकोप्रोटीन है। यह एक ग्लाइकोप्रोटीन डिमर है जो डाइसल्फ़ाइड पुलों से जुड़े दो बड़े उप-इकाइयों से बना है। फाइब्रोनेक्टिन विभिन्न तरीकों से विकास को प्रभावित करने में सक्षम प्रतीत होता है। सेलुलर, इंटरसेलुलर आसंजन और बाह्य मैट्रिक्स के साथ (ईसीएम के कोशिकाओं और अन्य अणुओं को बांधने की क्षमता रखता है, जैसे कोलेजन, फाइब्रिन, हेपरिन), सेल माइग्रेशन (सेल प्रति दिन 5 सेमी तक बढ़ सकता है - अल्बर्टाती, 2004) आदि। सबसे अच्छा ज्ञात आइसोफॉर्म, टाइप III, से बांधता है इंटेग्रिन. उत्तरार्द्ध ट्रांसमेम्ब्रेन प्रोटीन का एक परिवार है जो कोशिकाओं के आसंजन को की मान्यता के माध्यम से बाह्य मैट्रिक्स को प्रभावित करता है आरजीडी अनुक्रम. आरजीडी पेप्टाइड्स विभिन्न लंबाई की अमीनो एसिड श्रृंखलाएं हैं, जो साधारण ट्रिपेप्टाइड्स से शुरू होती हैं, जो अमीनो एसिड अनुक्रम आर्जिनिन-ग्लाइसिन-एसपारटिक एसिड की विशेषता है। यह अमीनो एसिड अनुक्रम जीव में सर्वव्यापी रूप से मौजूद है और कई शारीरिक कार्यों में शामिल है। यह आरजीडी अनुक्रम उन संरचनाओं में से एक का प्रतिनिधित्व करता है जो विशेष सेल लाइनों (जैसे भड़काऊ कोशिकाओं) के आसंजन की अनुमति देते हैं, ताकि वे अपना कार्य कर सकें। इंटीग्रिन और आरजीडी के बीच की कड़ी साइटोप्लाज्म में प्रतिक्रियाओं की एक श्रृंखला को प्रेरित करती है जिसमें साइटोस्केलेटन और अन्य प्रोटीन शामिल होते हैं जो सेल आसंजन, विकास और प्रवासन को नियंत्रित करते हैं। इसलिए इंटीग्रिन मैकेनोरिसेप्टर्स के रूप में कार्य करते हैं: वे चुनिंदा और एक मॉड्यूलर तरीके से, ट्रैक्शन और मैकेनिकल थ्रस्ट को ट्रांसड्यूस करते हैं। ईसीएम से सेल में और इसके विपरीत (हाइन्स, 2002)। अंत में, यह सच प्रतीत होता है कि फाइब्रोनेक्टिन तंतु व्यवस्थित होते हैं और केवल तनाव की उपस्थिति में ही सही ढंग से बनते हैं; यह खिंचाव स्वयं कोशिकाओं द्वारा उत्पन्न होता है (अल्बर्ट्स, 2002)।
ग्लूकोसामिनोग्लाइकेन्स (जीएजी) और प्रोटीयोग्लाइकेन्स (पीजी)
ग्लूकोसामिनोग्लाइकेन्स (जीएजीएस) और प्रोटीओग्लाइकेन्स (पीजी) संयोजी ऊतकों के भीतर परिभाषित एक अत्यधिक हाइड्रेटेड जेल जैसा पदार्थ बनाते हैं, जिसके भीतर फाइब्रिलर प्रोटीन रखे जाते हैं और इम्ब्रिकेट किए जाते हैं। पॉलीसेकेराइड जेल का यह रूप एक तरफ ईसीएम को काफी संपीड़ित ताकतों का विरोध करने की अनुमति देता है और दूसरी ओर रक्त और ऊतकों के बीच पोषक तत्वों, मेटाबोलाइट्स और हार्मोन के तेजी से और निरंतर प्रसार की अनुमति देता है।
जीएजी आमतौर पर सहसंयोजक रूप से एक प्रोटीन कोर से बंधते हैं, जिससे प्रोटीओग्लाइकेन्स (पीजीएस) को जन्म मिलता है। जीएजी और पीजी अकेले या समूहों में आसंजन अणुओं के लिए रिसेप्टर्स के रूप में या विकास कारकों, साइटोकिन्स और जमावट एंजाइमों जैसे परिसंचारी अणुओं पर जैव रासायनिक प्रक्रियाओं के उत्प्रेरक के रूप में कार्य करने में सक्षम हैं।
ग्लूकोसामिनोग्लाइकेन्स (जीएजी) को पॉलीसेकेराइड श्रृंखलाओं द्वारा दर्शाया जाता है जो कई बार दोहराई जाने वाली डिसैकराइड इकाइयों से बनी होती हैं। दो शर्कराओं में से एक हमेशा एक एमिनो चीनी (एन-एसिटाइलग्लुकोसामाइन या एन-एसिटाइलगैलेक्टोसामाइन) द्वारा लगभग हमेशा सल्फेट द्वारा दर्शाया जाता है। दूसरी चीनी आमतौर पर ग्लुकुरोनिक एसिड या इसका आइड्यूरोनिक आइसोमर एल है। जीएजी के 4 प्रमुख समूह हैं: हयालूरोनन्स, चोंड्रोइटिन सल्फेट्स और डर्माटन सल्फेट्स, हेपरान सल्फेट्स, केराटनसल्फेट्स।
ग्लूकोसामिनोग्लाइकेन्स की पॉलीसेकेराइड श्रृंखलाएं पॉलीपेप्टाइड श्रृंखलाओं की विशिष्ट गोलाकार संरचनाओं के अंदर मोड़ने के लिए वॉल्यूमेट्रिक रूप से बहुत कठोर हैं, साथ ही वे अत्यधिक हाइड्रोफिलिक हैं। इन कारणों से (और शायद हमारे लिए अज्ञात अन्य लोगों के लिए भी) जीएजी अत्यधिक अनुरूपता ग्रहण करते हैं। विस्तारित, अपने द्रव्यमान के संबंध में एक बड़ी मात्रा में कब्जा कर लेते हैं और इस प्रकार कम सांद्रता पर भी काफी मात्रा में जेल बनाते हैं। नकारात्मक चार्ज की उच्च मात्रा (जीएजी सबसे अधिक आयनिक कोशिकाओं का प्रतिनिधित्व करते हैं, आमतौर पर पशु कोशिकाओं द्वारा उत्पादित, सल्फेटेड होते हैं) कई उद्धरणों को आकर्षित करते हैं; इनमें से एक प्रमुख भूमिका Na + द्वारा निभाई जाती है जो पूरी आसमाटिक क्षमता देता है और ECM में भारी मात्रा में पानी को फंसा देता है। इस तरह, सूजन (टर्गर्स) उत्पन्न होते हैं जो ईसीएम को महत्वपूर्ण संपीड़न बलों का भी विरोध करने की अनुमति देते हैं (इसके लिए धन्यवाद, उदाहरण के लिए, कूल्हे की उपास्थि, शारीरिक परिस्थितियों में, कई सौ वायुमंडल के दबाव का पूरी तरह से विरोध कर सकती है)।
संयोजी ऊतक के अंदर, जीएजी वैश्विक वजन के 10-12% से कम का प्रतिनिधित्व करते हैं, हालांकि, उनकी विशेषताओं के लिए धन्यवाद, वे कई बाह्य रिक्त स्थान भरते हैं, विभिन्न आकारों और विद्युत आवेशों के घनत्व के हाइड्रेटेड जेल के छिद्र बनाते हैं, इस प्रकार कार्य करते हैं चुनिंदा प्रमुख बिंदुओं या "सर्वर" से जिसके माध्यम से MEC के अंदर अणुओं और कोशिकाओं के यातायात को उनके आकार, वजन और विद्युत आवेश के आधार पर नियंत्रित किया जाता है।
Hyaluronic एसिड (hyaluronan, hyaluronate) शायद GAGs का सबसे सरल प्रतिनिधित्व करता है। मनुष्य में यह लगभग 25,000 समान गैर-सल्फेटेड डिसैकराइड से बना होता है और आमतौर पर किसी भी "प्रोटीन कोर" से जुड़ा नहीं होता है, इसलिए इसकी एक असामान्य संरचना होती है। प्रायोगिक और आणविक-जैविक डेटा इस बात की पुष्टि करते हैं कि यह काफी दबावों के प्रतिरोध के संदर्भ में हड्डियों और जोड़ों के स्तर पर एक मौलिक भूमिका निभाता है। इसके अलावा, यह भ्रूण के विकास के दौरान ईसीएम में रिक्त स्थान भरने में एक बहुत ही महत्वपूर्ण भूमिका निभाता है: यह कोशिकाओं के बीच रिक्त स्थान बनाता है जिसमें वे बाद के चरणों में प्रवास करेंगे (अल्बर्गटी, 2004)।
जीएजी और पीजी, एक दूसरे के साथ जुड़कर, ईसीएम में विशाल बहुलक परिसरों को जन्म दे सकते हैं। उदाहरण के लिए . के अणु एग्रेकेनो, जो संयुक्त स्तर पर अधिकांश पीजी का प्रतिनिधित्व करते हैं, गैर-सहसंयोजक बंधनों के माध्यम से हाइलूरोनिक एसिड के साथ गठबंधन करते हैं, जिससे एक जीवाणु के आकार को एकत्रित किया जाता है।
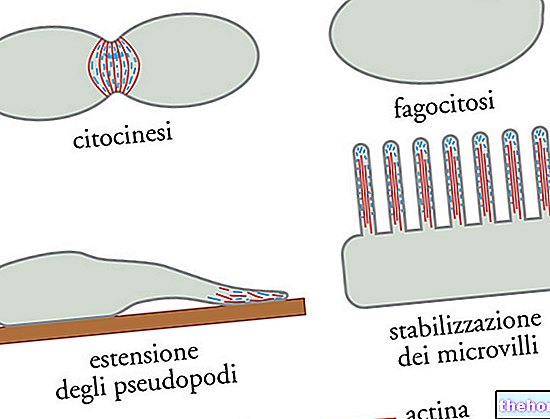
सभी पीजी ईसीएम द्वारा स्रावित नहीं होते हैं, कुछ प्लाज्मा झिल्ली के अभिन्न अंग हैं। सबसे अच्छी तरह से ज्ञात झिल्ली पीजी में, i सिंडीकैंस उनके पास जीएजी की तीन श्रृंखलाओं से बना एक बाह्य डोमेन है, जबकि इंट्रासेल्युलर को सेलुलर साइटोस्केलेटन (अल्बर्ट्स, 2002) के एक्टिन के साथ प्रतिक्रिया करने में सक्षम माना जाता है।
"Fibronectin, Glucosaminoglycans and Proteoglycans" पर अन्य लेख
- कोलेजन और इलास्टिन, बाह्य मैट्रिक्स में कोलेजन फाइबर
- कोशिकी साँचा
- सेलुलर संतुलन में बाह्य मैट्रिक्स का महत्व
- बाह्य मैट्रिक्स और विकृति के परिवर्तन
- संयोजी ऊतक और बाह्य मैट्रिक्स
- गहरी प्रावरणी - संयोजी ऊतक
- फेशियल मैकेनोरिसेप्टर्स और मायोफिब्रोब्लास्ट्स
- गहरी प्रावरणी बायोमैकेनिक्स
- मुद्रा और गतिशील संतुलन
- तन्यता और पेचदार गतियाँ
- निचले अंग और शरीर की गति
- ब्रीच सपोर्ट और स्टोमेटोगैथिक उपकरण
- नैदानिक मामले, पोस्टुरल परिवर्तन
- नैदानिक मामले, मुद्रा
- पोस्टुरल मूल्यांकन - नैदानिक मामला
- ग्रंथ सूची - बाह्य मैट्रिक्स से आसन तक। क्या कनेक्टिव सिस्टम हमारा सच्चा Deus ex machina है?