परिभाषा
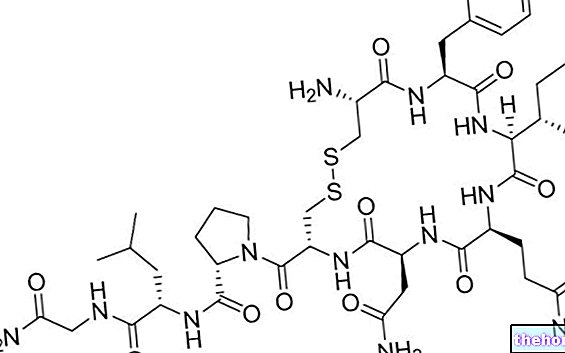
एंजाइम पौधे और पशु कोशिकाओं में उत्पादित प्रोटीन होते हैं, जो बिना संशोधित किए जैविक प्रतिक्रियाओं को तेज करने वाले उत्प्रेरक के रूप में कार्य करते हैं।
एंजाइम एक विशिष्ट पदार्थ के साथ मिलकर इसे एक अलग पदार्थ में बदलने का काम करते हैं; क्लासिक उदाहरण लार, पेट, अग्न्याशय और छोटी आंत में मौजूद पाचन एंजाइमों द्वारा दिए जाते हैं, जो पाचन में एक आवश्यक कार्य करते हैं और भोजन को बुनियादी घटकों में तोड़ने में मदद करते हैं, जिसे बाद में शरीर द्वारा अवशोषित और उपयोग किया जा सकता है, अन्य एंजाइमों द्वारा संसाधित किया जा सकता है या अपशिष्ट के रूप में उत्सर्जित।
प्रत्येक एंजाइम की एक विशिष्ट भूमिका होती है: वह जो वसा को तोड़ता है, उदाहरण के लिए, प्रोटीन या कार्बोहाइड्रेट पर कार्य नहीं करता है। जीव की भलाई के लिए एंजाइम आवश्यक हैं। एक एंजाइम की भी कमी, गंभीर गड़बड़ी का कारण बन सकती है। एक प्रसिद्ध उदाहरण फेनिलकेटोनुरिया (पीकेयू) है, जो एक आवश्यक अमीनो एसिड को चयापचय करने में असमर्थता की विशेषता वाली बीमारी है, फेनिलएलनिन, जिसके संचय से शारीरिक विकृति और मानसिक बीमारियां हो सकती हैं।
जैव रासायनिक अध्ययन
एंजाइम विशेष प्रोटीन होते हैं जिनमें जैविक उत्प्रेरक होने की विशेषता होती है, अर्थात, वे एक प्रतिक्रिया की सक्रियता ऊर्जा (ईट) को तोड़ने की क्षमता रखते हैं, इसके पथ को संशोधित करते हैं ताकि गतिज रूप से धीमी प्रक्रिया तेज हो।
एंजाइम थर्मोडायनामिक रूप से संभावित प्रतिक्रियाओं के कैनेटीक्स को बढ़ाते हैं और उत्प्रेरक के विपरीत, वे कमोबेश विशिष्ट होते हैं: इसलिए उनके पास सब्सट्रेट विशिष्टता होती है।
एंजाइम प्रतिक्रिया के स्टोइकोमेट्री में शामिल नहीं है: ऐसा होने के लिए, अंतिम उत्प्रेरक साइट प्रारंभिक एक के समान होनी चाहिए।
उत्प्रेरक क्रिया में लगभग हमेशा एक धीमा चरण होता है जो प्रक्रिया की गति को निर्धारित करता है।
जब हम एंजाइमों के बारे में बात करते हैं तो संतुलन प्रतिक्रियाओं के बारे में बात करना सही नहीं है, हम इसके बजाय बोलते हैं स्थिर अवस्था (वह अवस्था जिसमें एक निश्चित मेटाबोलाइट बनता है और लगातार खपत होता है, इसकी एकाग्रता समय के साथ लगभग स्थिर रहती है)। एक एंजाइम द्वारा उत्प्रेरित प्रतिक्रिया का उत्पाद आमतौर पर बाद की प्रतिक्रिया के लिए एक प्रतिक्रियाशील होता है, जो दूसरे एंजाइम द्वारा उत्प्रेरित होता है, और इसी तरह।
एंजाइमों द्वारा उत्प्रेरित प्रक्रियाओं में आमतौर पर प्रतिक्रियाओं के क्रम होते हैं।
एक एंजाइम (ई) द्वारा उत्प्रेरित एक सामान्य प्रतिक्रिया को निम्नानुसार संक्षेपित किया जा सकता है:

ई एंजाइम है
एस सब्सट्रेट है;
ES एंजाइम और सब्सट्रेट के बीच जोड़ का प्रतिनिधित्व करता है;
पी उत्पाद है;
K प्रतिक्रिया की दर स्थिरांक है।
एक सामान्य एंजाइम (ई) सब्सट्रेट (एस) के साथ मिलकर एक दर स्थिर K1 के साथ जोड़ (ES) बनाता है; यह दर स्थिर K2 के साथ, E + S में वापस अलग हो सकता है, या, (यदि "जीवन" लंबे समय तक रहता है) ) गति स्थिरांक K3 के साथ P बनाने के लिए आगे बढ़ सकता है।
उत्पाद (पी), बदले में, एंजाइम के साथ पुनर्संयोजन कर सकता है और दर स्थिर K4 के साथ जोड़ में सुधार कर सकता है।
जब एंजाइम और सब्सट्रेट मिश्रित होते हैं, तो समय का एक अंश होता है जिसमें दो प्रजातियों के बीच बैठक अभी तक नहीं हुई है: यानी, एक बहुत ही कम समय अंतराल है (जो प्रतिक्रिया पर निर्भर करता है) जिसमें एंजाइम और सब्सट्रेट होते हैं अभी तक नहीं मिला है, इस अवधि के बाद, एंजाइम और सब्सट्रेट बढ़ती मात्रा में संपर्क में आते हैं और ES व्यसन का निर्माण होता है। इसके बाद, एंजाइम सब्सट्रेट पर कार्य करता है और उत्पाद जारी किया जाता है। तब यह कहा जा सकता है कि c "एक प्रारंभिक समय अंतराल है जिसमें ES व्यसन की एकाग्रता को परिभाषित नहीं किया जा सकता है; इस अवधि के बाद, यह माना जाता है कि एक स्थिर स्थिति स्थापित किया जाता है, अर्थात्, जोड़ प्राप्त करने वाली प्रक्रियाओं की गति उन प्रक्रियाओं की गति के बराबर होती है जो व्यसन के विनाश की ओर ले जाती हैं।
माइकलिस-मेंटेन स्थिरांक (केएम) एक संतुलन स्थिरांक है (ऊपर वर्णित पहले संतुलन के लिए संदर्भित); यह कहा जा सकता है, एक अच्छे सन्निकटन के साथ (क्योंकि K3 को भी माना जाना चाहिए), कि KM को गतिज स्थिरांक K2 और K1 के बीच के अनुपात द्वारा दर्शाया गया है (ऊपर वर्णित पहले संतुलन में जोड़ ES के विनाश और गठन के लिए संदर्भित) .
माइकलिस-मेंटेन स्थिरांक के माध्यम से हमारे पास "एंजाइम और सब्सट्रेट के बीच संबंध का संकेत है: यदि केएम छोटा सी है" एंजाइम और सब्सट्रेट के बीच एक "उच्च आत्मीयता है, तो ईएस जोड़ स्थिर है।
एंजाइम विनियमन (या मॉड्यूलेशन) के अधीन हैं।
अतीत में मुख्य रूप से नकारात्मक मॉड्यूलेशन की बात होती थी, यानी एंजाइम की उत्प्रेरक क्षमताओं का निषेध लेकिन, एक सकारात्मक मॉड्यूलेशन भी हो सकता है, यानी ऐसी प्रजातियां हैं जो एक एंजाइम की उत्प्रेरक क्षमताओं को बढ़ाने में सक्षम हैं।
4 प्रकार के अवरोध हैं (गणितीय समीकरणों के साथ प्रयोगात्मक डेटा का मिलान करने के लिए एक मॉडल पर किए गए अनुमानों से प्राप्त):
- प्रतिस्पर्धी निषेध
- गैर-प्रतिस्पर्धी निषेध
- अप्रतिस्पर्धी निषेध
- प्रतिस्पर्धी निषेध
हम प्रतिस्पर्धी निषेध की बात करते हैं जब एक अणु (अवरोधक) सब्सट्रेट के साथ प्रतिस्पर्धा करने में सक्षम होता है।संरचनात्मक समानता के लिए, अवरोधक सब्सट्रेट के स्थान पर प्रतिक्रिया कर सकता है; इसलिए शब्दावली "प्रतिस्पर्धी अवरोध"। एंजाइम के अवरोधक या सब्सट्रेट से बंधे होने की संभावना दोनों की एकाग्रता और एंजाइम के साथ उनकी आत्मीयता पर निर्भर करती है; इसलिए प्रतिक्रिया दर इन कारकों पर निर्भर करती है।
अवरोधक की उपस्थिति के बिना समान प्रतिक्रिया दर प्राप्त करने के लिए, उच्च सब्सट्रेट एकाग्रता होना आवश्यक है।
यह प्रयोगात्मक रूप से दिखाया गया है कि, एक अवरोधक की उपस्थिति में, माइकलिस-मेन्टेन निरंतर बढ़ता है।
के संबंध में, इसके बजाय, "गैर-प्रतिस्पर्धी निषेध, अणु के बीच की बातचीत जो एक न्यूनाधिक (सकारात्मक या नकारात्मक-अवरोधक) और" एंजाइम के रूप में कार्य करना चाहिए, एक ऐसी साइट में होती है जो उस साइट से अलग होती है जिसमें बातचीत होती है एंजाइम और सब्सट्रेट के बीच होता है; इसलिए हम एलोस्टेरिक मॉडुलन की बात करते हैं (यूनानी से) एलोस्टेरोस → अन्य साइट)।
यदि अवरोधक एंजाइम को बांधता है, तो यह एंजाइम की संरचना में बदलाव ला सकता है और इसके परिणामस्वरूप, उस दक्षता को कम कर सकता है जिसके साथ सब्सट्रेट एंजाइम को बांधता है।
इस प्रकार की प्रक्रिया में, माइकलिस-मेंटेन स्थिरांक स्थिर रहता है क्योंकि यह मान एंजाइम और सब्सट्रेट के बीच संतुलन पर निर्भर करता है और यहां तक कि एक अवरोधक की उपस्थिति में भी, ये संतुलन नहीं बदलता है।
अप्रतिस्पर्धी निषेध की घटना दुर्लभ है; एक विशिष्ट अप्रतिस्पर्धी अवरोधक एक ऐसा पदार्थ है जो ES व्यसन से विपरीत रूप से बंधता है और ESI को जन्म देता है:

सब्सट्रेट की अधिकता से अवरोध कभी-कभी अप्रतिस्पर्धी हो सकता है, क्योंकि यह तब होता है जब एक दूसरा सब्सट्रेट अणु ES कॉम्प्लेक्स से जुड़ जाता है, जिससे ESS कॉम्प्लेक्स को जन्म दिया जाता है।
दूसरी ओर, एक प्रतिस्पर्धी अवरोधक, केवल पिछले मामले की तरह ही सब्सट्रेट एंजाइम एडक्ट से बंध सकता है: सब्सट्रेट को मुक्त एंजाइम से बांधना एक गठनात्मक संशोधन को प्रेरित करता है जो साइट को अवरोधक के लिए सुलभ बनाता है।
माइकलिस मेंटेन स्थिरांक कम हो जाता है क्योंकि अवरोधक एकाग्रता बढ़ जाती है: जाहिर है, इसलिए सब्सट्रेट के लिए एंजाइम की आत्मीयता बढ़ जाती है।
सेरीन प्रोटीज
वे एंजाइमों का एक परिवार हैं जिनसे काइमोट्रिप्सिन और ट्रिप्सिन संबंधित हैं।
काइमोट्रिप्सिन एक प्रोटीयोलाइटिक और हाइड्रोलाइटिक एंजाइम है जो हाइड्रोफोबिक और एरोमैटिक अमीनो एसिड के दाईं ओर कट जाता है।
जीन का उत्पाद जो काइमोट्रिप्सिन के लिए कोड करता है वह सक्रिय नहीं है (यह एक कमांड के साथ सक्रिय होता है); काइमोट्रिप्सिन के निष्क्रिय रूप को 245 अमीनो एसिड की पॉलीपेप्टाइड श्रृंखला द्वारा दर्शाया गया है। पांच डाइसल्फ़ाइड पुलों और अन्य मामूली अंतःक्रियाओं (इलेक्ट्रोस्टैटिक, वैन डेर वाल्स बल, हाइड्रोजन बांड, आदि) के कारण काइमोट्रिप्सिन का गोलाकार आकार होता है।
काइमोट्रिप्सिन अग्न्याशय के काइमोस कोशिकाओं द्वारा निर्मित होता है जहां यह विशेष झिल्ली में निहित होता है और भोजन के पाचन के समय अग्नाशयी वाहिनी के माध्यम से आंत में निष्कासित होता है: काइमोट्रिप्सिन वास्तव में एक पाचक एंजाइम है। प्रोटीन और पोषक तत्व जो हम आहार के माध्यम से ग्रहण करते हैं, पाचन के अधीन होते हैं और छोटी श्रृंखलाओं में कम हो जाते हैं और अवशोषित हो जाते हैं और ऊर्जा में परिवर्तित हो जाते हैं (जैसे एमाइलेज और प्रोटीज पोषक तत्वों को ग्लूकोज और अमीनो एसिड में तोड़ देते हैं जो रक्त वाहिकाओं के माध्यम से कोशिकाओं तक पहुंचते हैं। वे पोर्टल शिरा तक पहुँचते हैं और वहाँ से उन्हें लीवर तक पहुँचाया जाता है जहाँ वे आगे के उपचार से गुजरते हैं)।
एंजाइम एक गैर-सक्रिय रूप में निर्मित होते हैं और केवल तभी सक्रिय होते हैं जब वे "उस स्थान पर पहुँचते हैं जहाँ उन्हें काम करना चाहिए"; एक बार उनकी कार्रवाई समाप्त हो जाने के बाद, उन्हें निष्क्रिय कर दिया जाता है। एक एंजाइम, एक बार निष्क्रिय हो जाने पर, पुन: सक्रिय नहीं किया जा सकता है: "आगे उत्प्रेरक क्रिया करने के लिए, इसे एक अन्य एंजाइम अणु द्वारा प्रतिस्थापित किया जाना चाहिए"। यदि अग्न्याशय में पहले से ही सक्रिय रूप में काइमिट्रिप्सिन का उत्पादन किया गया था, तो यह बाद वाले पर हमला करेगा: अग्नाशयशोथ पाचन एंजाइमों के कारण विकृति है जो पहले से ही अग्न्याशय में सक्रिय हैं (और आवश्यक साइटों में नहीं); उनमें से कुछ अगर समय पर इलाज नहीं किया जाता है, मौत की ओर ले जाते हैं।
काइमोट्रिप्सिन और सभी सेरीन प्रोटीज में, उत्प्रेरक क्रिया एक सेरीन की साइड चेन में अल्कोहल आयन (-CH2O-) के अस्तित्व के कारण होती है।
सेरीन प्रोटीज इस नाम को ठीक से लेते हैं क्योंकि उनकी उत्प्रेरक क्रिया एक सेरीन के कारण होती है।
एक बार जब सभी एंजाइम ने अपना कार्य किया है, तो सब्सट्रेट पर फिर से काम करने में सक्षम होने से पहले, इसे पानी से बहाल किया जाना चाहिए; पानी द्वारा सेरीन की "रिलीज" प्रक्रिया का सबसे धीमा चरण है, और यह यह चरण है जो उत्प्रेरण की गति को निर्धारित करता है।
उत्प्रेरक क्रिया दो चरणों में होती है:
- उत्प्रेरक गुणों के साथ आयनों का निर्माण (आयन अल्कोहल) और कार्बोनिल कार्बन (सी = ओ) पर बाद में न्यूक्लियोफिलिक हमले पेप्टाइड बंधन के दरार और एस्टर के गठन के साथ;
- उत्प्रेरक की बहाली के साथ पानी का हमला (अपनी उत्प्रेरक क्रिया को फिर से करने में सक्षम)।
सेरीन प्रोटीज परिवार से संबंधित विभिन्न एंजाइम विभिन्न अमीनो एसिड से बने हो सकते हैं, लेकिन उन सभी के लिए, उत्प्रेरक साइट को सेरीन की साइड चेन के अल्कोहल आयन द्वारा दर्शाया जाता है।
सेरीन प्रोटीज का एक उपपरिवार जमावट में शामिल एंजाइमों का होता है (जिसमें प्रोटीन का परिवर्तन होता है, उनके निष्क्रिय रूप से "एक अन्य रूप जो सक्रिय होता है)। ये एंजाइम सुनिश्चित करते हैं कि जमावट यथासंभव प्रभावी है और इसमें सीमित है स्थान और समय (जमावट जल्दी होनी चाहिए और केवल घायल क्षेत्र के आसपास ही होनी चाहिए)। जमावट में शामिल एंजाइम एक कैस्केड में सक्रिय होते हैं (एक एंजाइम के सक्रियण से, अरबों एंजाइम प्राप्त होते हैं: प्रत्येक सक्रिय एंजाइम , बदले में कई अन्य एंजाइमों को सक्रिय करता है)।
घनास्त्रता जमावट एंजाइमों की खराबी के कारण एक विकृति है: यह सक्रियण के कारण होता है, बिना आवश्यकता के (क्योंकि कोई चोट नहीं है), जमावट में उपयोग किए जाने वाले एंजाइमों की।
अन्य एंजाइमों के लिए नियामक (नियामक) एंजाइम और निरोधात्मक एंजाइम होते हैं: बाद वाले के साथ बातचीत करते हुए, वे अपनी गतिविधि को विनियमित या बाधित करते हैं; यहां तक कि एक एंजाइम का उत्पाद भी एंजाइम के लिए अवरोधक हो सकता है। ऐसे एंजाइम भी होते हैं जो जितना अधिक काम करते हैं, उतना ही अधिक सब्सट्रेट मौजूद होता है।
लाइसोजाइम
लुइगी पाश्चर ने पेट्री डिश पर छींकने से पता लगाया कि बलगम में एक एंजाइम होता है जो बैक्टीरिया को मारने में सक्षम होता है: लाइसोजाइम; ग्रीक से: लिसो = किस आकार; ज़िमो = एंजाइम।
लाइसोजाइम बैक्टीरिया की कोशिका भित्ति को तोड़ने में सक्षम है। बैक्टीरिया, और सामान्य रूप से एककोशिकीय जीवों को यांत्रिक रूप से प्रतिरोधी संरचनाओं की आवश्यकता होती है जो उनके आकार को सीमित करते हैं; बैक्टीरिया के अंदर बहुत अधिक आसमाटिक दबाव होता है इसलिए वे पानी को आकर्षित करते हैं। प्लाज़्मा झिल्ली फट जाती यदि कोई कोशिका भित्ति नहीं होती जो पानी के प्रवेश का विरोध करती है और जीवाणु की मात्रा को सीमित करती है।
सेल की दीवार में एक पॉलीसेकेराइड श्रृंखला होती है जिसमें एन-एसिटाइल-ग्लूकोसामाइन (एनएजी) के अणु और एन-एसिटाइल-मुरामिक एसिड (एनएएम) के अणु वैकल्पिक होते हैं; एनएजी और एनएएम के बीच का बंधन हाइड्रोलिसिस से टूट जाता है। NAM का कार्बोक्सिल समूह, कोशिका भित्ति में, एक अमीनो एसिड के साथ पेप्टाइड बॉन्ड में लगा होता है।
विभिन्न शृंखलाओं के बीच, छद्म-पेप्टाइड बंधों से बने पुलों का निर्माण होता है: शाखाकरण लाइसिन अणु के कारण होता है; समग्र रूप से संरचना बहुत शाखित है और यह इसे एक उच्च स्थिरता प्रदान करती है।
लाइसोजाइम एक एंटीबायोटिक है (बैक्टीरिया को मारता है): यह बैक्टीरिया की दीवार में दरार बनाकर काम करता है; जब यह संरचना (जो यांत्रिक रूप से प्रतिरोधी होती है) टूट जाती है, तो जीवाणु फटने तक पानी खींचता है। लाइसोजाइम एनएएम और एनएजी के बीच β-1,4 ग्लूकोसिडिक बंधन को तोड़ने का प्रबंधन करता है।
लाइसोजाइम की उत्प्रेरक साइट को एक खांचे द्वारा दर्शाया जाता है जो एंजाइम के साथ चलता है जिसमें पॉलीसेकेराइड श्रृंखला डाली जाती है: श्रृंखला के छह ग्लूकोसिडिक रिंग खांचे में रखे जाते हैं।
ग्रूव सी की स्थिति तीन में "एक चोक है: इस स्थिति में केवल एक एनएजी रखा जा सकता है, क्योंकि एनएएम, जो उच्च आयामों का है, प्रवेश नहीं कर सकता है। वास्तविक उत्प्रेरक साइट चार और पांच पदों के बीच है: चूंकि एक है एनएजी तीसरे स्थान पर, कट एनएएम और एनएजी के बीच होगा (और इसके विपरीत नहीं); इसलिए, कटौती विशिष्ट है।
लाइसोजाइम के काम करने के लिए इष्टतम पीएच पांच है। एंजाइम की उत्प्रेरक साइट में, यानी चार और पांच स्थितियों के बीच, एक एसपारटिक एसिड और एक ग्लूटामिक एसिड की साइड चेन होती हैं।
होमोलॉजी की डिग्री: प्रोटीन संरचनाओं के बीच रिश्तेदारी (यानी समानता) को मापता है।
लाइसोजाइम और लैक्टोज-सिंथेज के बीच एक मजबूत संबंध है।
लैक्टोज सिंथेटेस लैक्टोज को संश्लेषित करता है (जो मुख्य दूध चीनी है): लैक्टोज एक गैलेक्टोसिल ग्लूकोसाइड है जिसमें सी "गैलेक्टोज और ग्लूकोज के बीच एक β-1,4 ग्लूकोसिडिक बंधन है।
इसलिए, लैक्टोज सिंथेटेस लाइसोजाइम द्वारा उत्प्रेरित प्रतिक्रिया के विपरीत उत्प्रेरित करता है (जो बदले में β-1,4 ग्लूकोसिडिक बंधन को विभाजित करता है)
लैक्टोज सिंथेटेस एक डिमर है, अर्थात यह दो प्रोटीन श्रृंखलाओं से बना होता है, जिनमें से एक में उत्प्रेरक गुण होते हैं और यह लाइसोजाइम के बराबर होता है और दूसरा एक नियामक सबयूनिट होता है।
गर्भावस्था के दौरान, ग्लाइकोप्रोटीन को स्तन ग्रंथि की कोशिकाओं द्वारा गैलाटोसिल-ट्रांसफेरेज़ की क्रिया द्वारा संश्लेषित किया जाता है (इसमें "लाइसोज़ाइम के साथ 40% का अनुक्रम समरूपता है): यह एंजाइम एक गैलेक्टोसिल समूह को एक उच्च-ऊर्जा संरचना से स्थानांतरित करने में सक्षम है। एक ग्लाइकोप्रोटीन संरचना। गर्भावस्था के दौरान, जीन की अभिव्यक्ति जो गैलेक्टोसिसिल-ट्रांसफरेज़ के लिए कोड करती है, प्रेरित होती है (अन्य जीन की अभिव्यक्ति भी होती है जो अन्य उत्पाद भी देती है): स्तन के आकार में वृद्धि होती है क्योंकि यह सक्रिय होता है स्तन ग्रंथि (पहले निष्क्रिय) जिसे दूध का उत्पादन करना चाहिए। प्रसव के दौरान, α-lactalbumin का उत्पादन होता है जो एक नियामक प्रोटीन है: यह गैलेक्टोसिल-ट्रांसफरेज़ (सब्सट्रेट के भेदभाव से) की उत्प्रेरक क्षमता को विनियमित करने में सक्षम है। α-lactalalbumin द्वारा संशोधित गैलेक्टोसिल-ट्रांसफरेज़ एक ग्लूकोज अणु पर एक गैलेक्टोसिल को स्थानांतरित करने में सक्षम है: एक β-1,4 ग्लाइकोसिडिक बंधन बनाता है और लैक्टोज (लैक्टोज सिंथेटेज़) देता है।
इसलिए, गैलेक्टोज ट्रांसफरेज प्रसव से पहले स्तन ग्रंथि तैयार करता है और प्रसव के बाद दूध का उत्पादन करता है।
ग्लाइकोप्रोटीन का उत्पादन करने के लिए, गैलेक्टोसिल ट्रांसफ़ेज़ एक गैलेक्टोसिल और एक एनएजी से बंधता है; बच्चे के जन्म के दौरान लैक्टल एल्ब्यूमिन गैलेक्टोसिलट्रांसफेरेज से बंध जाता है जिससे बाद वाला ग्लूकोज को पहचान लेता है और अब लैक्टोज देने के लिए एनएजी नहीं रह जाता है।


.jpg)